Clear Sky Science · nl
Ruimtelijk‐tijdelijke transcriptomica van de hersenen onthult risicogene-hotspots bij belangrijke neuropsychiatrische aandoeningen
Waarom timing in de hersenen ertoe doet
Veel psychiatrische en neurologische aandoeningen doen zich op specifieke leeftijden voor, van autisme in de kindertijd tot de ziekte van Alzheimer op latere leeftijd. Deze studie stelt een eenvoudige maar krachtige vraag: zijn de genen die het risico op deze aandoeningen verhogen het meest actief in de hersenen op dezelfde tijden en locaties waarop de symptomen gewoonlijk optreden? Door te traceren wanneer en waar risicogenen tijdens de menselijke hersenontwikkeling aan gaan, brengen de auteurs kwetsbaarheids-"hotspots" in kaart die kunnen helpen verklaren wie ziek wordt, wanneer, en waarom bepaalde hersencircuits betrokken zijn.
Risicogenen volgen gedurende het leven
Om deze kaart te maken combineerden de onderzoekers meerdere grote openbare datasets die meten welke genen actief zijn in verschillende delen van de menselijke hersenen, vanaf de vroege zwangerschap tot de volwassenheid. Ze richtten zich op risicogenen geïdentificeerd door grote genetische studies voor 15 kenmerken, waaronder intelligentie, autisme, aandachtstekort-/hyperactiviteitsstoornis, Tourette, obsessief-compulsieve stoornis, stemmings- en angststoornissen, epilepsie en degeneratieve ziekten zoals Alzheimer en Parkinson. Voor elk kenmerk onderzochten ze of de risicogenen meer gebruikt werden dan verwacht in bepaalde hersenregio’s, leeftijden of celtypen, met behulp van zowel bundelweefsel- als enkelcelgegevens, waarbij verrijking werd opgevat als een teken van verhoogde kwetsbaarheid.
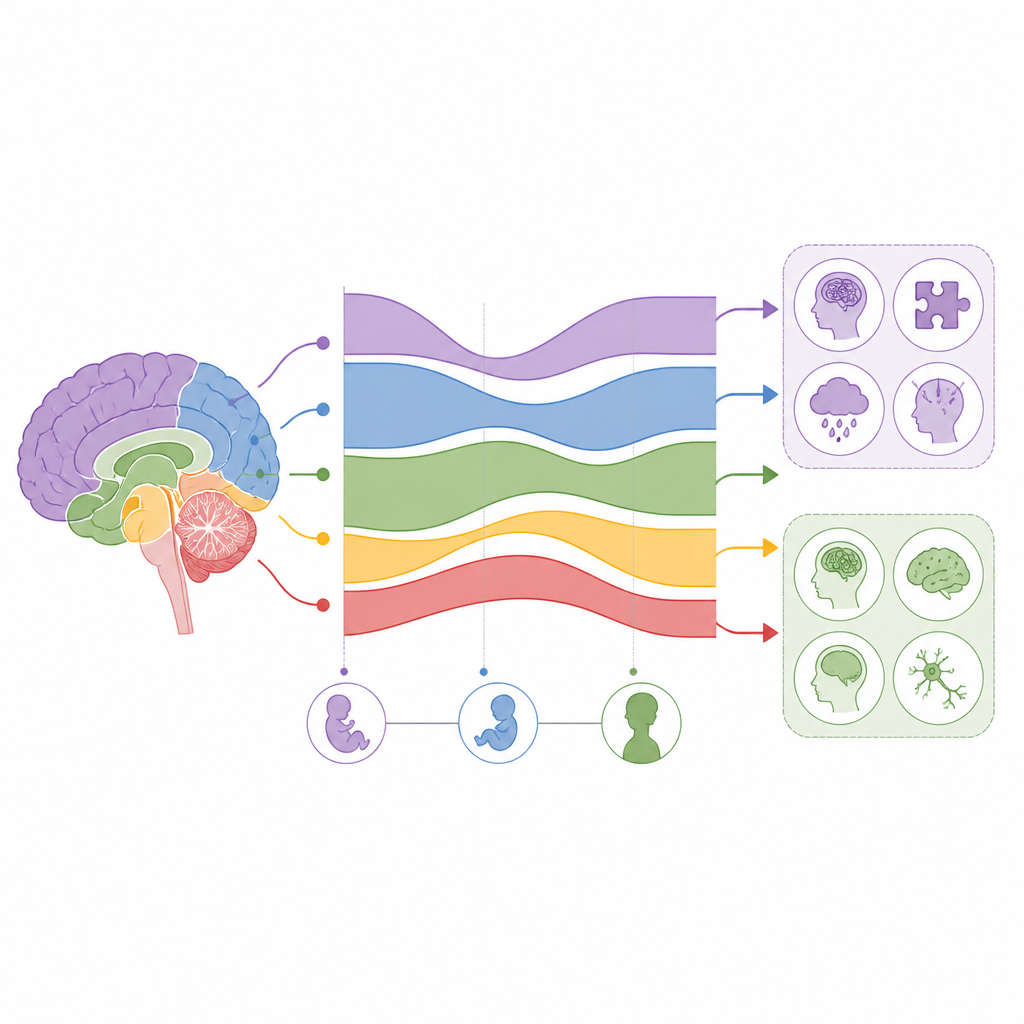
Kwetsbaarheid in vroege versus latere levensfasen
Er kwam een duidelijk patroon naar voren: kenmerken die doorgaans in de kindertijd beginnen, zoals autisme, ADHD, Tourette en hogere of lagere intelligentie, vertoonden de sterkste risicogene-activiteit vóór de geboorte. Daarentegen lieten aandoeningen die meestal op volwassen leeftijd optreden, waaronder epilepsie, de ziekte van Alzheimer en Parkinson, piekactiviteit van hun risicogenen na de geboorte zien, vaak in de middelbare leeftijd. Sommige aandoeningen, met name ernstige depressie, obsessief-compulsieve stoornis en schizofrenie, hadden complexere profielen, waarbij risicogenen zowel rond de geboorte als opnieuw in de adolescentie of jongvolwassenheid opduiken. Over het geheel genomen volgde de timing van risicogene-activiteit ruwweg de typische leeftijd waarop symptomen pieken, wat het idee ondersteunt dat veel van deze aandoeningen voortkomen uit langdurige ontwikkelingsprocessen in plaats van plotselinge gebeurtenissen.
Hersencircuits als risicohotspots
De studie wees ook aan waar in de hersenen deze risicogenen het meest actief zijn. Veel psychiatrische kenmerken deelden een brede betrokkenheid van de cortex, die denken, plannen en sociaal gedrag ondersteunt. Er waren echter noemenswaardige verschillen in diepere structuren. Risicogenen voor ADHD waren bijzonder verrijkt in de thalamus en het striatum, belangrijke knooppunten voor aandacht en bewegingscontrole, terwijl genen die met paniekstoornis en neuroticisme geassocieerd werden, oplichtten in de amygdala, een centrum voor emotie en angst. Obsessief-compulsieve stoornis toonde sterke verrijking in striatum, thalamus en cerebellum, in overeenstemming met lang bestaande circuitmodellen van de aandoening. Daarentegen waren risicogenen voor autisme, Tourette en schizofrenie relatief uitgeput in veel subcorticale regio’s, wat wijst op een meer uitgesproken corticale oorsprong.
Inzoomen op cellen en moleculaire routes
Om mechanismen te begrijpen, groepeerden de auteurs genen die de neiging hebben om samen aan te gaan in co-expressie-"modules" en onderzochten welke modules verrijkt waren voor risicogenen en wanneer en waar ze actief waren. Sommige modules werden voornamelijk gebruikt door gliacellen, zoals microglia, astrocyten en cellen die myeline vormen, en werden gekoppeld aan Alzheimer, paniekstoornis en ADHD. Anderen werden gebruikt door exciterende en inhiberende neuronen en waren verrijkt voor synapsvorming, signaaloverdracht en voorhersenenontwikkeling, waarmee ze werden verbonden met intelligentie, autisme, depressie, schizofrenie en epilepsie. Weer andere modules waren het meest actief zeer vroeg in de foetale fase en betrokken bij chromatine- en celdelingscontrole, wat suggereert dat verstoringen in hoe hersencellen ontstaan en geprogrammeerd worden het toneel kunnen bereiden voor latere stemmings- en cognitieve problemen.
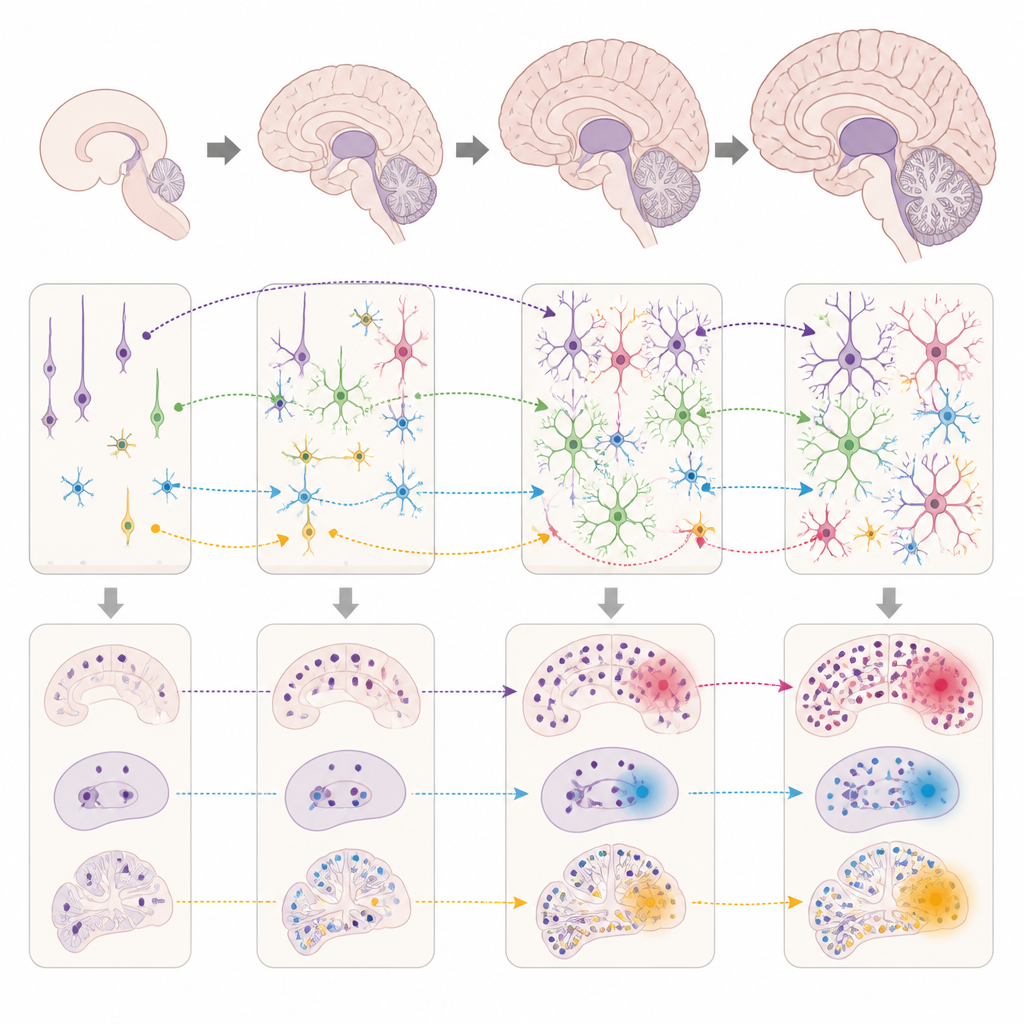
Wat dit betekent voor het begrijpen van hersenaandoeningen
In gewone bewoordingen suggereert dit werk dat dezelfde genen het risico niet overal en altijd verhogen; in plaats daarvan werken ze in specifieke hersenregio’s, celtypen en ontwikkelingsvensters. Wanneer die vensters samenvallen met de circuits die aandacht, emotie of geheugen ondersteunen, is de weg vrij voor bepaalde aandoeningen om te ontstaan. Door deze patronen voor veel aandoeningen tegelijk in kaart te brengen, biedt de studie een systeemniveauzicht dat genetische bevindingen verbindt met hersenontwikkeling en anatomie. Op de lange termijn zouden dergelijke kaarten preciezer onderzoek kunnen sturen naar wanneer en waar men moet zoeken naar vroege waarschuwingssignalen, en welke cellulaire processen de meest veelbelovende doelen voor behandeling zijn.
Bronvermelding: Liu, W., Shimogori, T. Spatiotemporal brain transcriptomics reveal risk gene hot-spots in major neuropsychiatric disorders. Commun Biol 9, 634 (2026). https://doi.org/10.1038/s42003-026-10045-x
Trefwoorden: hersenontwikkeling, neuropsychiatrische aandoeningen, genexpressie, risicogenen, hersencircuits