Clear Sky Science · fr
La transcriptomique spatiotemporelle du cerveau révèle des points chauds de gènes de risque dans les principales maladies neuropsychiatriques
Pourquoi le timing dans le cerveau compte
Beaucoup de troubles mentaux et neurologiques apparaissent d’abord à des âges particuliers, de l’autisme infantile à la maladie d’Alzheimer en fin de vie. Cette étude pose une question simple mais puissante : les gènes qui augmentent le risque de ces affections sont‑ils surtout actifs dans le cerveau aux mêmes périodes et aux mêmes endroits où les symptômes émergent habituellement ? En retraçant quand et où les gènes de risque s’activent au cours du développement cérébral humain, les auteurs cartographient des « points chauds » de vulnérabilité qui peuvent aider à expliquer qui tombe malade, quand, et pourquoi certains circuits cérébraux sont impliqués.
Suivre les gènes de risque tout au long de la vie
Pour construire cette carte, les chercheurs ont combiné plusieurs grands ensembles de données publiques mesurant quels gènes sont actifs dans différentes parties du cerveau humain, depuis la grossesse précoce jusqu’à l’âge adulte. Ils se sont concentrés sur les gènes de risque identifiés par de larges études génétiques pour 15 traits, y compris l’intelligence, l’autisme, le trouble déficitaire de l’attention avec ou sans hyperactivité, le syndrome de Tourette, le trouble obsessionnel compulsif, les troubles de l’humeur et d’anxiété, l’épilepsie et les maladies dégénératives comme Alzheimer et Parkinson. Pour chaque trait, ils ont évalué si ses gènes de risque étaient utilisés plus que prévu dans des régions cérébrales, des âges ou des types cellulaires particuliers, en utilisant à la fois des données de tissus en masse et des données unicellulaires, et en considérant l’enrichissement comme un signe de vulnérabilité accrue.
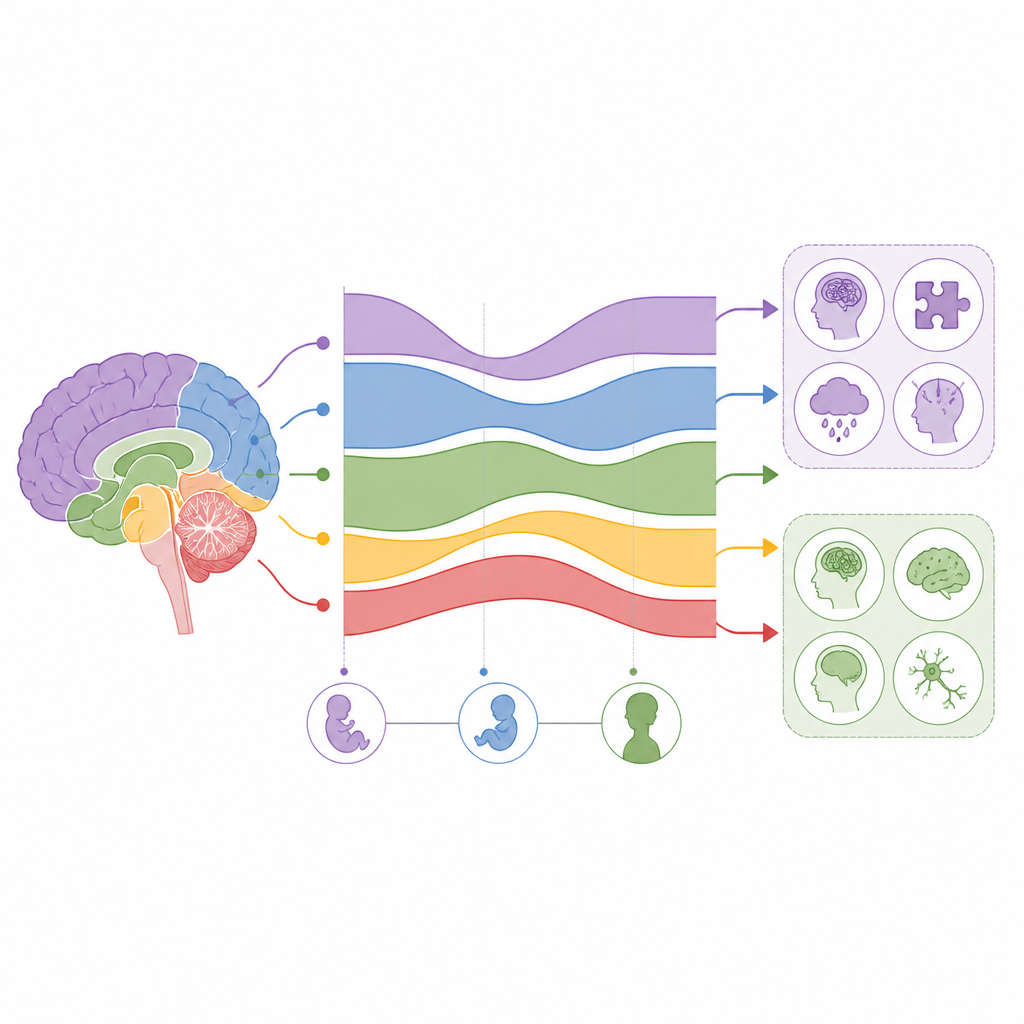
Vulnérabilité en début de vie versus en fin de vie
Un schéma clair est apparu : les traits qui ont tendance à débuter pendant l’enfance, comme l’autisme, le TDAH, le syndrome de Tourette et des variations de l’intelligence, présentaient la plus forte activité des gènes de risque avant la naissance. En revanche, les affections qui apparaissent habituellement à l’âge adulte, notamment l’épilepsie, la maladie d’Alzheimer et la maladie de Parkinson, montraient un pic d’activité de leurs gènes de risque après la naissance, souvent à l’âge moyen de la vie. Certaines maladies, en particulier la dépression majeure, le trouble obsessionnel compulsif et la schizophrénie, avaient des profils plus complexes, avec des gènes de risque s’activant à la fois autour de la naissance et de nouveau à l’adolescence ou au début de l’âge adulte. Globalement, la chronologie d’activité des gènes de risque suivait approximativement l’âge typique d’apparition des symptômes, soutenant l’idée que nombre de ces affections résultent de processus développementaux de longue durée plutôt que d’événements soudains.
Les circuits cérébraux comme points chauds de risque
L’étude a aussi identifié où dans le cerveau ces gènes de risque sont le plus actifs. De nombreux traits psychiatriques partageaient une implication étendue du cortex cérébral, qui soutient la réflexion, la planification et les comportements sociaux. Mais des différences notables existaient dans les structures profondes. Les gènes de risque pour le TDAH étaient particulièrement enrichis dans le thalamus et le striatum, des plaques tournantes clés pour l’attention et le contrôle du mouvement, tandis que les gènes associés au trouble panique et au névrosisme s’illuminaient dans l’amygdale, centre des émotions et de la peur. Le trouble obsessionnel compulsif montrait un fort enrichissement dans le striatum, le thalamus et le cervelet, en accord avec les modèles de circuits de longue date de la maladie. En revanche, les gènes de risque pour l’autisme, le syndrome de Tourette et la schizophrénie étaient relativement appauvris dans de nombreuses régions sous‑corticales, suggérant une origine plus fortement corticale.
Zoom sur les cellules et les voies moléculaires
Pour comprendre les mécanismes, les auteurs ont regroupé les gènes qui s’activent ensemble en « modules » de co‑expression et ont examiné quels modules étaient enrichis en gènes de risque, et quand et où ils étaient actifs. Certains modules étaient principalement utilisés par les cellules gliales, comme les microglies, les astrocytes et les cellules qui forment la myéline, et étaient liés à la maladie d’Alzheimer, au trouble panique et au TDAH. D’autres concernaient des neurones excitateurs et inhibiteurs et étaient enrichis pour la formation des synapses, la signalisation et le développement du télencéphale, les reliant à l’intelligence, l’autisme, la dépression, la schizophrénie et l’épilepsie. D’autres modules encore étaient très actifs au tout début de la vie fœtale et impliquaient le contrôle de la chromatine et du cycle cellulaire, suggérant que des perturbations de la naissance et de la programmation des cellules cérébrales pourraient préparer le terrain pour de futurs problèmes cognitifs et de l’humeur.
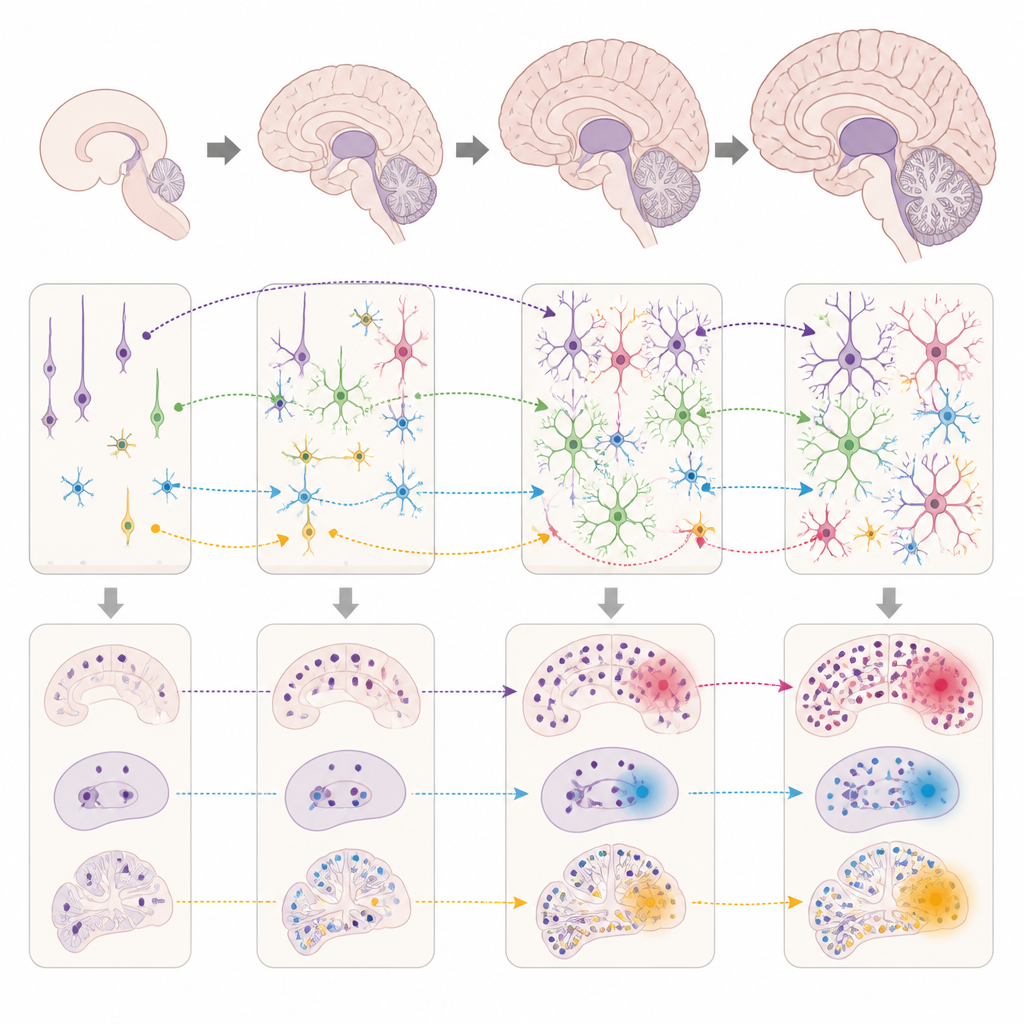
Ce que cela signifie pour la compréhension des troubles cérébraux
Concrètement, ce travail suggère que les mêmes gènes n’augmentent pas le risque partout et tout le temps ; ils agissent plutôt dans des régions cérébrales, des types cellulaires et des fenêtres développementales spécifiques. Lorsque ces fenêtres coïncident avec les circuits qui soutiennent l’attention, l’émotion ou la mémoire, le terrain est propice à l’émergence de troubles particuliers. En cartographiant ces schémas à travers de nombreuses affections simultanément, l’étude offre une vue au niveau systémique qui relie les découvertes génétiques au développement et à l’anatomie cérébrale. À long terme, de telles cartes pourraient orienter des recherches plus précises sur quand et où chercher des signes précurseurs, et quels processus cellulaires pourraient constituer les cibles de traitement les plus prometteuses.
Citation: Liu, W., Shimogori, T. Spatiotemporal brain transcriptomics reveal risk gene hot-spots in major neuropsychiatric disorders. Commun Biol 9, 634 (2026). https://doi.org/10.1038/s42003-026-10045-x
Mots-clés: développement cérébral, troubles neuropsychiatriques, expression génique, gènes de risque, circuits cérébraux