Clear Sky Science · nl
Dopamine-neuron-specifieke RNA-sequencing onthult dat Neprilysine 1 downstream van het cohesinecomplex werkt om leren te onderdrukken
Waarom dit belangrijk is voor het dagelijkse geheugen
We denken meestal dat beter geheugen iets is dat je kunt trainen of met medicijnen kunt bereiken. Deze studie in fruitvliegen suggereert een andere mogelijkheid: de hersenen kunnen ingebouwde remmen hebben die leren bewust terughouden, en sommige van die remmen worden tijdens vroege ontwikkeling ingesteld maar kunnen later in het leven nog worden aangepast. Door één zo’n rem te ontdekken, leveren de auteurs aanwijzingen voor hoe normaal geheugen wordt bijgesteld en waarom bepaalde genetische aandoeningen tot verstandelijke beperking leiden.
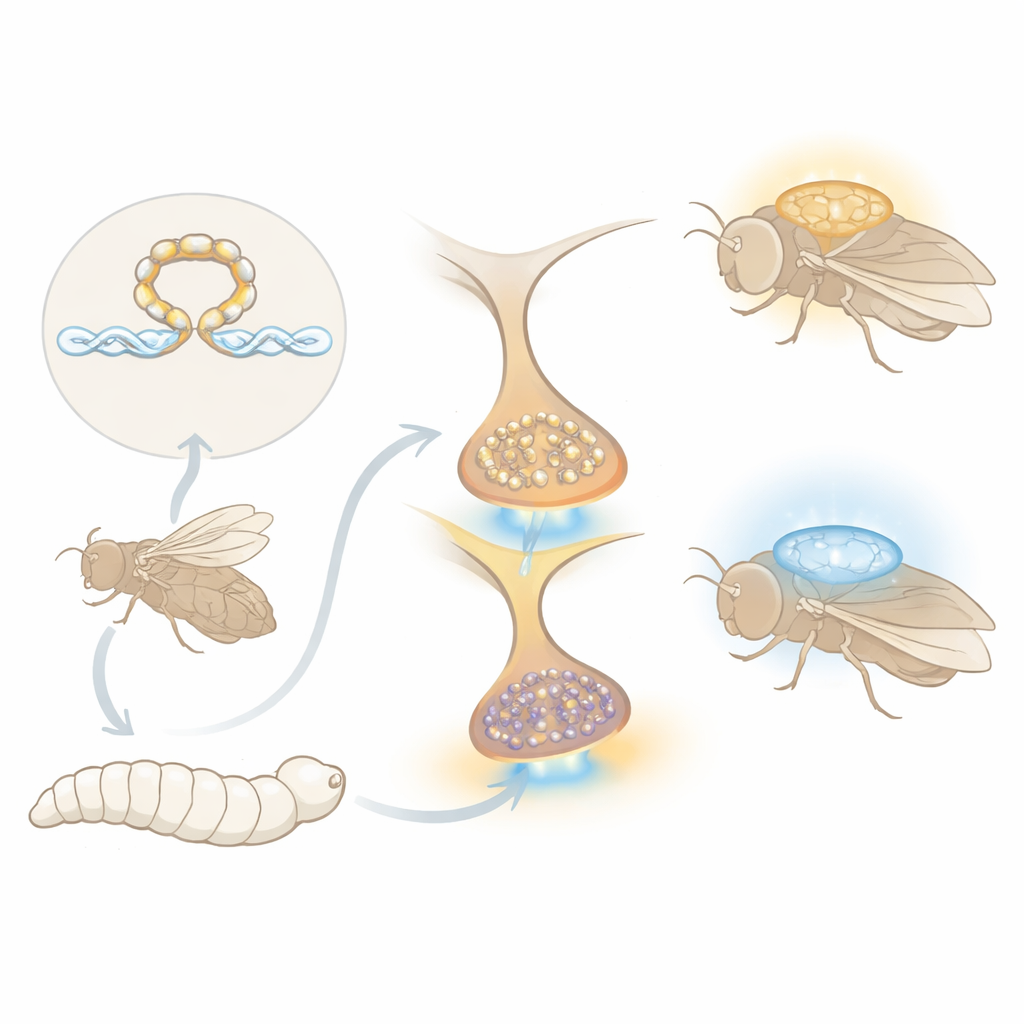
Een moleculaire rem op leren
Vorig werk van deze groep identificeerde een eiwit genaamd Stromalin als een onverwachte geheugenonderdrukker. Stromalin maakt deel uit van het cohesinecomplex, vooral bekend om zusterchromatiden tijdens celdeling bij elkaar te houden, maar het helpt ook te reguleren welke genen aan- of uitgezet worden. Bij fruitvliegen leidde het verminderen van Stromalin in een kleine groep dopaminerge neuronen tot ongeveer een verdubbeling van het aantal kleine chemische pakketjes, synaptische blaasjes genoemd, bij hun verbindingen, wat resulteerde in sterkere dopamine-afgifte en beter leren in een geur–schoktaak. Wat onduidelijk bleef, was hoe een genregulerend complex dat in de celkern werkt, kan bepalen hoeveel blaasjes worden opgebouwd voor toekomstige communicatie.
Het bericht lezen in dopaminerge cellen
Om deze kloof te overbruggen isoleerden de onderzoekers slechts 25 dopaminerge neuronen uit zich ontwikkelende vliegenlarven en bepaalden ze het RNA, een momentopname van welke genen actief zijn. Door normale cellen te vergelijken met cellen zonder Stromalin vonden ze 160 genen waarvan de activiteit veranderde. Vervolgens gebruikten ze een grootschalige genetische screening om elk van deze kandidaatgenen specifiek in dopaminerge neuronen uit te schakelen en stelden twee vragen: leerden de vliegen beter, en toonden de neuronen meer merkers voor synaptische blaasjes in hun terminals? Deze tweeledige filter beperkte het aantal tot een handvol genen waarvan verlies de effecten van Stromalin op geheugen en synaptische merkers nabootste.
Scherpstelling op Neprilysine 1
Onder de kandidaten stak één gen eruit: Neprilysine 1 (Nep1), dat codeert voor een membraaneiwit dat kleine signaalpeptiden buiten de cel knipt. Met een onafhankelijke methode om genactiviteit in de hele hersenen te meten, bevestigde het team dat het verminderen van zowel Stromalin als een andere cohesinesubeenheid, SMC1, consequent de Nep1-niveaus verlaagde. Wanneer ze Nep1 alleen in dopaminerge neuronen onderdrukten, leerden vliegen sneller en onthielden beter, en hun dopaminerge terminals droegen meer merker voor synaptische blaasjes zowel tijdens late larvale stadia als bij volwassenen. Directe beeldvorming van dopamineafgifte toonde dat deze neuronen sterke pulsen van dopamine bleven afgeven bij herhaalde schokken, in plaats van te wennen en te verzwakken zoals bij normale vliegen. Cruciaal was dat het verminderen van blaasje‑transport met een motorproteïne-mutatie de door Nep1 veroorzaakte toename in leren en synaptische merkers tenietdeed, wat impliceert dat Nep1 normaal gezien de beschikbare blaaspool beperkt.
De rem terugzetten downstream van cohesine
Om te testen of Nep1 werkelijk downstream van Stromalin ligt, produceerden de auteurs extra Nep1 terwijl ze tegelijk Stromalin verminderden. In dopaminerge neuronen bracht deze combinatie zowel de merkers voor synaptische blaasjes als het geheugenvermogen weer terug richting normaal, en keerde zo de versterking om die alleen door verlies van Stromalin werd gezien. Vergelijkbare rescuemutaties traden op wanneer deze manipulaties over het hele brein werden toegepast. Interessant is dat hoewel cohesine’s invloed op Nep1-niveaus lijkt te worden ingesteld tijdens een kritieke larvale periode, het verminderen van Nep1-activiteit alleen in de volwassenheid nog steeds voldoende was om leren te verbeteren, wat laat zien dat de rem na de ontwikkeling kan worden bijgesteld. Tegelijkertijd bracht het verwijderen van Nep1 of SMC1 in alle neuronen het geheugen schade toe, wat echo’s oproept van de cognitieve problemen die gezien worden bij mensen met cohesine-gerelateerde syndromen.
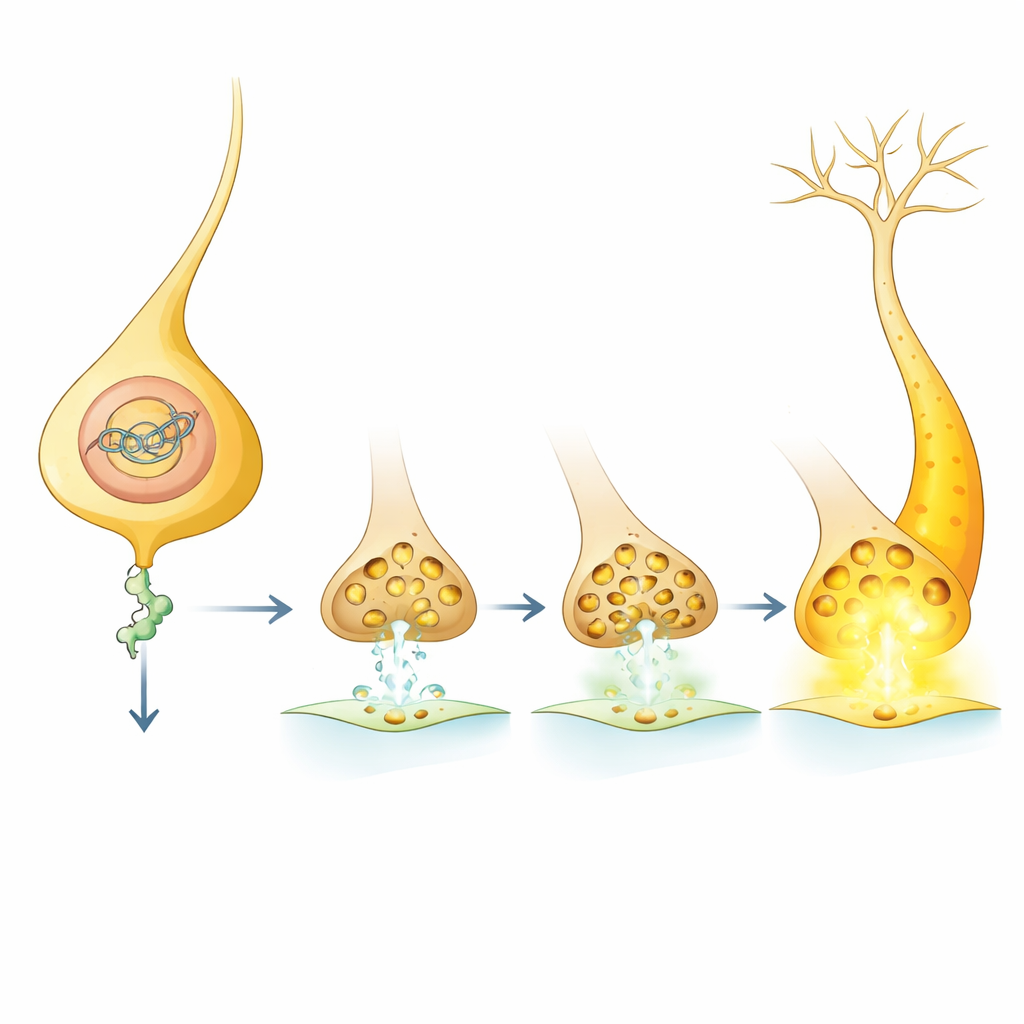
Wat dit betekent voor het begrijpen en behandelen van geheugenproblemen
In gewone bewoordingen werkt cohesine als een ontwikkelingsknop die instelt hoe sterk bepaalde dopaminerge paden kunnen communiceren met downstream hersencentra door de niveaus van Nep1 bij te sturen. Wanneer cohesinefunctie afneemt, dalen Nep1-niveaus, hopen zich meer synaptische blaasjes op en worden dopaminesignalen sterker, wat vliegen in sommige circuits beter laat leren maar anderen schaadt wanneer veranderingen wijdverspreid zijn. Omdat Nep1 leren nog steeds kan beïnvloeden wanneer het alleen bij volwassenen wordt gemanipuleerd, suggereert het werk dat sommige gevolgen van vroege genregulatie-afwijkingen later verzacht kunnen worden door downstream spelers zoals Nep1 te targeten. Hoewel deze resultaten afkomstig zijn van fruitvliegen, sluiten ze aan bij bevindingen in muismodellen en bij menselijke patiënten, en suggereren dat het fijn afstellen van soortgelijke moleculaire remmen op termijn zou kunnen helpen om leren en geheugen in ontwikkelingsstoornissen te herkaderen.
Bronvermelding: Pimenov, I., MacMullen, C.M., Ezeh, C. et al. Dopamine neuron specific RNA-sequencing reveals Neprilysin 1 acts downstream of the cohesin complex to suppress learning. Commun Biol 9, 441 (2026). https://doi.org/10.1038/s42003-026-09690-z
Trefwoorden: genen die geheugen onderdrukken, dopaminerge neuronen, synaptische blaasjes, cohesinecomplex, neprilysine