Clear Sky Science · fr
Le séquençage de l’ARN spécifique aux neurones dopaminergiques révèle que Neprilysin 1 agit en aval du complexe cohesine pour supprimer l’apprentissage
Pourquoi c’est important pour la mémoire quotidienne
On imagine généralement qu’une meilleure mémoire s’acquiert par l’entraînement ou des médicaments. Cette étude chez la mouche du vinaigre suggère une autre possibilité : le cerveau pourrait comporter des freins intégrés qui limitent volontairement l’apprentissage, et certains de ces freins sont programmés tôt dans le développement mais peuvent être modulés plus tard. En mettant au jour l’un de ces freins, les auteurs donnent des indications sur la façon dont la mémoire normale est réglée et pourquoi certains troubles génétiques entraînent un retard intellectuel.
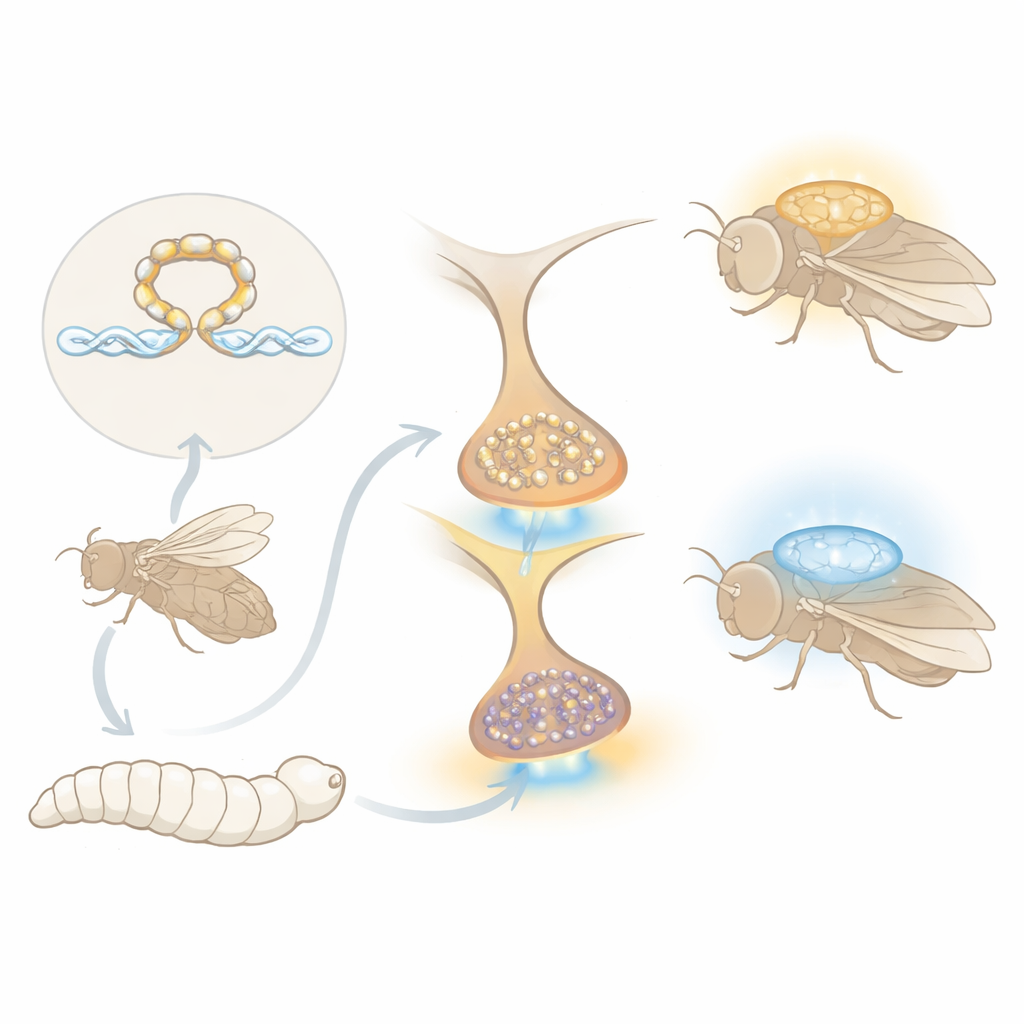
Un frein moléculaire à l’apprentissage
Des travaux précédents de ce groupe avaient identifié une protéine appelée Stromalin comme un surprenant suppresseur de mémoire. Stromalin fait partie du complexe cohesine, connu pour maintenir les chromatides sœurs ensemble lors de la division cellulaire, mais il participe aussi au contrôle de l’activation des gènes. Chez la mouche, réduire Stromalin dans un petit groupe de neurones producteurs de dopamine double approximativement le nombre de petits paquets chimiques, appelés vésicules synaptiques, à leurs connexions, entraînant une libération de dopamine plus forte et une meilleure acquisition dans une tâche odorat–choc. Restait à expliquer comment un complexe de régulation génique agissant dans le noyau cellulaire peut dicter combien de vésicules sont construites pour la communication future.
Lire le message dans les cellules dopaminergiques
Pour combler ce fossé, les chercheurs ont isolé seulement 25 neurones dopaminergiques de larves de mouche en développement et séquencé leur ARN, offrant un instantané des gènes actifs. En comparant les cellules normales à celles dépourvues de Stromalin, ils ont trouvé 160 gènes dont l’activité changeait. Ils ont ensuite réalisé un criblage génétique à grande échelle pour éteindre chacun de ces gènes candidats spécifiquement dans les neurones dopaminergiques et ont posé deux questions : la mouche apprenait-elle mieux, et les neurones montraient-ils plus de marqueur de vésicule synaptique à leurs terminaisons ? Ce filtre en deux étapes a réduit le champ à une poignée de gènes dont la perte imitait les effets de Stromalin sur la mémoire et les marqueurs synaptiques.
Projecteur sur Neprilysin 1
Parmi les candidats, un gène a émergé : Neprilysin 1 (Nep1), qui code pour une enzyme membranaire clivant de petits peptides de signalisation à l’extérieur des cellules. En utilisant une méthode indépendante pour mesurer l’activité génique dans tout le cerveau, l’équipe a confirmé que réduire soit Stromalin soit une autre sous-unité de la cohesine, SMC1, abaissait systématiquement les niveaux de Nep1. Lorsqu’ils ont réduit Nep1 uniquement dans les neurones dopaminergiques, les mouches apprenaient plus vite et retenaient mieux, et leurs terminaisons dopaminergiques présentaient davantage de marqueur de vésicule synaptique tant à la fin du stade larvaire qu’à l’âge adulte. L’imagerie directe de la libération de dopamine a montré que ces neurones continuaient à libérer de fortes impulsions de dopamine lors de chocs répétés, au lieu de s’adapter et de s’affaiblir comme chez les mouches normales. De façon cruciale, freiner le transport des vésicules par une mutation affectant une protéine motrice annulait le renforcement de l’apprentissage et des marqueurs synaptiques induit par la perte de Nep1, ce qui suggère que Nep1 limite normalement le réservoir de vésicules disponible.
Réarmer le frein en aval de la cohesine
Pour tester si Nep1 se situe véritablement en aval de Stromalin, les auteurs ont surproduit Nep1 tout en réduisant Stromalin. Dans les neurones dopaminergiques, cette combinaison a rétabli à la fois les marqueurs de vésicules synaptiques et les performances mnésiques vers des valeurs normales, contrebalançant l’amélioration observée lors de la perte de Stromalin seule. Des rescues similaires sont apparues lorsque ces manipulations ont été étendues à l’ensemble du cerveau. Fait intéressant, alors que l’influence de la cohesine sur les niveaux de Nep1 semble se fixer durant une fenêtre larvaire critique, réduire l’activité de Nep1 seulement à l’âge adulte suffisait encore à améliorer l’apprentissage, montrant que le frein peut être ajusté après le développement. En revanche, couper Nep1 ou SMC1 dans tous les neurones nuisait à la mémoire, faisant écho aux troubles cognitifs observés chez des patients avec des syndromes liés à la cohesine.
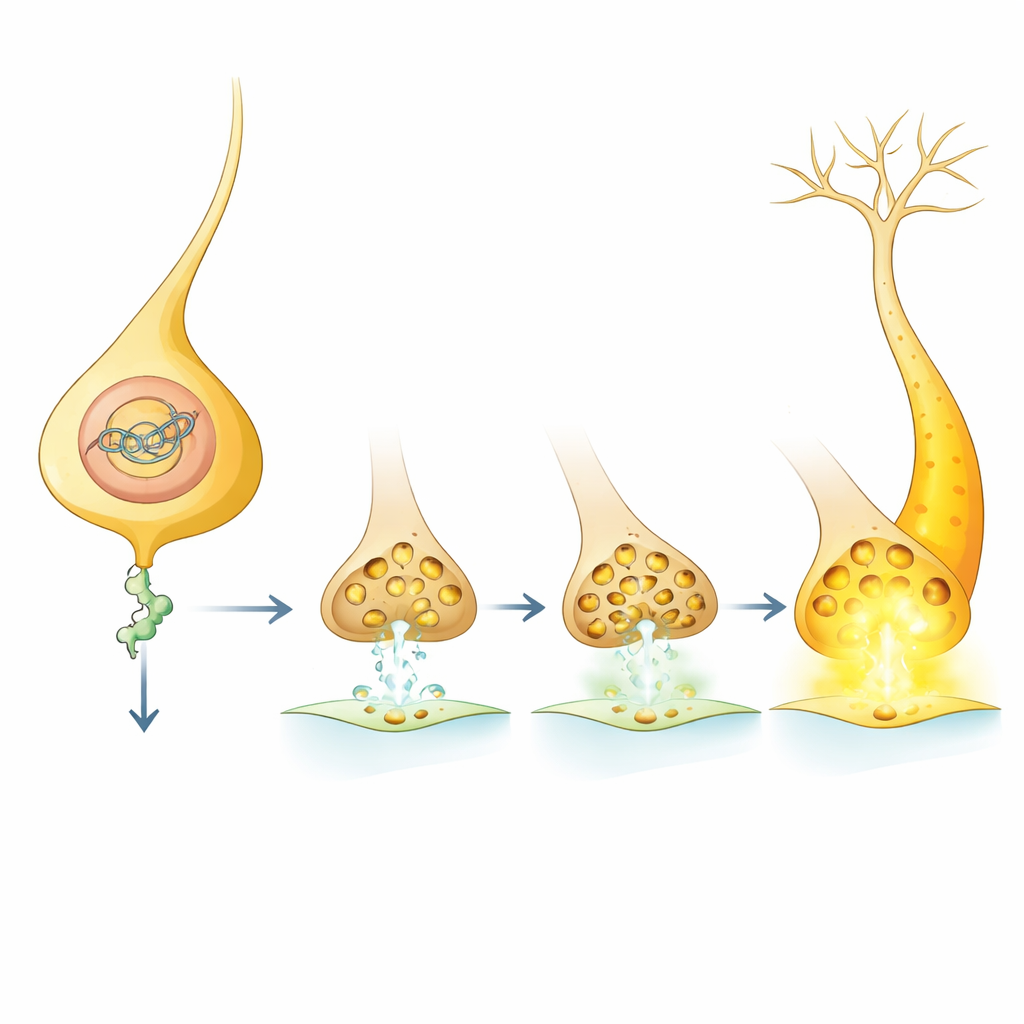
Ce que cela signifie pour la compréhension et le traitement des problèmes mnésiques
Concrètement, la cohesine agit comme un cadran développemental qui règle l’intensité avec laquelle certaines voies dopaminergiques peuvent communiquer avec des centres cérébraux en aval en modulant les niveaux de Nep1. Quand la fonction de la cohesine diminue, les niveaux de Nep1 chutent, davantage de vésicules synaptiques s’accumulent et les signaux dopaminergiques se renforcent, améliorant l’apprentissage dans certains circuits mais en détériorant d’autres lorsque les changements sont généralisés. Parce que Nep1 peut encore façonner l’apprentissage lorsqu’il est manipulé seulement à l’âge adulte, ces résultats suggèrent que certaines conséquences d’un défaut précoce de régulation génique pourraient être atténuées plus tard en ciblant des acteurs en aval comme Nep1. Bien que ces résultats proviennent de la mouche, ils résonnent avec des observations chez la souris et chez l’humain, laissant entendre qu’un ajustement fin de freins moléculaires similaires pourrait un jour aider à rééquilibrer apprentissage et mémoire dans les troubles du développement du cerveau.
Citation: Pimenov, I., MacMullen, C.M., Ezeh, C. et al. Dopamine neuron specific RNA-sequencing reveals Neprilysin 1 acts downstream of the cohesin complex to suppress learning. Commun Biol 9, 441 (2026). https://doi.org/10.1038/s42003-026-09690-z
Mots-clés: gènes suppresseurs de mémoire, neurones dopaminergiques, vésicules synaptiques, complexe cohesine, neprilysine