Clear Sky Science · nl
Therapeutische reacties voorspellen bij gemetastaseerde colorectale kanker via gepersonaliseerde functionele profilering van patiënt-afgeleide sferoïden
Betere behandelovereenkomsten vinden
Voor mensen met gevorderde colorectale kanker kan het kiezen van het juiste middel voelen als proberen en vergissen. Deze studie verkent een manier om veel geneesmiddelen rechtstreeks te testen op de kankercellen van een patiënt die in het laboratorium zijn gekweekt, met als doel te voorspellen welke behandelingen waarschijnlijk helpen en welke mogelijk falen voordat kostbare tijd verloren gaat.
Waarom huidige middelen niet genoeg zijn
Moderne kankerzorg leunt vaak op het uitlezen van het DNA van de tumor om naar mutaties te zoeken die wijzen op specifieke geneesmiddelen. Hoewel deze aanpak sommige patiënten heeft geholpen, krijgt de meerderheid van de mensen met gevorderde solide tumoren nog steeds geen succesvolle DNA-gematchte behandeling. Veel tumoren missen duidelijke genetische ‘‘handvatten’’, en zelfs wanneer mutaties worden gevonden, blijven de responspercentages op gerichte middelen beperkt. De auteurs betogen dat het direct meten van hoe de kankercellen van een patiënt op geneesmiddelen reageren in een schaaltje genetische tests kan aanvullen en behandelingsbeslissingen kan verscherpen.
Tumorweefsel omzetten in mini-tumoren
Het onderzoeksteam verzamelde tumorweefsel van twaalf patiënten met gemetastaseerde colorectale kanker en kweekte de cellen als driedimensionale clusters die sferoïden worden genoemd. Deze kleine celballetjes bootsen echte tumoren beter na dan platte cellagen. De wetenschappers bevestigden dat de sferoïden onder de microscoop en op DNA-niveau sterk leken op de oorspronkelijke kankers, met behoud van dezelfde belangrijke mutaties en een groot deel van de onderliggende diversiteit. Ze toonden ook aan dat ingevroren en later ontdooide sferoïden zich in grote lijnen hetzelfde gedroegen als vers gekweekte exemplaren, een belangrijke stap richting het opbouwen van levende biobanken met patiëntmonsters.
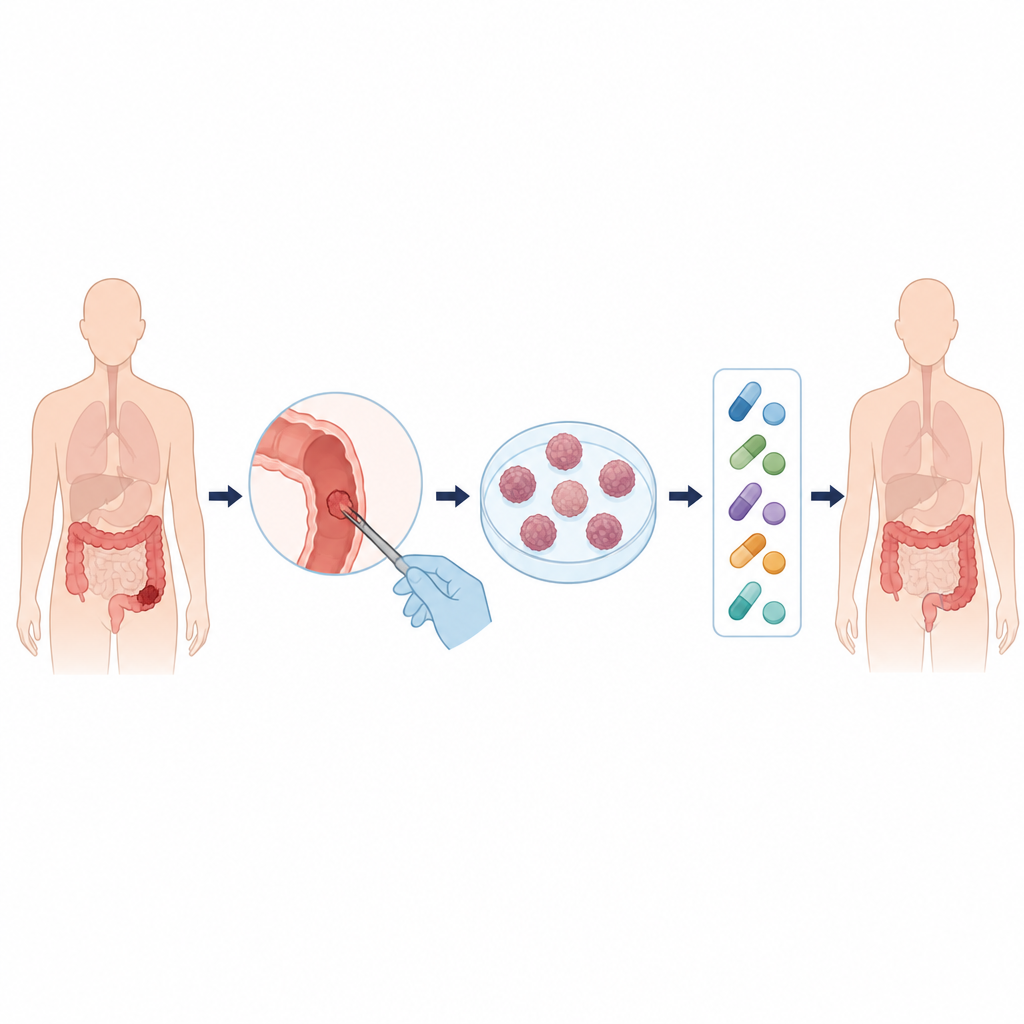
De cellen van patiënten onderwerpen aan medicijntests
Met behulp van geautomatiseerde printers en miniaturiseerde platen stelde het team de sferoïden bloot aan 42 kankermiddelen plus vijf standaardbehandelingen, afzonderlijk of in combinaties. Ze volgden hoe goed elk middel de cellen vertraagde of doodde en vergeleken deze laboratoriumresultaten met hoe dezelfde patiënten daadwerkelijk in de kliniek hadden gereageerd. Voor middelen die een groeisignaal aan de celoppervlakte blokkeren dat bekendstaat als EGFR, kwamen de patronen goed overeen. Sferoïden van patiënten van wie bekend was dat hun tumoren op basis van DNA of beeldvorming resistent waren tegen anti‑EGFR-therapie, waren in het lab ook resistent tegen deze middelen. Daarentegen waren sferoïden van patiënten met stabiele of krimpende ziekte onder anti‑EGFR-behandeling vaak gevoeliger in het schaaltje.
Verborgen kansen en blinde vlekken ontdekken
De tests toonden soms behandelingsopties aan die eenvoudig DNA‑onderzoek kunnen missen. De sferoïden van één patiënt waren bijvoorbeeld zeer gevoelig voor EGFR-blokkerende middelen, ook al voorspelde geen duidelijke genetische aanwijzing dit, wat illustreert hoe functionele testen onverwachte zwakke plekken kunnen blootleggen. De screens wezen ook tumoren aan met zeldzame veranderingen in verwante eiwitten (ERBB2 en ERBB3) die ze bijzonder vatbaar maakten voor bepaalde middelen die twee doelen tegelijk aanvallen. Aan de andere kant vertoonden geneesmiddelen gericht op het afsnijden van bloedvatgroei rond tumoren weinig activiteit in de sferoïden en weerspiegelden ze de uitkomsten bij patiënten niet, waarschijnlijk omdat het labmodel geen bloedvaten en ondersteunend weefsel bevat. Reacties op standaard chemotherapiemengsels varieerden sterk, met de duidelijkste medicijngevoeligheid in monsters van patiënten die nog geen chemotherapie hadden gekregen.
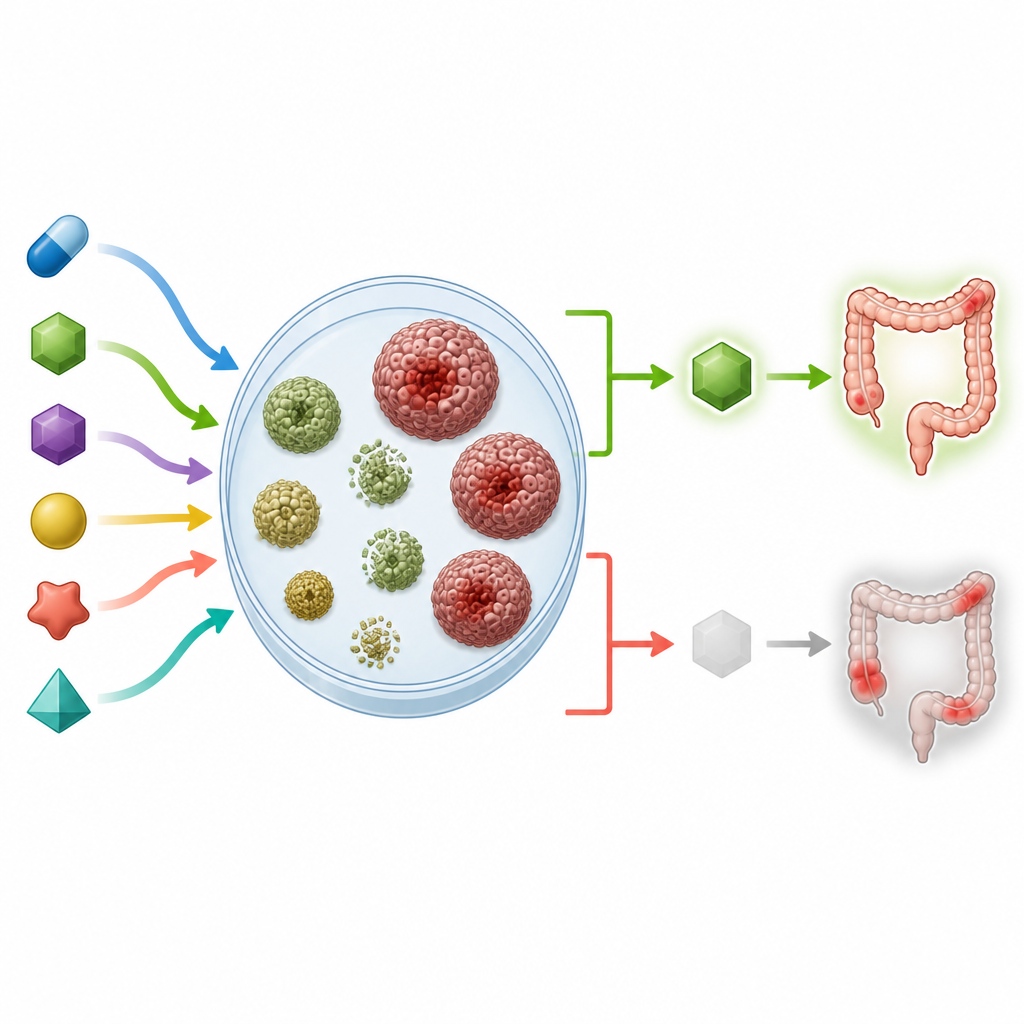
Wat dit voor patiënten zou kunnen betekenen
Dit werk suggereert dat het testen van veel geneesmiddelen op patiënt-afgeleide sferoïden zowel kan bevestigen wat genetische tests voorspellen als nieuwe behandelrichtingen kan onthullen, vooral voor therapieën gericht op EGFR en verwante doelen. Hoewel de aanpak nog enkele weken in beslag neemt en verfijning nodig heeft, toonde ze aan dat kleine, in het laboratorium gekweekte kopieën van iemands tumor kunnen weerspiegelen hoe die persoon in werkelijkheid op bepaalde behandelingen reageert. Met snellere workflows, meer gerichte medicijnpanelen en modellen die de tumoromgeving beter omvatten, kan dit soort gepersonaliseerde functionele profilering op een dag artsen helpen therapieën te kiezen die elke patiënt een betere kans op voordeel geven en middelen vermijden die waarschijnlijk niet werken.
Bronvermelding: El-Khoury, V., Smajović, LN., Mgrditchian, T. et al. Predicting therapeutic responses in metastatic colorectal cancer through personalized functional profiling of patient-derived spheroids. npj Precis. Onc. 10, 181 (2026). https://doi.org/10.1038/s41698-026-01356-7
Trefwoorden: gemetastaseerde colorectale kanker, patiënt-afgeleide sferoïden, medicijngevoeligheidstest, EGFR-remmers, functionele precisie-oncologie