Clear Sky Science · de
Vorhersage therapeutischer Ansprechraten beim metastasierten kolorektalen Karzinom durch personalisierte funktionelle Profilierung patientenabgeleiteter Sphäroide
Bessere Übereinstimmungen für Therapien finden
Für Menschen mit fortgeschrittenem Darmkrebs kann die Auswahl des richtigen Medikaments wie Ausprobieren wirken. Diese Studie untersucht eine Methode, bei der viele Arzneimittel direkt an den im Labor gezüchteten Krebszellen eines Patienten getestet werden, mit dem Ziel vorherzusagen, welche Behandlungen wahrscheinlich helfen und welche wahrscheinlich versagen, bevor kostbare Zeit verloren geht.
Warum die heutigen Werkzeuge nicht ausreichen
Die moderne Krebsmedizin stützt sich häufig auf die Analyse der Tumor‑DNA, um nach Mutationen zu suchen, die auf bestimmte Medikamente hinweisen. Während dieser Ansatz einigen Patientinnen und Patienten geholfen hat, erhalten die meisten Menschen mit fortgeschrittenen soliden Tumoren dennoch keine erfolgreiche, DNA‑abgestimmte Behandlung. Viele Tumoren bieten keine klaren genetischen „Anhaltspunkte“, und selbst wenn Mutationen gefunden werden, bleiben die Ansprechraten auf gezielte Wirkstoffe bescheiden. Die Autorinnen und Autoren argumentieren, dass das direkte Messen, wie die Krebszellen eines Patienten in einer Schale auf Medikamente reagieren, die genetische Diagnostik ergänzen und die Therapieentscheidung schärfen kann.
Vom Tumorprobe zum Mini‑Tumor
Das Forschungsteam sammelte Tumorgewebe von zwölf Patientinnen und Patienten mit metastasiertem kolorektalem Krebs und kultivierte die Zellen als dreidimensionale Verbände, sogenannte Sphäroide. Diese winzigen Zellkugeln bilden echte Tumoren besser nach als flache Zellschichten. Die Wissenschaftler bestätigten, dass die Sphäroide dem ursprünglichen Tumor unter dem Mikroskop und auf DNA‑Ebene ähnlich blieben, indem sie dieselben wichtigen Mutationen und einen Großteil der zugrundeliegenden Vielfalt bewahrten. Sie zeigten außerdem, dass eingefrorene und später aufgetaute Sphäroide sich ähnlich verhalten wie frisch gezüchtete — ein wichtiger Schritt zum Aufbau lebender Biobanken von Patientenproben.
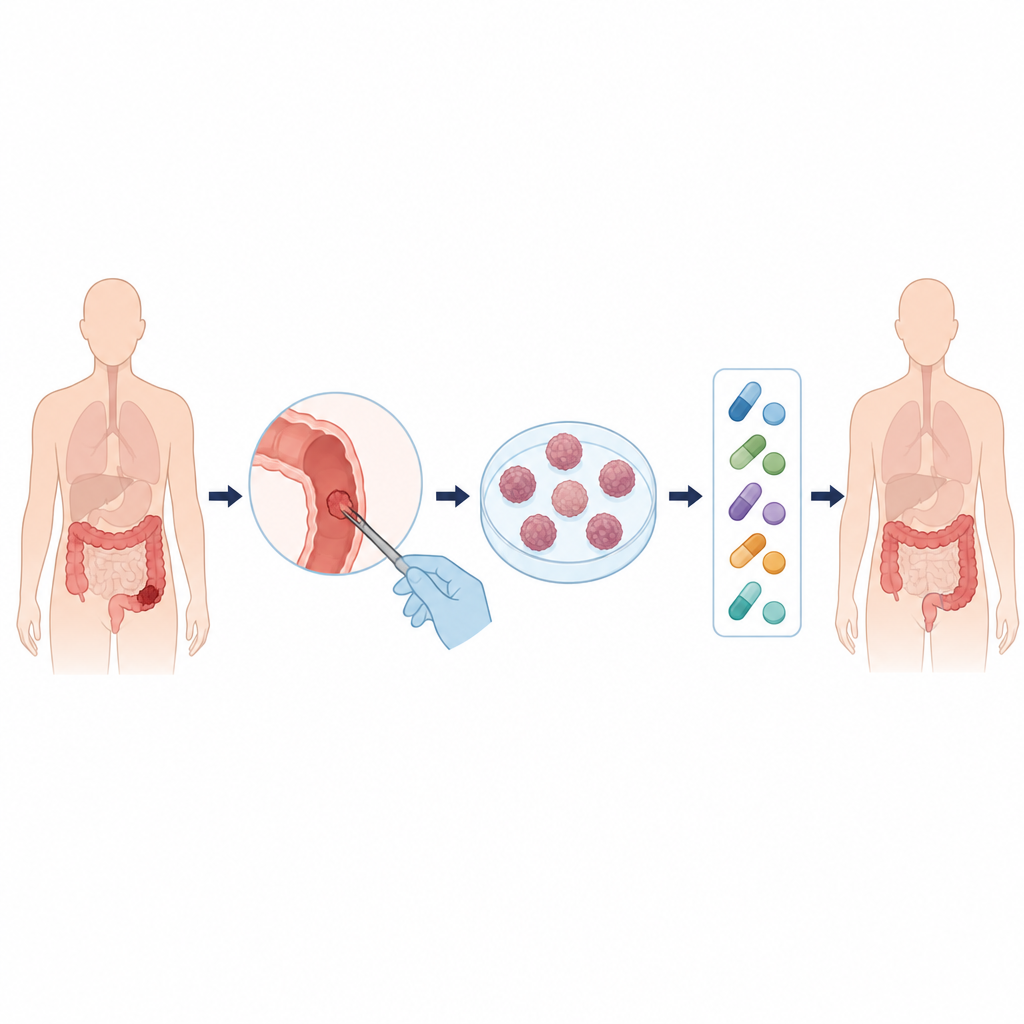
Patientenzellen in Wirkstofftests bringen
Mittels automatisierter Drucker und miniaturisierter Platten setzte das Team die Sphäroide 42 Krebsmedikamenten sowie fünf Standardtherapien aus, einzeln oder in Kombination. Sie verfolgten, wie gut jedes Mittel das Zellwachstum verlangsamte oder die Zellen abtötete, und verglichen diese Laborergebnisse mit dem klinischen Ansprechen derselben Patientinnen und Patienten. Bei Wirkstoffen, die ein Wachstumsignal an der Zelloberfläche namens EGFR blockieren, stimmten die Muster gut überein. Sphäroide von Patientinnen und Patienten, deren Tumoren bekanntermaßen — durch DNA‑Befunde oder Bildgebung — gegen Anti‑EGFR‑Therapie resistent waren, zeigten im Labor ebenfalls Resistenzen. Im Gegensatz dazu waren Sphäroide von Personen mit stabilem oder schrumpfendem Tumor unter Anti‑EGFR‑Behandlung im Reagenzglas tendenziell empfindlicher.
Verborgene Chancen und blinde Flecken aufspüren
Die Tests zeigten manchmal Behandlungsoptionen auf, die die einfache DNA‑Analyse übersehen hätte. Bei einer Patientin waren die Sphäroide sehr empfindlich gegenüber EGFR‑blockierenden Wirkstoffen, obwohl kein offensichtlicher genetischer Hinweis dies vorhersagte — ein Beispiel dafür, wie funktionelle Tests unerwartete Verwundbarkeiten offenbaren können. Die Screenings wiesen zudem auf Tumoren mit seltenen Veränderungen in verwandten Molekülen (ERBB2 und ERBB3) hin, die sie besonders anfällig für bestimmte Dual‑Target‑Medikamente machten. Andererseits zeigten Mittel, die das Tumor‑umgebende Gefäßwachstum blockieren sollen, in den Sphäroiden kaum Wirksamkeit und spiegelten nicht das klinische Ansprechen wider — vermutlich, weil das Labormodell über keine Blutgefäße und Stützgewebe verfügt. Die Ansprechraten auf konventionelle Chemotherapieregime variierten stark; die deutlichste Empfindlichkeit zeigte sich in Proben von Patientinnen und Patienten, die zuvor noch keine Chemotherapie erhalten hatten.
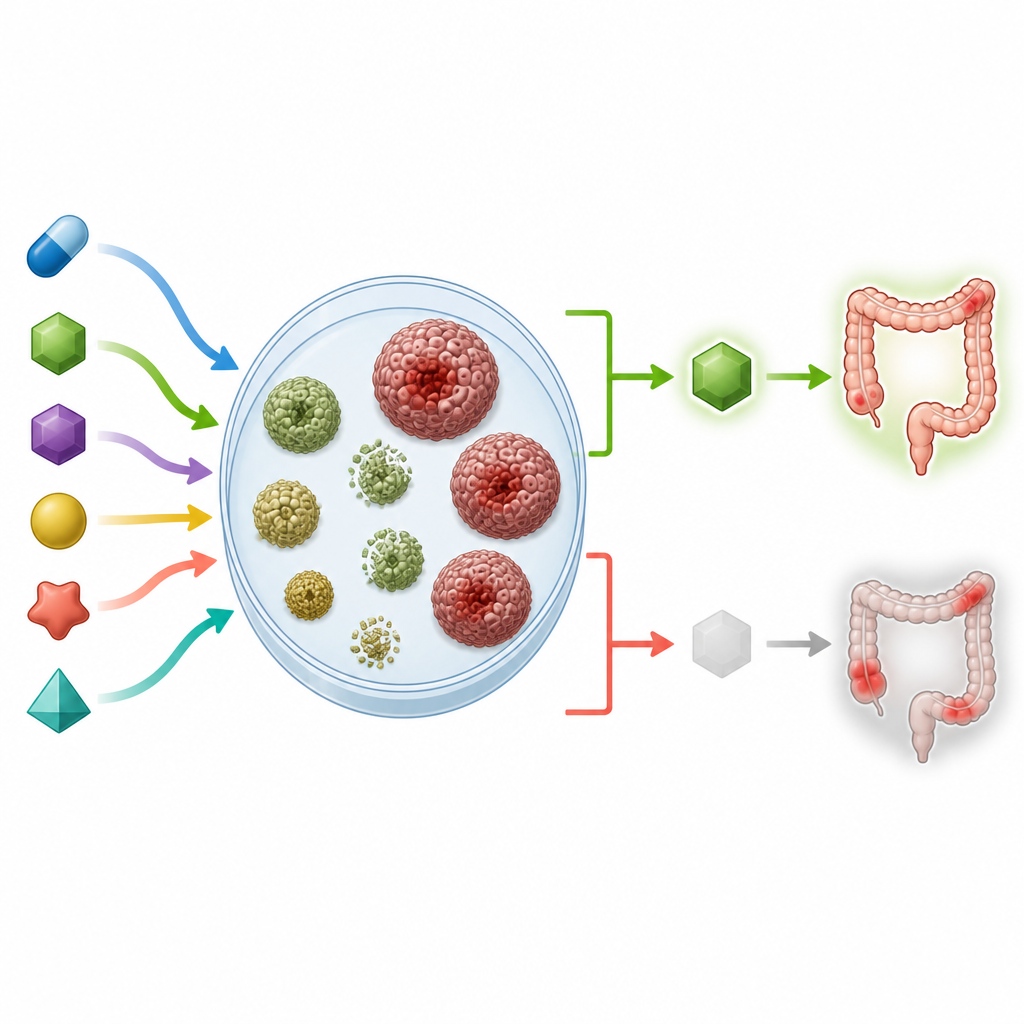
Was das für Patientinnen und Patienten bedeuten könnte
Diese Arbeit legt nahe, dass das Testen vieler Wirkstoffe an patientenabgeleiteten Sphäroiden sowohl Vorhersagen aus genetischen Tests bestätigen als auch neue therapeutische Ansätze aufzeigen kann, insbesondere für Therapien, die auf EGFR und verwandte Ziele abzielen. Zwar dauert der Ansatz noch mehrere Wochen und bedarf weiterer Verfeinerung, doch zeigte er, dass kleine, im Labor gezüchtete Kopien eines individuellen Tumors das klinische Ansprechen auf manche Behandlungen widerspiegeln können. Mit schnelleren Abläufen, fokussierteren Wirkstoffpanels und Modellen, die die Tumorumgebung besser einbeziehen, könnte diese Art personalisierter funktioneller Profilierung eines Tages Ärztinnen und Ärzten helfen, Therapien auszuwählen, die jeder Patientin und jedem Patienten eine höhere Wahrscheinlichkeit für einen Nutzen bieten und unnötige, wahrscheinlich wirkungslose Medikamente vermeiden.
Zitation: El-Khoury, V., Smajović, LN., Mgrditchian, T. et al. Predicting therapeutic responses in metastatic colorectal cancer through personalized functional profiling of patient-derived spheroids. npj Precis. Onc. 10, 181 (2026). https://doi.org/10.1038/s41698-026-01356-7
Schlüsselwörter: metastasiertes kolorektales Karzinom, patientenabgeleitete Sphäroide, Wirkstoff‑Empfindlichkeitstests, EGFR‑Inhibitoren, funktionelle Präzisionsonkologie