Clear Sky Science · nl
Melkvetbol EGF- en factor V/VIII-domein bevatte (MFGE8) als een nieuwe speler bij equiene endometriumfibrose
Waarom dit belangrijk is voor paardenhouders en fokkers
Veel merries worden minder vruchtbaar naarmate ze ouder worden, vaak om redenen die verborgen blijven totdat een dracht herhaaldelijk faalt. Deze studie kijkt in de baarmoeder van oudere merries om één veelvoorkomende oorzaak te begrijpen: littekenvorming van het baarmoederslijmvlies, bekend als endometriumfibrose. De auteurs richten zich op twee boodschapperproteïnen die deze stapels littekenweefsel schijnbaar tegengesteld beïnvloeden—één die littekenvorming stimuleert en een andere die die mogelijk helpt te remmen—en leveren daarmee aanwijzingen voor toekomstige behandelingen die de vruchtbaarheid bij ouder wordende paarden zouden kunnen behouden.
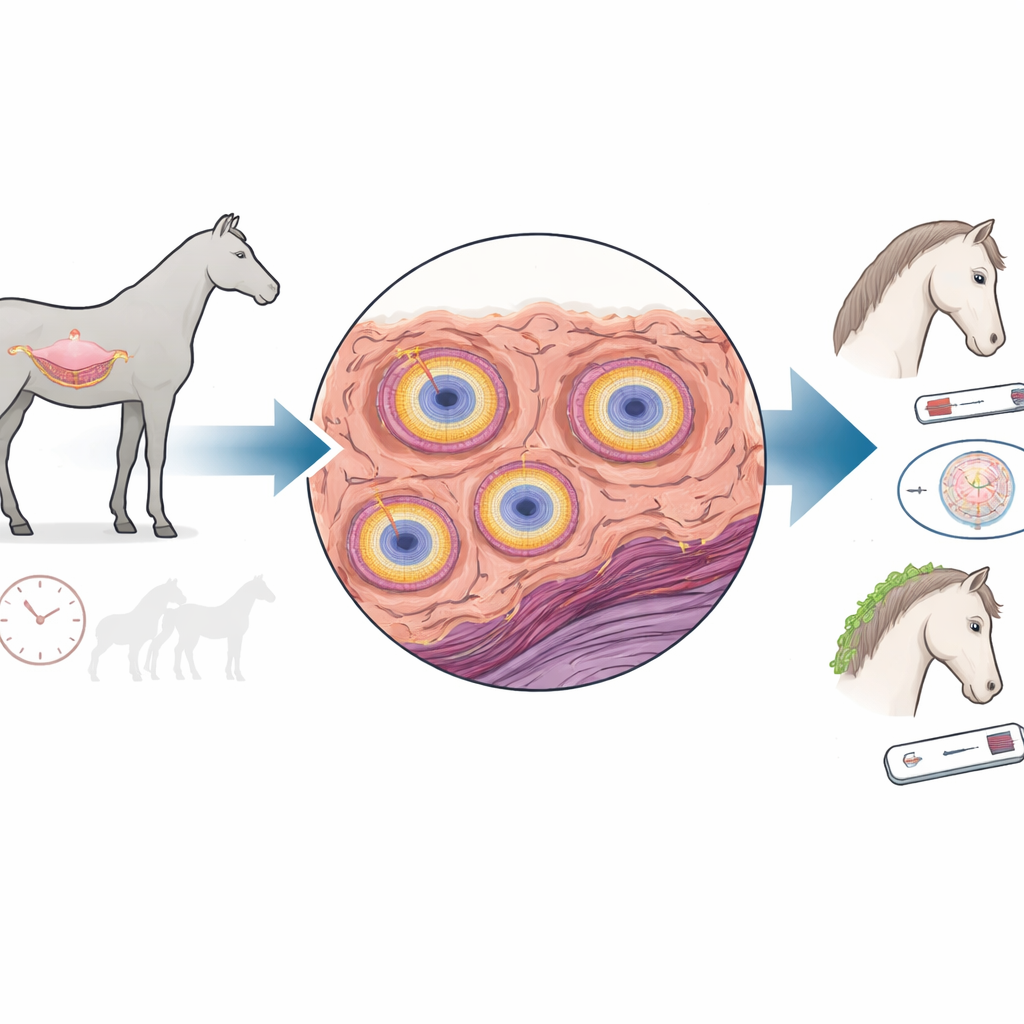
Littekens in de baarmoeder en verloren vruchtbaarheid
In een gezonde merrie scheiden kleine klieren in het baarmoederslijmvlies voedende vloeistoffen af die de allereerste stadia van de dracht ondersteunen. Met de leeftijd raken deze klieren bij veel merries ingesloten in lagen littekenweefsel en stijve tussencelmaterialen. Dit proces, fibrose of endometrose genoemd, verstoort de functie van de klieren en hangt sterk samen met onvruchtbaarheid. De littekenvorming ontstaat wanneer normale wondgenezing uit balans raakt: reparatiecellen die fibroblasten heten transformeren in krachtiger ‘myofibroblasten’ die overtollig collageen en andere bouwstenen van littekenweefsel aanleggen, en vervolgens niet goed uitschakelen.
Twee moleculaire signalen met tegengestelde neigingen
Het team richtte zich op transforming growth factor beta 1, een bekende aanjager van littekenvorming in veel organen, en op MFGE8, een minder bekend eiwit dat in andere weefsels vaak als een rem op fibrose werkt. Met een techniek die zichtbaar maakt waar bepaalde genen actief zijn in weefselplaten, brachten ze vier sleutelspelers in de merriebaarmoeder in kaart: het littekensignaal, zijn hulpstoffen CCN2 en TAGLN, en MFGE8. Ze vonden dat wanneer het littekensignaal sterk actief was in kliergebieden, zijn hulpstoffen bijna altijd ook actief waren, en het omliggende weefsel veel lagen fibroblastachtige cellen en zware littekenvorming vertoonde. Daarentegen werd MFGE8 het sterkst gezien rond klieren die al fibrotisch waren, waarmee het nauw verbonden leek met de ziekte, hoewel zijn exacte rol alleen uit lokalisatie niet direct op te maken was.
Inzoomen op individuele cellen
Om te zien hoe deze signalen celgedrag veranderen, kweekten de onderzoekers baarmoederfibroblasten van meerdere merries op zachte, met collageen beklede gels die beter echte weefsels nabootsen dan standaard plastic labschotels. Ze blootstelden de cellen vervolgens aan óf het littekensignaal óf aan MFGE8 en onderzochten de genactiviteit per cel met single-cell-sequencing. Het littekensignaal veroorzaakte ingrijpende veranderingen in bijna alle fibroblastgroepen: genen voor collageen en andere matrixcomponenten stegen sterk, factoren die groei en overleving bevorderen namen toe, en beschermende immuunachtige signalen bekend als interferonen werden onderdrukt. Gezamenlijk schetsen deze verschuivingen het beeld van een weefselomgeving die geneigd is te verharden en littekenvorming te ontwikkelen.
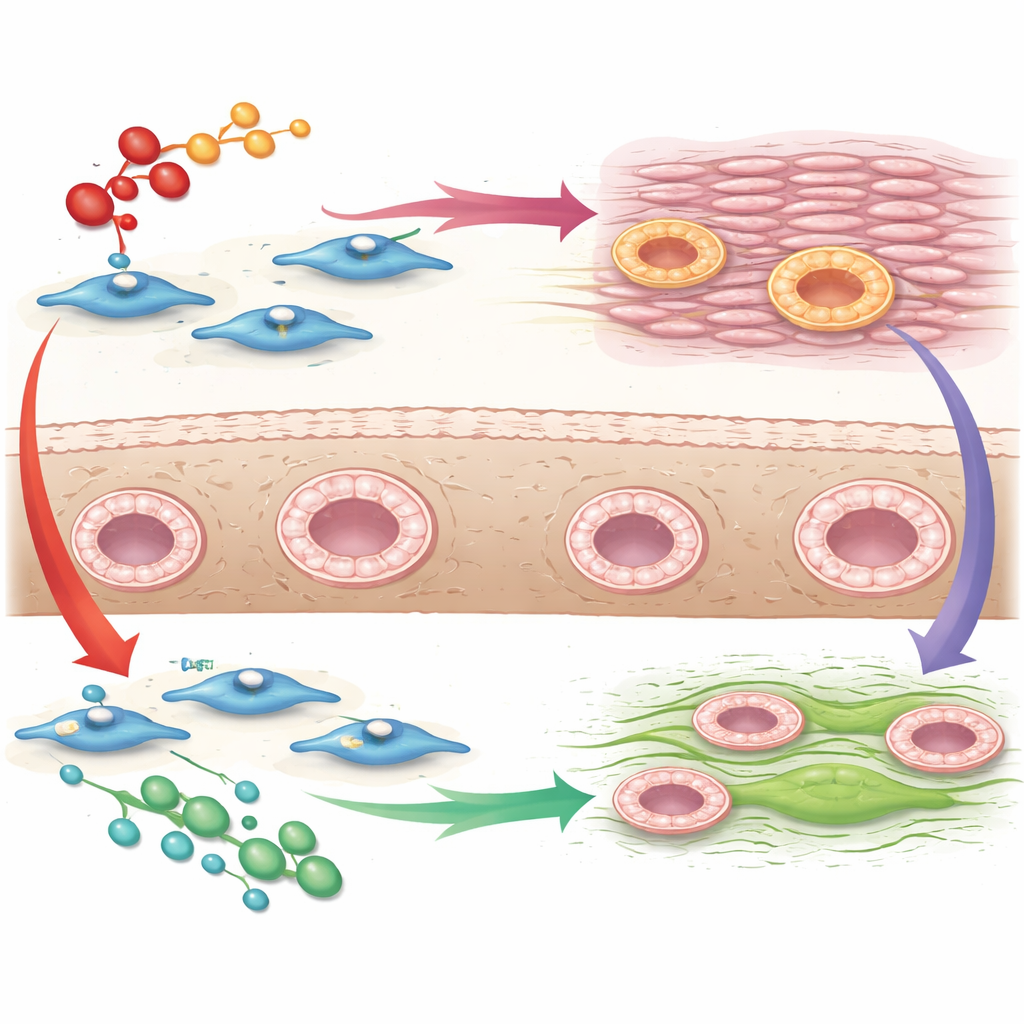
Een subtiel maar veelbelovend tegenwicht
De invloed van MFGE8 was bescheidener en leek het sterkst in een duidelijk subgroep van fibroblasten. In deze cellen wezen genpatronen op vertraagde groei en beweging, minder activatie van routes die gekoppeld zijn aan ongecontroleerde littekenvorming, en meer activiteit in een regulerend pad gecentreerd rond een eiwit genaamd PTEN, dat in andere organen helpt het littekenvormende gedrag te beperken. MFGE8 zette ook sommige fibroblastgroepen aan tot verhoogde type I-interferon-signalen—routes waarvan andere studies hebben aangetoond dat ze fibrose kunnen remmen—en verminderde de niveaus van LIF, een molecuul dat in nieren en longen aan schadelijke littekenvorming is gekoppeld. Niet elke wijziging wees eenduidig in een anti-littekenrichting, maar het algemene beeld suggereerde dat MFGE8 de neiging heeft om het uit de hand lopende herstel dat door het littekensignaal wordt getriggerd tegen te werken in plaats van te versterken.
Wat dit betekent voor toekomstige zorg van merries
Gezamenlijk bevestigt het werk het littekensignaal als een belangrijke aanjager van baarmoederschade bij ouder wordende merries en wijst het TAGLN aan als een praktisch merkteken voor actief littekenvormende cellen. Tegelijkertijd, door de nauwe koppeling tussen MFGE8 en fibrotische gebieden en de celniveau-effecten die beperkte groei en meer gebalanceerde signalering bevorderen, wordt het geïdentificeerd als een nieuwe en intrigerende speler die mogelijk helpt fibrose te beperken in plaats van te veroorzaken. Hoewel deze bevindingen vroeg zijn en gebaseerd op laboratoriummodellen, vormen ze de basis voor toekomstige strategieën die het evenwicht in de merriebaarmoeder kunnen doen verschuiven van littekenvorming naar gezond herstel, en zo mogelijk de vruchtbare jaren van waardevolle fokmerries kunnen verlengen.
Bronvermelding: zu Klampen, E., Neufeld, G. & Klein, C. Milk fat globule EGF and factor V/VIII domain containing (MFGE8) as a novel player in equine endometrial fibrosis. Sci Rep 16, 12045 (2026). https://doi.org/10.1038/s41598-026-46595-7
Trefwoorden: hengstachtige vruchtbaarheid, baarmoeder littekenvorming, fibrose, groeifactoren, single-cell-analyse