Clear Sky Science · nl
N2-(1-carboxyethyl)-2′-deoxyguanosine als genotoxische glycatie‑marker geassocieerd met veranderingen in chromatine‑architectuur bij plaveiselcelcarcinoom van de mond
Waarom dit belangrijk is voor dagelijkse tabaksgebruikers
Mondkanker is een groot en groeiend gezondheidsprobleem in Zuid‑Azië, vooral bij mensen die rookloze tabaksproducten gebruiken zoals gutka, naswar, paan en khaini. Deze studie kijkt onder de microscoop en stelt een simpele maar urgente vraag: wat doen deze producten precies met het DNA in de cellen van de mond? De onderzoekers richten zich op een specifiek soort chemisch litteken op DNA, genaamd CEdG, en tonen aan hoe dit alledaagse tabaksgewoonten verbindt met ingrijpende veranderingen in de manier waarop ons genetisch materiaal in cellen is verpakt en georganiseerd.
Een verborgen chemische stof in veel gebruikte kauwproducten
Rookloze tabak ontstaat door bladeren te drogen, te conserveren en te fermenteren. Deze stappen voegen niet alleen smaak toe: ze produceren reactieve chemicaliën die bekendstaan als glycotoxines. Eén daarvan, methylglyoxal, kan zonder enzymatische tussenkomst aan DNA binden. Wanneer het reageert met een DNA‑bouwsteen genaamd guanine, ontstaat een stabiele beschadiging die CEdG wordt genoemd. Eerder onderzoek bij andere ziekten liet zien dat CEdG DNA kan beschadigen en genetische fouten kan bevorderen, maar de rol ervan bij mondkanker was niet eerder onderzocht. In deze studie maten de auteurs eerst methylglyoxal in populaire merken rookloze tabak en vonden hoge niveaus in veelgebruikte producten zoals gutka, naswar, khaini en zarda, met lagere niveaus in paan en paan masala. Dit ondersteunt het idee dat gebruikers telkens wanneer ze tabak tegen wang of tandvlees houden hun mondcellen herhaaldelijk blootstellen aan methylglyoxal.
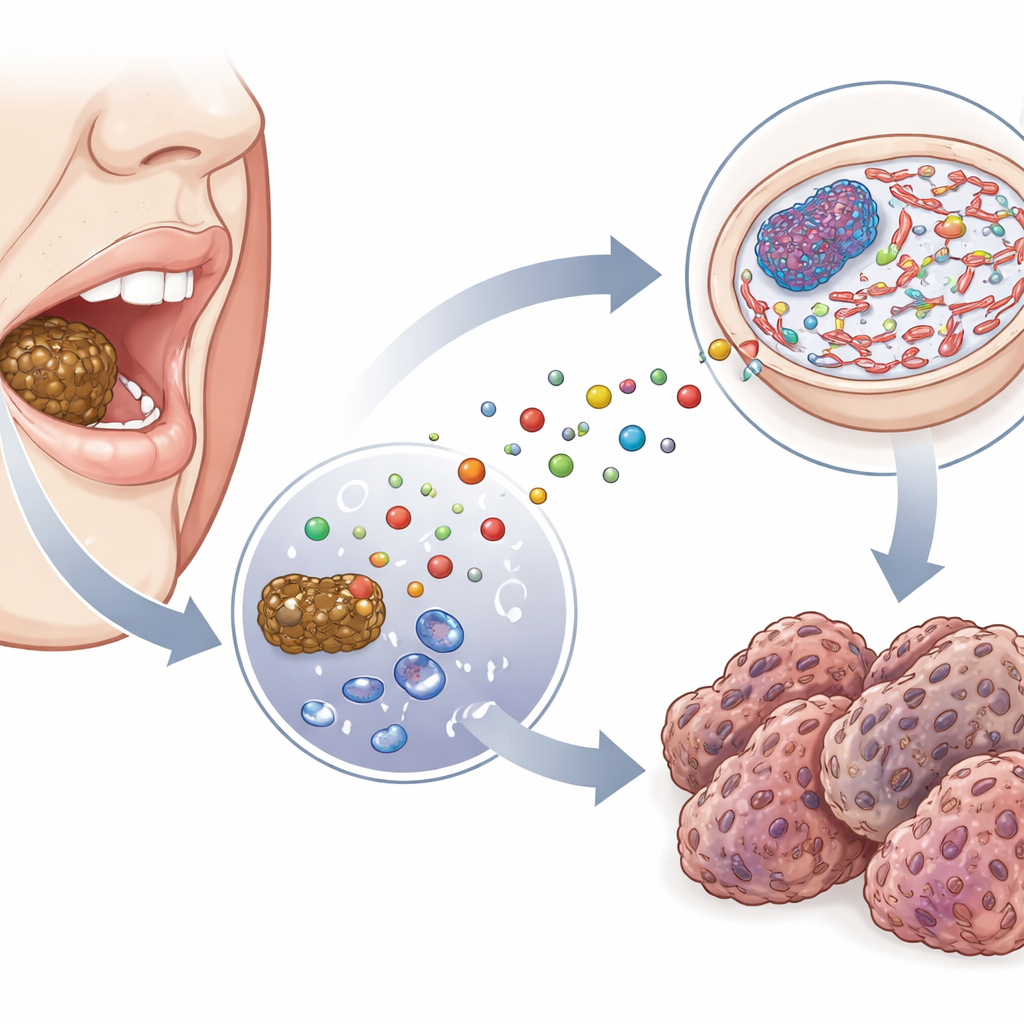
DNA‑littekenen in mondtumoren volgen
Om te zien of deze blootstelling een spoor op DNA achterlaat, onderzocht het team weefselmonsters van patiënten met plaveiselcelcarcinoom van de mond en vergeleek die met normaal weefsel dat uit dezelfde mond en op korte afstand van de tumor was genomen. Met een fluorescerend antilichaam dat specifiek CEdG herkent, visualiseerden ze waar deze DNA‑beschadiging in cellen voorkomt. Kankergezwellen toonden veel meer fel gekleurde kernen, een hoger totaal signaal en grotere variatie van cel tot cel dan nabijgelegen gezond weefsel. Belangrijk is dat het oplichten zich concentreerde in de kern, waar het DNA van de cel is opgeslagen, en niet in het omringende cytoplasma. Deze patronen wijzen erop dat CEdG niet alleen aanwezig is maar verrijkt in het genetisch materiaal van tumorcellen bij mensen die rookloze tabak gebruiken.
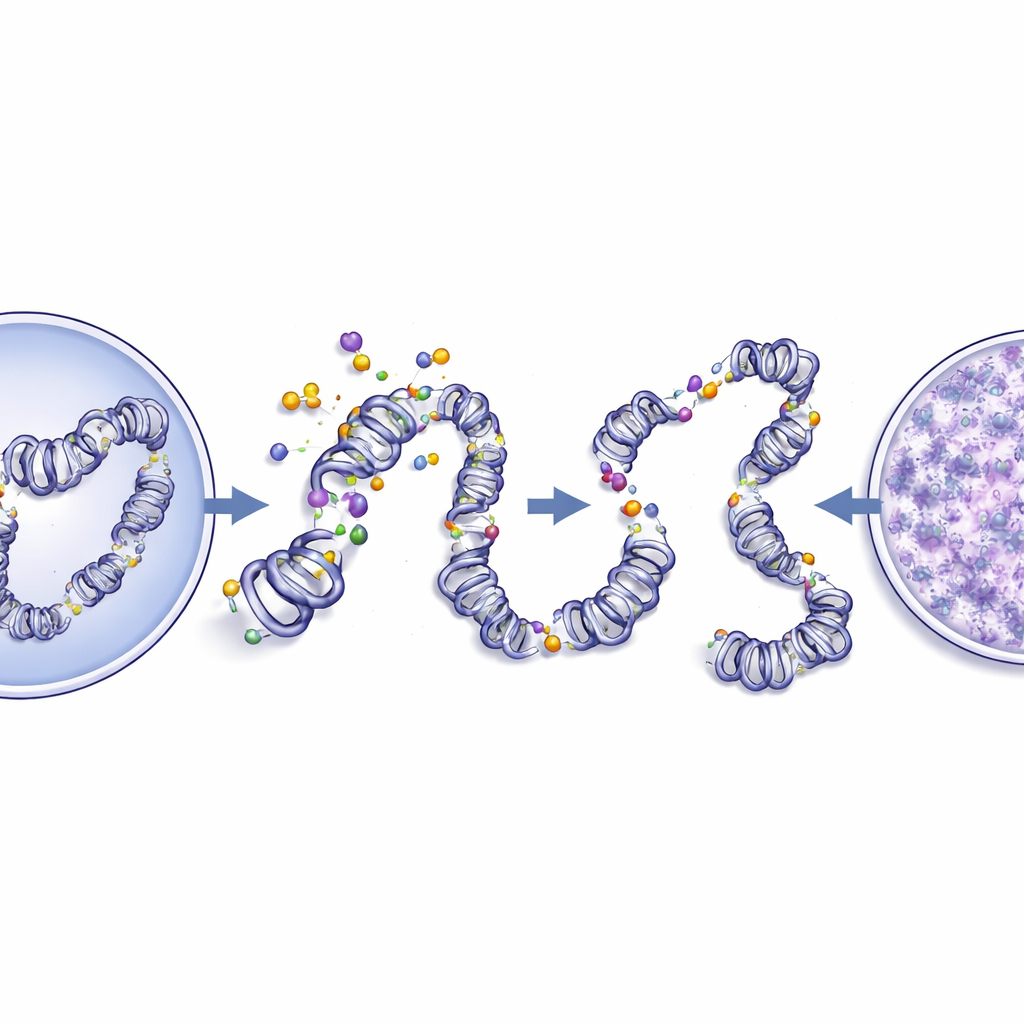
Wanneer DNA‑verpakking van ordelijk naar chaotisch verandert
In gezonde cellen is DNA geen losse streng; het is gevouwen in een zorgvuldig gelaagde structuur die chromatine heet. De manier waarop dit materiaal is verpakt beïnvloedt welke genen aan of uit staan. De onderzoekers gebruikten hoge‑resolutiebeelden van standaard gekleurde preparaten om de grootte en vorm van kernen te meten en de fijne textuur van chromatine te analyseren. Vergeleken met normaal weefsel hadden kankercellen grotere, onregelmatiger kernen en chromatine dat er meer gedesorganiseerd en 'korrelig' uitzag. Digitale analyse liet hogere entropie, contrast en fractale dimensie zien—kenmerken die duiden op een meer chaotische, minder compacte ordening—en verlaagde maten van orde en gladheid. Wanneer deze beeldgebaseerde metingen rechtstreeks werden vergeleken met CEdG‑niveaus, ging sterkere CEdG‑kleuring samen met meer verstoorde chromatinetextuur. Deze nauwe correlatie suggereert dat DNA‑glycatie en de architectonische herinrichting van chromatine nauw aan elkaar verbonden zijn in mondtumoren.
Tabaksblootstelling, DNA‑schade en tumorgedrag met elkaar verbinden
Door chemische metingen in tabaksproducten te combineren met precisie‑imaging van DNA‑letsels en computationele analyse van kernstructuur, schetst de studie een keten van gebeurtenissen: methylglyoxalrijke rookloze tabak kan CEdG in DNA genereren; CEdG is overvloedig en ongelijke verdeeld binnen de kernen van orale kankercellen; en hogere CEdG‑niveaus correleren met kernen waarvan het chromatine zijn normale organisatie heeft verloren. Omdat chromatinestructuur helpt bepalen welke genen actief zijn, kan zulke desorganisatie bijdragen aan de onstabiele genexpressiepatronen die kankerontwikkeling en uitzaaiing stimuleren. Het werk benadrukt ook CEdG als een specifiek type marker—een die directe schade aan DNA weerspiegelt door een bekende omgevingsblootstelling, in plaats van een downstream reactiemolecuul.
Wat dit kan betekenen voor preventie en zorg
Voor het grote publiek is de kernboodschap dat rookloze tabak niet alleen het mondoppervlak irriteert; het kan blijvende chemische littekens op DNA achterlaten die gekoppeld zijn aan de interne architectuur van het genetisch materiaal in onze cellen. Hoewel deze studie nog niet kan aantonen dat CEdG mondkanker veroorzaakt, laat ze zien dat hogere niveaus van dit letsel samengaan met zowel zware methylglyoxalblootstelling als ingrijpende verstoring van chromatine in tumoren. Met verder onderzoek in grotere groepen en preciezere metingen zou CEdG een weefselgebaseerd teken van tabaksgerelateerde DNA‑schade kunnen worden en mogelijk een hulpmiddel voor het volgen van risico of behandelrespons bij mensen die rookloze tabak gebruiken.
Bronvermelding: Khan, G., Waraich, R.S., Khan, H. et al. N2-(1-carboxyethyl)-2′-deoxyguanosine as a genotoxic glycation marker associated with chromatin architectural alterations in oral squamous cell carcinoma. Sci Rep 16, 12715 (2026). https://doi.org/10.1038/s41598-026-45839-w
Trefwoorden: mondkanker, rookloze tabak, DNA‑schade, chromatinestructuur, methylglyoxal