Clear Sky Science · de
N2-(1-carboxyethyl)-2′-deoxyguanosin als genotoxischer Glykationsmarker, verbunden mit Veränderungen der Chromatinarchitektur bei Plattenepithelkarzinomen der Mundhöhle
Warum das für alltägliche Tabaknutzer wichtig ist
Mundkrebs ist ein großes und zunehmendes Gesundheitsproblem in Südasien, besonders bei Menschen, die rauchlose Tabakprodukte wie Gutka, Naswar, Paan und Khaini verwenden. Diese Studie blickt unter das Mikroskop, um eine einfache, aber dringende Frage zu stellen: Was genau bewirken diese Produkte an der DNA in den Zellen der Mundhöhle? Die Forschenden konzentrieren sich auf eine spezielle chemische Narbe auf der DNA, genannt CEdG, und zeigen, wie sie alltägliche Tabakgewohnheiten mit tiefgreifenden Veränderungen in der Art und Weise verbindet, wie unser Erbgut in den Zellen verpackt und organisiert ist.
Ein versteckter Stoff in gängigen Kautabakprodukten
Rauchloser Tabak entsteht durch Trocknen, Fermentieren und Konservieren von Blättern. Diese Schritte tun mehr, als nur Geschmack zu erzeugen: Sie erzeugen reaktive Chemikalien, sog. Glykotoxine. Eines davon, Methylglyoxal, kann ohne Hilfe von Enzymen an die DNA binden. Wenn es mit einer DNA-Baustein namens Guanin reagiert, entsteht eine stabile Läsion, CEdG. Frühere Arbeiten bei anderen Krankheiten zeigten, dass CEdG DNA schädigen und genetische Fehler fördern kann, doch seine Rolle beim Mundkrebs war bislang unerforscht. In dieser Studie maßen die Autorinnen und Autoren zunächst Methylglyoxal in populären Marken rauchlosen Tabaks und fanden hohe Konzentrationen in weit verbreiteten Produkten wie Gutka, Naswar, Khaini und Zarda, mit niedrigeren Werten in Paan und Paan Masala. Das stützt die Idee, dass Nutzerinnen und Nutzer die Zellen ihrer Mundhöhle bei jedem Hinaushalten von Tabak gegen Wange oder Zahnfleisch wiederholt Methylglyoxal aussetzen.
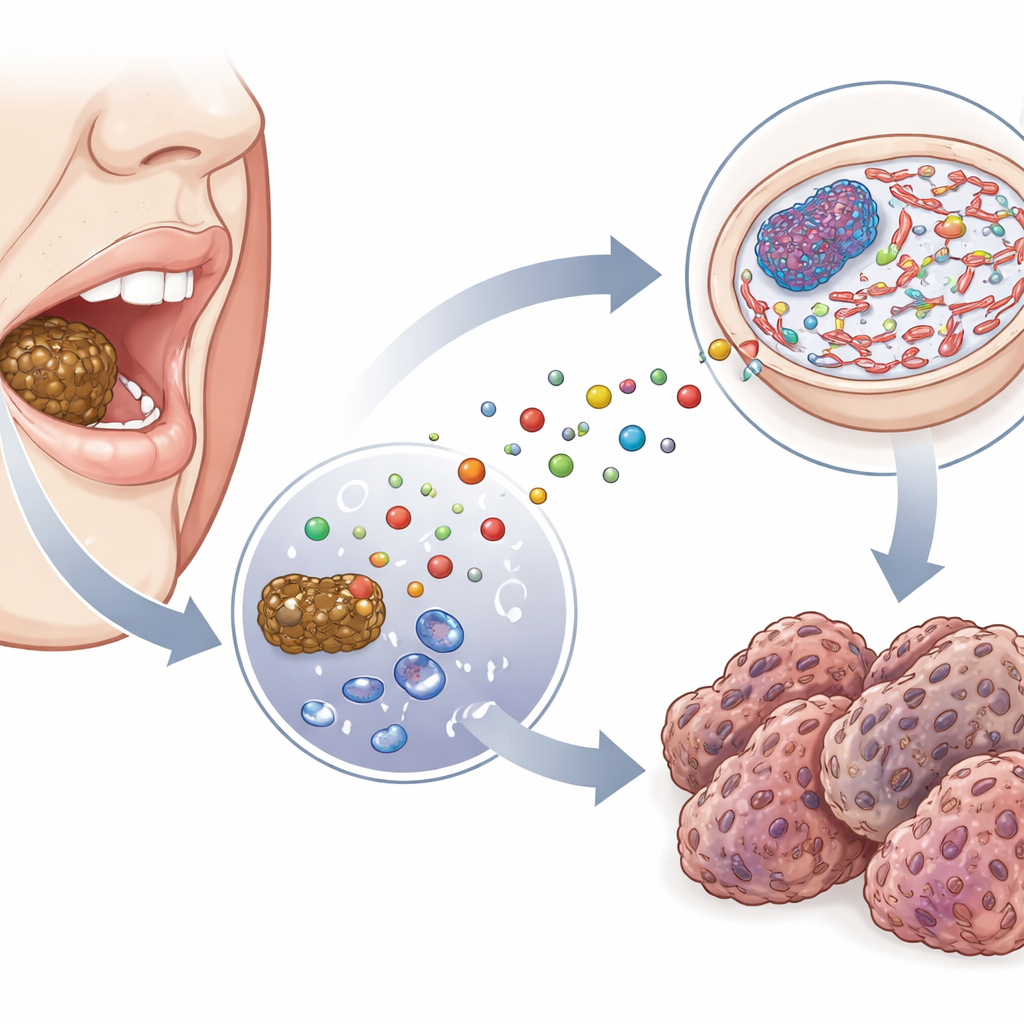
DNA-Narben in Mundtumoren nachverfolgen
Um zu sehen, ob diese Exposition Spuren in der DNA hinterlässt, untersuchte das Team Gewebeproben von Patientinnen und Patienten mit Plattenepithelkarzinom der Mundhöhle und verglich sie mit normalem Gewebe, das aus demselben Mund in kurzer Entfernung zum Tumor entnommen wurde. Mit einem fluoreszierenden Antikörper, der spezifisch CEdG erkennt, visualisierten sie, wo diese DNA-Läsion innerhalb der Zellen auftritt. Das Tumorgewebe zeigte deutlich mehr hell gefärbte Zellkerne, ein insgesamt stärkeres Signal und größere Unterschiede von Zelle zu Zelle als das nahegelegene gesunde Gewebe. Wichtig war, dass das Leuchten im Zellkern konzentriert war, also an dem Ort, an dem die DNA gespeichert ist, und nicht im umgebenden Zytoplasma. Diese Muster deuten darauf hin, dass CEdG nicht nur vorhanden, sondern in dem Erbgut von Tumorzellen bei Personen, die rauchlosen Tabak verwenden, angereichert ist.
Wenn die DNA-Verpackung von geordnet zu chaotisch wird
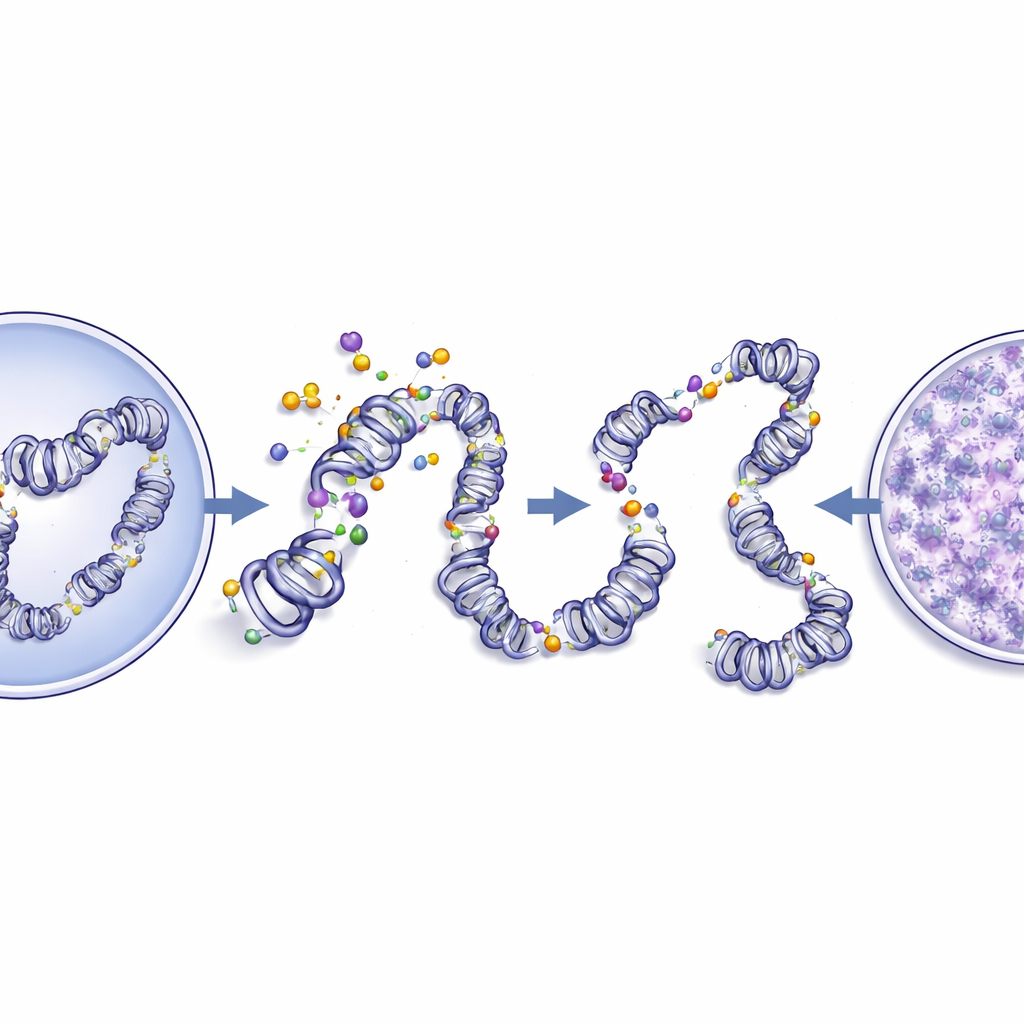
Die DNA in gesunden Zellen ist nicht einfach eine lose Schnur; sie ist zu einer sorgfältig geschichteten Struktur gefaltet, dem Chromatin. Die Art, wie dieses Material verpackt ist, beeinflusst, welche Gene an- oder abgeschaltet sind. Die Forschenden nutzten hochauflösende Bilder von standardmäßig gefärbten Schnitten, um Größe und Form der Zellkerne zu messen und die feine Textur des Chromatins zu analysieren. Im Vergleich zum normalen Gewebe hatten Krebszellen größere, unregelmäßigere Kerne und ein Chromatinbild, das unorganisierter und „körniger“ wirkte. Die digitale Analyse zeigte höhere Entropie, Kontrast und fraktale Dimension – Merkmale, die auf eine chaotischere, weniger kompakte Anordnung hinweisen – sowie verminderte Maße für Ordnung und Glätte. Beim direkten Vergleich dieser bildbasierten Messungen mit CEdG-Werten gingen stärkeres CEdG-Färben und eine stärker gestörte Chromatintextur Hand in Hand. Diese enge Korrelation legt nahe, dass DNA-Glykation und der architektonische Umbau des Chromatins in Mundtumoren eng miteinander verknüpft sind.
Tabakexposition, DNA-Schäden und Tumorverhalten verknüpfen
Durch die Kombination chemischer Messungen in Tabakprodukten, präziser Bildgebung von DNA-Läsionen und computergestützter Analyse der Kernstruktur skizziert die Studie eine Ereigniskette: Methylglyoxal-reicher rauchloser Tabak kann CEdG in der DNA erzeugen; CEdG ist in den Zellkernen von Mundtumoren häufig und ungleich verteilt; und höhere CEdG-Werte korrelieren mit Kernen, deren Chromatin seine normale Organisation verloren hat. Da die Chromatinstruktur mitbestimmt, welche Gene aktiv sind, kann eine solche Desorganisation zu instabilen Genaktivitätsmustern beitragen, die das Tumorwachstum und die Ausbreitung fördern. Die Arbeit hebt zudem CEdG als einen eigenständigen Marker hervor — einen, der direkte Schäden an der DNA durch eine bekannte Umweltbelastung widerspiegelt, statt ein nachgeschaltetes Reaktionsmolekül.
Was das für Prävention und Versorgung bedeuten könnte
Für Laien ist die Kernbotschaft: Rauchloser Tabak reizt nicht nur die Mundoberfläche; er kann dauerhafte chemische Narben in der DNA hinterlassen, die mit der inneren Architektur des Erbguts unserer Zellen verbunden sind. Obwohl diese Studie noch nicht beweisen kann, dass CEdG Mundkrebs verursacht, zeigt sie, dass höhere Werte dieser Läsion sowohl mit starker Methylglyoxal-Exposition als auch mit tiefgreifender Störung des Chromatins in Tumoren einhergehen. Mit weiteren Untersuchungen in größeren Kohorten und präziseren Messungen könnte CEdG zu einem gewebebasierten Hinweis auf tabakbedingte DNA-Schäden werden und möglicherweise ein Instrument zur Risikoüberwachung oder zur Bewertung des Therapieansprechens bei Nutzerinnen und Nutzern rauchlosen Tabaks darstellen.
Zitation: Khan, G., Waraich, R.S., Khan, H. et al. N2-(1-carboxyethyl)-2′-deoxyguanosine as a genotoxic glycation marker associated with chromatin architectural alterations in oral squamous cell carcinoma. Sci Rep 16, 12715 (2026). https://doi.org/10.1038/s41598-026-45839-w
Schlüsselwörter: Mundkrebs, rauchloser Tabak, DNA-Schäden, Chromatinstruktur, Methylglyoxal