Clear Sky Science · nl
Voorspellende simulaties van houdingscontrole: de rol van signaalruis en neurale vertragingen bij de ziekte van Parkinson onderzoeken
Waarom balansproblemen bij Parkinson belangrijk zijn
Veel mensen met de ziekte van Parkinson maken zich het meest zorgen over iets heel alledaags: rechtop blijven staan. Naarmate de ziekte vordert, kan zelfs stilstaand staan onstabiel worden, wat het risico op vallen en letsel vergroot. Artsen zien echter alleen het zichtbare gewiebel, niet de interne werking van het zenuwstelsel die het veroorzaakt. Deze studie gebruikt computersimulaties van lichaam en brein die samenwerken om twee verborgen verdachten te onderzoeken — ruizige bewegingssignalen en vertraagde zenuwverwerking — en hoe die de balans bij de ziekte van Parkinson kunnen verslechteren.
Inzicht in het balanssysteem
Om in balans te blijven houdt ons lichaam voortdurend het zwaartepunt boven de voeten. Zintuiglijke prikkels in de huid, spieren, het binnenoor en de ogen sturen informatie naar de hersenen, die vervolgens commando’s naar de beenspieren en romp sturen om kleine correcties uit te voeren. Deze cyclus draait vele keren per seconde en wordt altijd beïnvloed door achtergrond «gepraat» zoals ademhaling, hartslag en willekeurige fluctuaties in zenuwsignalen. Bij de ziekte van Parkinson vertraagt en verandert de ritmiek in diepe hersenregio’s, de basale ganglia, waardoor bewegingen trager worden; hoe dit precies de lus voor staande balans beïnvloedt, is moeilijk direct in levende mensen te meten.
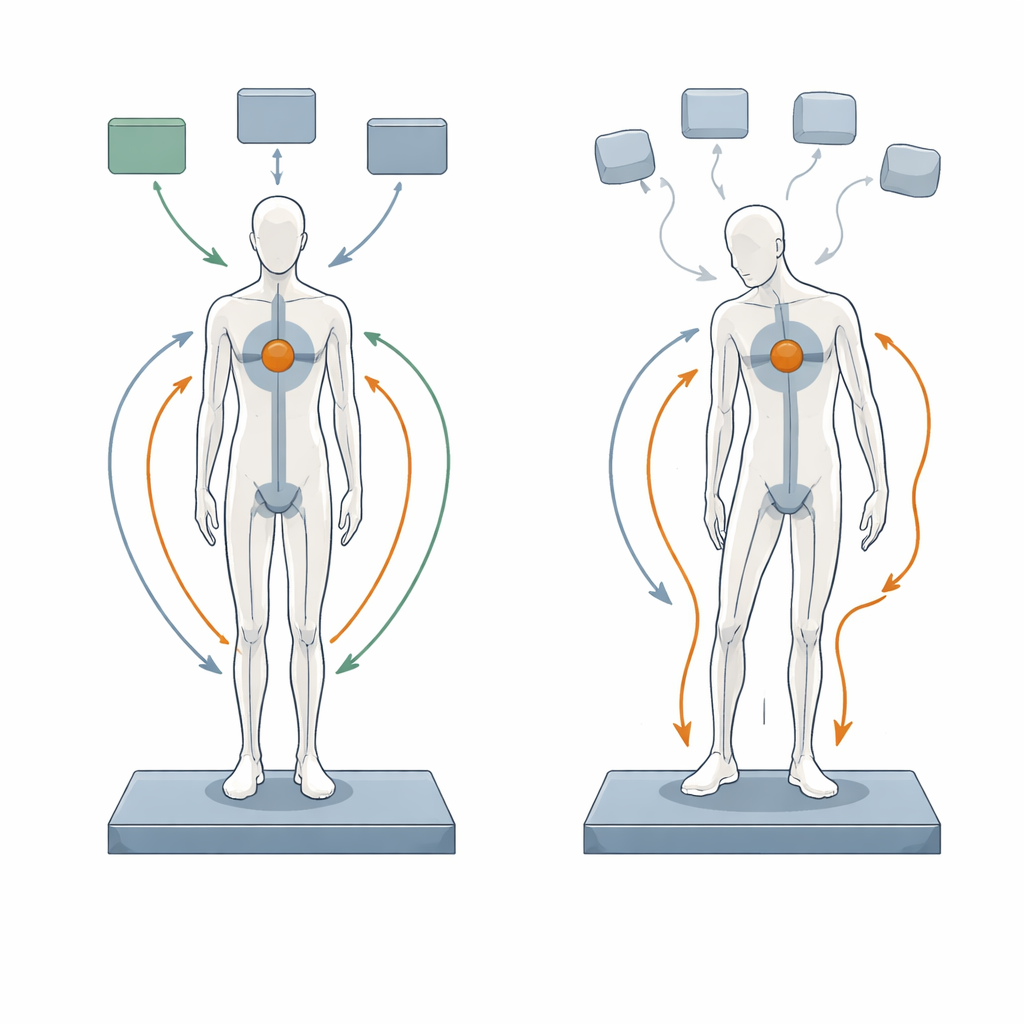
Een virtueel persoon bouwen
De onderzoekers bouwden voort op een bestaand digitaal model dat een vereenvoudigd menselijk skelet en beenspieren koppelt aan een regelsysteem dat het zenuwstelsel vertegenwoordigt. In deze virtuele persoon rapporteren sensors de lichaamshouding, vergelijkt een controller dit met een ideale rechtopstaande houding en stuurt vervolgens commando’s naar de spieren, die krachten genereren en de gewrichten bewegen. Het model bevat ook realistische vertragingen terwijl signalen door zenuwen en hersenbanen reizen, plus willekeurige interne ruis die wordt toegevoegd aan de uitgaande motorcommando’s. Door de hoeveelheid ruis of de lengte van de vertraging aan te passen, kon het team zien hoe het gesimuleerde lichaam gedurende 75 seconden stilstaand voor- en achteruit zwaaide, en deze resultaten vergelijken met bewegingsopnamedata van 31 mensen met Parkinson en 31 gezonde leeftijdsgenoten.
Hoe ruizige signalen het zwaaien veranderen
In de eerste reeks simulaties verhoogde het team twee typen ruis in de uitgaande spiercommando’s: constante achtergrondruis en signaalafhankelijke ruis die toenam met de sterkte van het commando. Naarmate een van beide typen ruis toenam, zwaaide de virtuele persoon meer. Het traject van de druk onder de voeten werd langer en breder, en de gewrichten in bekken, heupen, knieën en enkels doorliepen grotere hoeken. Ook nam de spieractiviteit toe, wat de extra inspanning weerspiegelt die nodig is om het wankelere lichaam te beheersen. Deze patronen kwamen sterk overeen met de verschillen tussen de gezonde vrijwilligers en mensen met Parkinson, vooral voor de constante achtergrondruis, wat suggereert dat minder precieze motorische signalen een belangrijke bijdrage kunnen leveren aan reële instabiliteit.
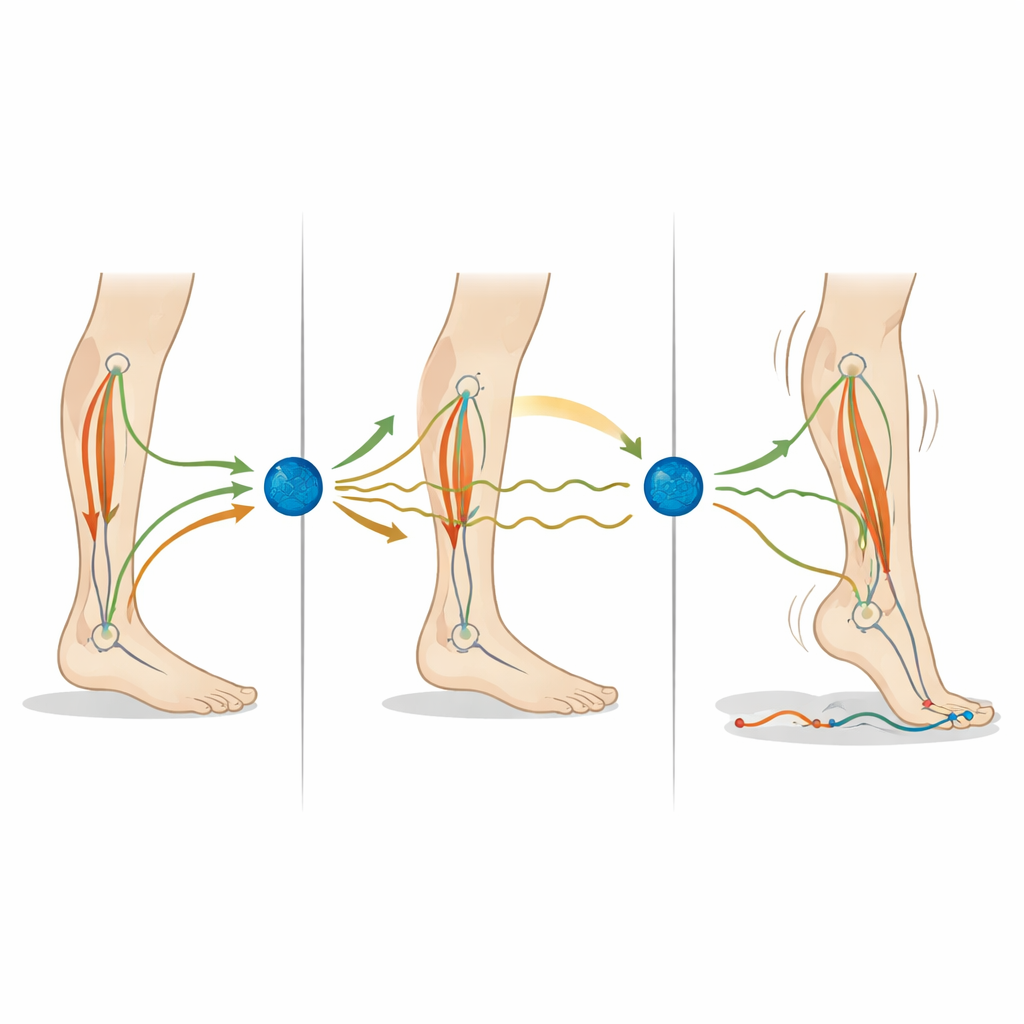
Wat tragere zenuwen doen met staan
Vervolgens verlengden de onderzoekers de totale tijd die signalen nodig hebben om door de balanslus te reizen, om tragere neurale verwerking na te bootsen. Met extra vertraging namen de meeste maatstaven voor zwaaien opnieuw toe: het gesimuleerde drukcentrum zwierf verder en de gewrichtsbewegingen werden groter. Deze veranderingen traden op ongeacht of het model begon met weinig of veel ruis, hoewel sommige zwaai‑eigenschappen, zoals de exacte voor‑achterpositie van de druk onder de voeten en de gemiddelde zwaaifrequentie, weinig veranderden — een weerspiegeling van de experimentele data. De resultaten suggereren dat zowel meer ruis in signalen als langere verwerkingstijden het zenuwstelsel in een minder stabiele manier van staan kunnen duwen die lijkt op de ziekte van Parkinson.
Wat dit betekent voor mensen met Parkinson
Voor niet‑experts is de kernboodschap dat balansproblemen bij Parkinson niet alleen kunnen voortkomen uit zwakke spieren of stijve gewrichten, maar ook uit verborgen veranderingen in hoe zuiver en hoe snel het brein en de zenuwen communiceren. Door deze interne factoren in een virtuele patiënt bij te stellen en de uitkomsten te matchen met echte bewegingsdata, toont de studie aan dat toegenomen ruis en vertraagde verwerking samen Parkinson‑achtig zwaaien kunnen nabootsen. In de toekomst zouden vergelijkbare modellen artsen kunnen helpen om iemands interne regels instelllingen te schatten met eenvoudige balanstests, te volgen hoe deze in de loop van de tijd of met behandeling veranderen, en uiteindelijk meer gerichte therapieën en revalidatieprogramma’s te ontwerpen om mensen stabieler op de been te houden.
Bronvermelding: Shanbhag, J., Wechsler, I., Fleischmann, S. et al. Predictive simulations of postural control: exploring the role of signal noise and neural delays in Parkinson’s disease. Sci Rep 16, 9849 (2026). https://doi.org/10.1038/s41598-026-45161-5
Trefwoorden: Ziekte van Parkinson, houdingscontrole, balans, neuromusculoskeletale simulatie, vallen