Clear Sky Science · fr
Simulations prédictives du contrôle postural : explorer le rôle du bruit du signal et des délais neuronaux dans la maladie de Parkinson
Pourquoi les problèmes d’équilibre dans la maladie de Parkinson importent
Beaucoup de personnes atteintes de la maladie de Parkinson craignent surtout quelque chose de très terre‑à‑terre : rester debout. À mesure que la maladie progresse, même la station debout au repos peut devenir instable, augmentant le risque de chutes et de blessures. Pourtant, les médecins ne voient que le balancement extérieur, pas le fonctionnement interne du système nerveux qui en est la cause. Cette étude utilise des simulations informatiques du corps et du cerveau travaillant ensemble pour explorer deux suspects cachés — des signaux moteurs bruyants et un traitement nerveux ralenti — et comment ils pourraient aggraver l’équilibre dans la maladie de Parkinson.
Regarder à l’intérieur du système d’équilibre
Pour rester en équilibre, notre corps maintient en permanence le centre de masse au‑dessus des pieds. Des capteurs dans la peau, les muscles, l’oreille interne et les yeux envoient des informations au cerveau, qui transmet ensuite des commandes aux muscles des jambes et du tronc pour effectuer de petites corrections. Ce cycle fonctionne plusieurs fois par seconde et est toujours influencé par le « bruit » de fond provenant de la respiration, du rythme cardiaque et des fluctuations aléatoires des signaux nerveux. Dans la maladie de Parkinson, des altérations de régions profondes du cerveau appelées ganglions de la base ralentissent le mouvement et modifient l’activité rythmique cérébrale, mais il est difficile de mesurer directement comment cela affecte la boucle de contrôle de la station debout chez de vraies personnes.
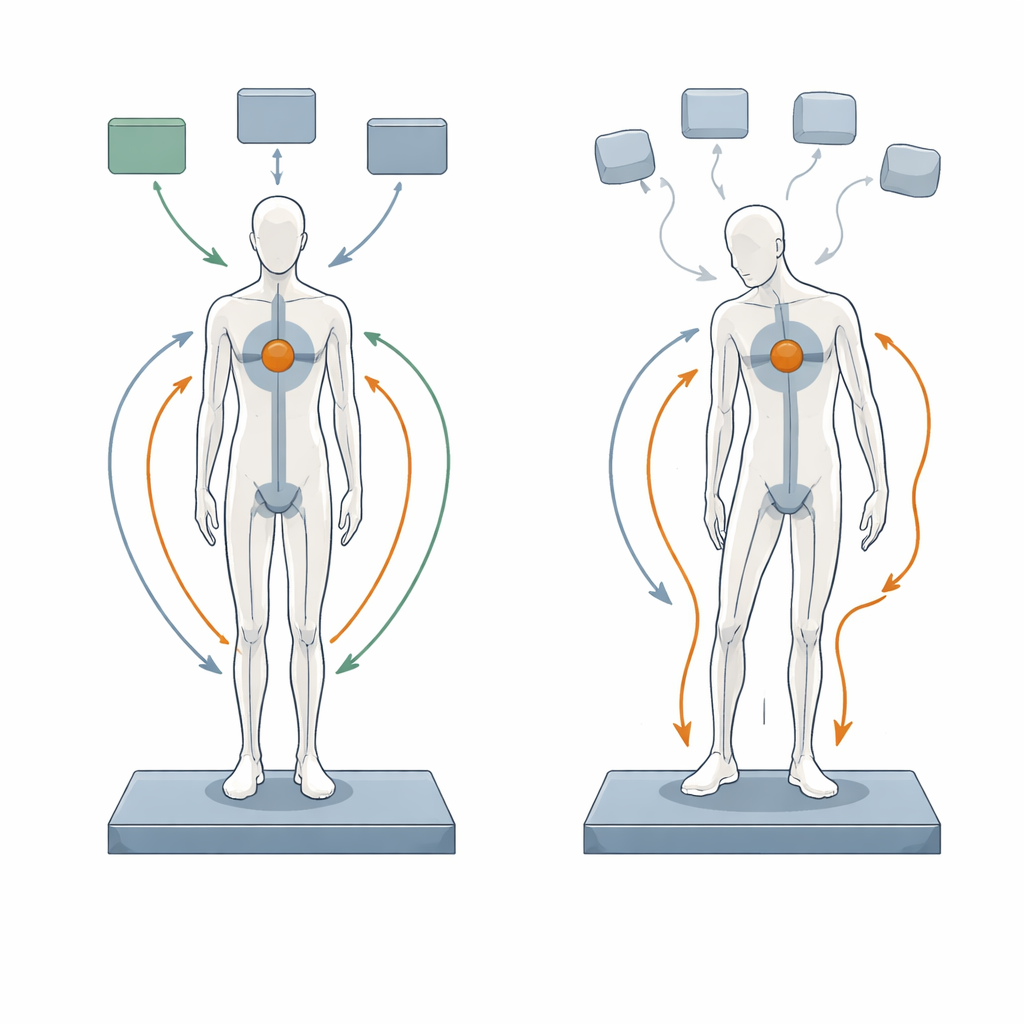
Construire une personne virtuelle
Les chercheurs se sont appuyés sur un modèle numérique existant qui relie un squelette humain simplifié et les muscles des jambes à un système de contrôle représentant le système nerveux. Dans cette personne virtuelle, les signaux sensoriels renseignent sur la position du corps, un contrôleur compare cela à une posture verticale idéale, puis envoie des commandes aux muscles, lesquels génèrent des forces et déplacent les articulations. Le modèle inclut aussi des délais réalistes pendant que les signaux circulent le long des nerfs et à travers les voies cérébrales, ainsi qu’un bruit interne aléatoire ajouté aux commandes motrices sortantes. En ajustant la quantité de bruit ou la durée des délais, l’équipe a pu observer comment le corps simulé se balançait d’avant en arrière pendant 75 secondes de station debout au repos, puis comparer ces résultats à des données de capture de mouvement provenant de 31 personnes atteintes de Parkinson et de 31 témoins en bonne santé.
Comment des signaux bruyants modifient le balancement
Dans la première série de simulations, l’équipe a augmenté deux types de bruit dans les commandes musculaires sortantes : un bruit de fond constant et un bruit dépendant du signal qui augmentait avec la force de la commande. À mesure que l’un ou l’autre type de bruit augmentait, la personne virtuelle se balançait davantage. La trajectoire tracée par la pression sous les pieds devenait plus longue et plus large, et les articulations du bassin, des hanches, des genoux et des chevilles parcouraient des amplitudes plus grandes. L’activité musculaire augmentait également, reflétant l’effort supplémentaire nécessaire pour contrôler un corps plus instable. Ces schémas correspondaient étroitement aux différences observées entre les volontaires sains et ceux atteints de Parkinson, en particulier pour le bruit de fond constant, ce qui suggère que des signaux moteurs moins précis pourraient être un contributeur clé de l’instabilité réelle.
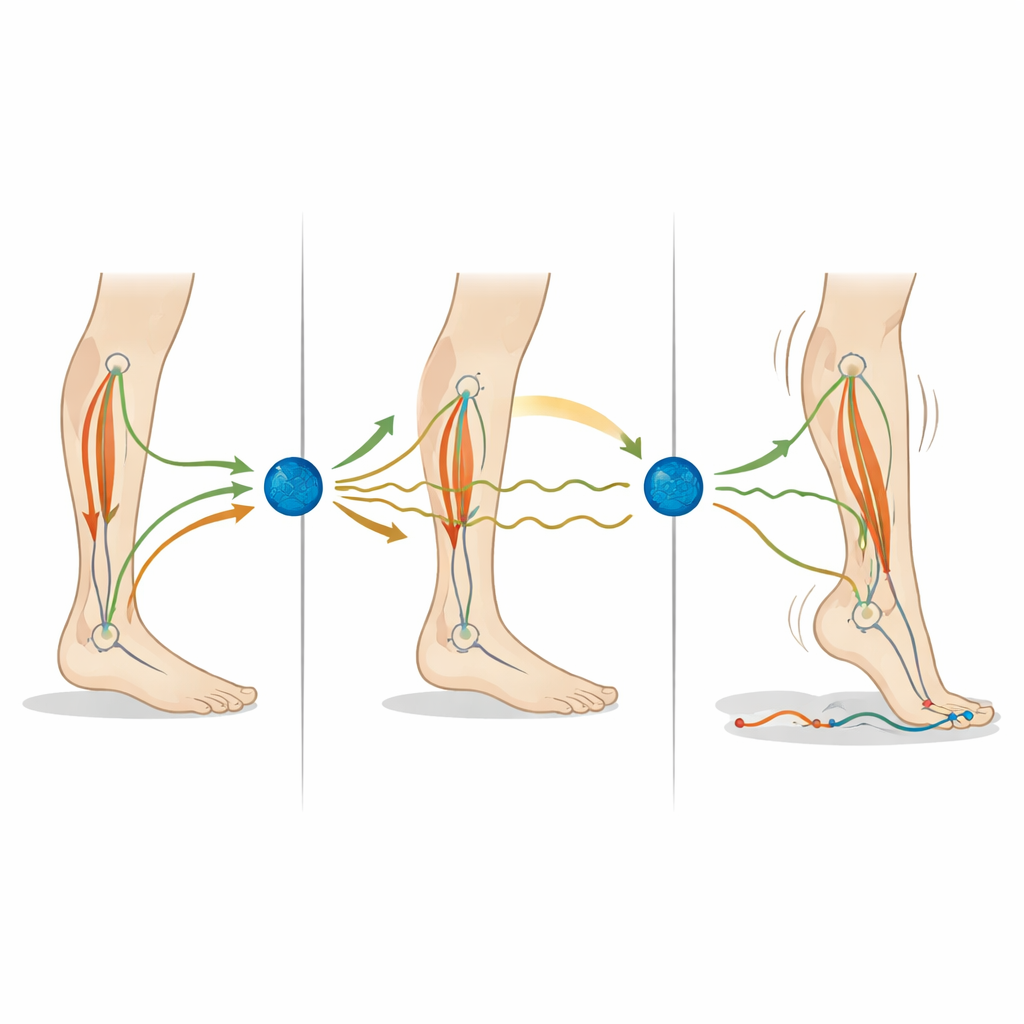
Ce que des nerfs plus lents font à la station debout
Puis, les chercheurs ont allongé le temps total de transit des signaux à travers la boucle de contrôle de l’équilibre, mimant un traitement neural plus lent. Avec ce délai additionnel, la plupart des mesures de balancement augmentaient à nouveau : le centre de pression simulé errait davantage et les mouvements articulaires devenaient plus importants. Ces changements apparaissaient que le modèle parte d’un faible ou d’un fort niveau de bruit, bien que certaines caractéristiques du balancement, comme la position exacte avant‑arrière de la pression sous les pieds et la fréquence moyenne du balancement, aient peu changé — reflétant les données expérimentales. Les résultats suggèrent que des signaux plus bruyants et des temps de traitement plus longs peuvent tous deux pousser le système nerveux vers une façon de se tenir moins stable, ressemblant à la station debout observée dans la maladie de Parkinson.
Ce que cela signifie pour les personnes atteintes de Parkinson
Pour les non‑spécialistes, le message clé est que les problèmes d’équilibre dans la maladie de Parkinson peuvent provenir non seulement de muscles faibles ou d’articulations raides, mais aussi de changements cachés dans la qualité et la rapidité de la communication entre le cerveau et les nerfs. En ajustant ces facteurs internes dans un patient virtuel et en comparant les résultats à des données réelles de mouvement, l’étude montre que l’augmentation du bruit et les délais de traitement peuvent conjointement recréer un balancement de type Parkinson. À l’avenir, des modèles similaires pourraient aider les médecins à estimer les réglages de contrôle internes d’une personne à partir de simples tests d’équilibre, suivre leur évolution dans le temps ou sous traitement, et finalement concevoir des thérapies et des programmes de rééducation plus ciblés pour maintenir les personnes plus stables sur leurs pieds.
Citation: Shanbhag, J., Wechsler, I., Fleischmann, S. et al. Predictive simulations of postural control: exploring the role of signal noise and neural delays in Parkinson’s disease. Sci Rep 16, 9849 (2026). https://doi.org/10.1038/s41598-026-45161-5
Mots-clés: maladie de Parkinson, contrôle postural, équilibre, simulation neuromusculosquelettique, chutes