Clear Sky Science · nl
Proteomische analyse identificeert verschillende signaalroutes bij lumbale tussenwervelschijfdegeneratie tussen type 2-diabetische en niet-diabetische patiënten
Waarom je rug en bloedglucose met elkaar verbonden zijn
Laag rugpijn is een van de belangrijkste redenen waarom mensen werk missen, en versleten tussenwervelschijven liggen vaak aan de basis. Deze studie stelt een vraag die voor miljoenen mensen met type 2-diabetes van belang is: verandert diabetes de manier waarop de zachte kussentjes tussen de wervellichamen afbreken, en zo ja, hoe? Door in te zoomen op duizenden eiwitten in deze schijven, onthullen de onderzoekers onderscheidende moleculaire patronen die verschillen tussen mensen met en zonder diabetes, en bieden ze aanwijzingen waarom rugproblemen bij sommige patiënten ernstiger of eerder kunnen optreden.
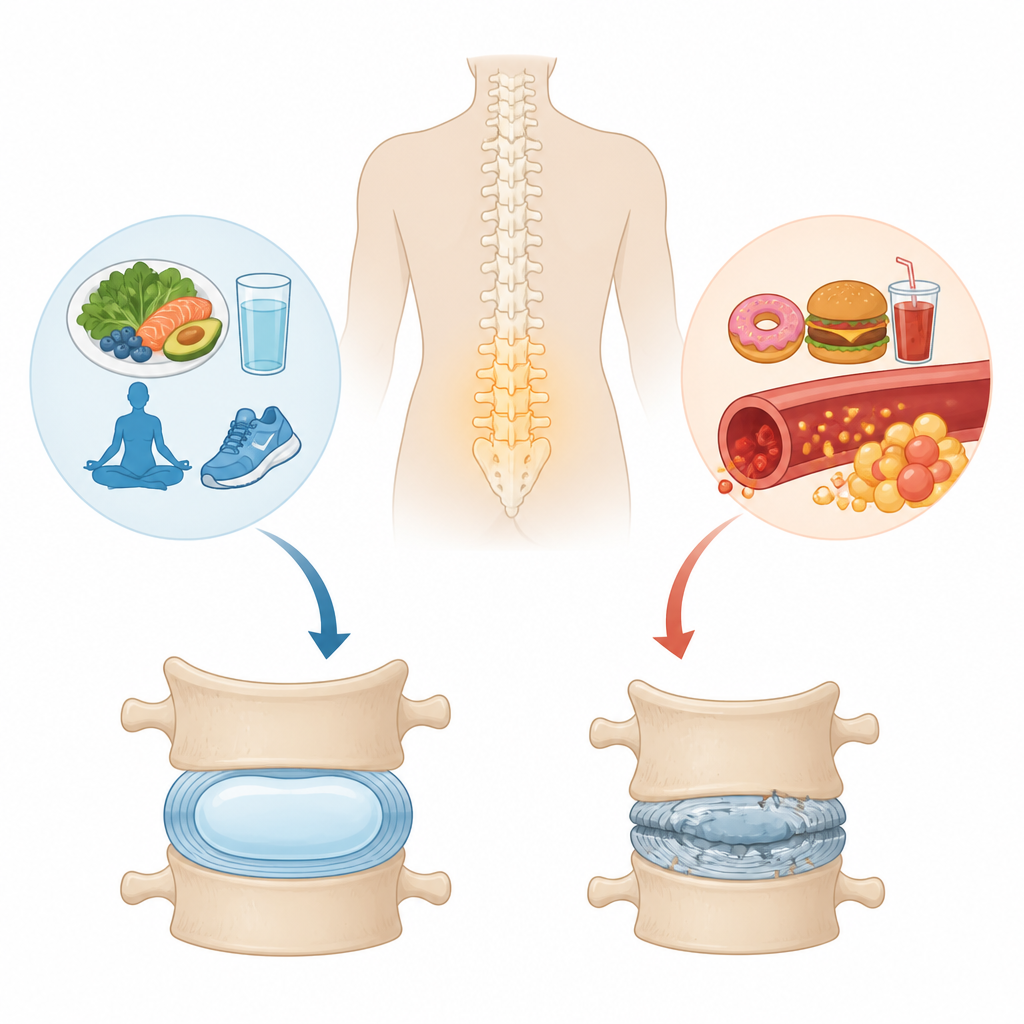
De kussentjes die ons in beweging houden
Tussen elke wervel bevindt zich een klein, geleiachtig kussentje genaamd een tussenwervelschijf. Het centrum, de nucleus pulposus, is rijk aan waterbindende eiwitten die als schokdemper fungeren. In de loop van de tijd, of na letsel, kan deze structuur slijten — een proces dat bekendstaat als schijfdegeneratie en dat nauw samenhangt met chronische lage rugpijn. Type 2-diabetes, een langdurige aandoening gekoppeld aan hoge bloedglucose en laaggradige ontsteking, is in grote bevolkingsstudies in verband gebracht met een verhoogd risico op schijfproblemen, maar tot nu toe hadden wetenschappers de gedetailleerde eiwitsamenstelling van schijven van diabetische en niet-diabetische patiënten niet rechtstreeks vergeleken.
De eiwitvingerafdruk van tussenwervelschijven lezen
Het team verzamelde weefsel uit het midden van lumbale schijven die tijdens operaties waren verwijderd bij negen volwassenen met ernstige schijfziekte, vijf met type 2-diabetes en vier zonder. Met een techniek genaamd kwantitatieve proteomica maten ze de niveaus van bijna 3.900 verschillende eiwitten in deze monsters. Bij vergelijking van de twee groepen vonden ze dat 221 eiwitten duidelijk hoger en 233 lager waren in schijven van mensen met diabetes. Computergestuurde analyses lieten zien dat schijven van diabetische patiënten een duidelijk verschillend eiwitpatroon hadden dan die van niet-diabetische patiënten, wat bevestigt dat diabetes geassocieerd is met een andere interne omgeving in deze beschadigde kussentjes.
Hoe diabetes het energiegebruik en de structuur van de schijf verschuift
Een belangrijk verschil lag in hoe schijfcellen met energie omgaan. In diabetische schijven waren veel eiwitten verbonden aan de energiecentrales van de cel, de mitochondriën, verhoogd, en volledige routes die betrokken zijn bij het verbranden van brandstof en het produceren van energie waren actiever. Dit patroon wijst op hogere oxidatieve stress, een toestand waarin reactieve moleculen cellen en hun omgeving kunnen beschadigen. Tegelijkertijd waren eiwitten die helpen bij het opbouwen en organiseren van het ondersteunende gel- en vezelmatrix van de schijf vaak verminderd in diabetische schijven. Belangrijke structurele componenten, zoals het grote proteoglycaan versican, en verschillende moleculen in de extracellulaire ruimte, waren lager, wat suggereert dat het kussende weefsel van de schijf kwetsbaarder is in aanwezigheid van diabetes.
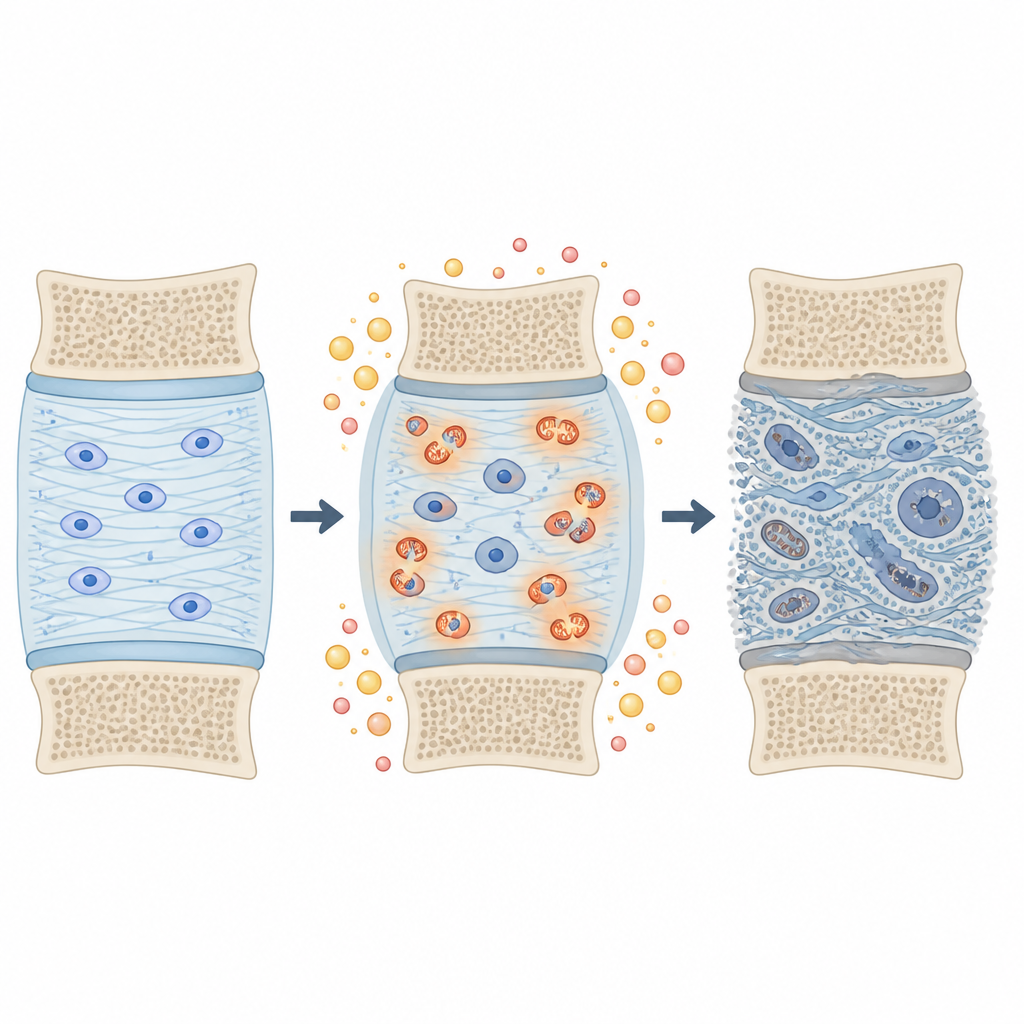
Chemische aanpassingen aan het skelet van de schijf
De onderzoekers bekeken ook een subtiele chemische wijziging genaamd prolinehydroxylatie, die vooral veel voorkomt in collageen, het belangrijkste vezelige eiwit van bindweefsel. Ze vonden meer dan tweeduizend van deze gewijzigde sites verdeeld over 230 eiwitten, waarvan veel in collageens en andere extracellulaire componenten. In diabetische schijven waren sommige van deze modificaties op collageen verhoogd, waardoor een dicht verbonden netwerk van gewijzigde eiwitten ontstond. Dit patroon komt overeen met een omgeving onder oxidatieve stress, waarin het skelet van de schijf chemisch wordt aangepast op manieren die het stijf of zwak kunnen maken en het gevoeliger voor scheuren of beschadigingen onder dagelijkse belasting.
Wat dit betekent voor patiënten en toekomstige zorg
Gezamenlijk suggereren de bevindingen dat type 2-diabetes niet simpelweg de gewone slijtage van tussenwervelschijven versnelt; het herschikt de innerlijke chemie van de schijf op specifieke manieren. Diabetische schijven tonen tekenen van overbelaste energiesystemen, hogere oxidatieve stress en diepere schade aan de kussende matrix dan schijven van niet-diabetische patiënten. Hoewel deze kleine studie geen oorzakelijk verband kan aantonen, levert zij een gedetailleerde kaart van kandidaat-eiwitten en routes die mogelijk op een dag kunnen leiden tot bloedtests, beeldvormingsmarkers of gerichte behandelingen. Voor mensen met diabetes en rugpijn benadrukt dit onderzoek dat het beheersen van metabole gezondheid een belangrijk onderdeel kan zijn van het beschermen van de wervelkolom, terwijl onderzoekers nu een scherper moleculair vertrekpunt hebben voor het ontwerpen van toekomstige therapieën.
Bronvermelding: Moinuddin, F.M., Zhong, J., Astudillo Potes, M.D. et al. Proteomic analysis identifies distinct signaling pathways in lumbar intervertebral disc degeneration between type-2 diabetic and non-diabetic patients. Sci Rep 16, 15151 (2026). https://doi.org/10.1038/s41598-026-44970-y
Trefwoorden: laag rugpijn, tussenwervelschijf, type 2 diabetes, proteomica, oxidatieve stress