Clear Sky Science · de
Proteomische Analyse identifiziert unterschiedliche Signalwege bei Lendenbandscheibendegeneration zwischen Typ-2-Diabetikern und Nicht-Diabetikern
Warum Rücken und Blutzucker zusammenhängen
Chronische Rückenschmerzen sind eine der Hauptursachen für Arbeitsausfälle, und verschlissene Bandscheiben sind häufig verantwortlich. Diese Studie stellt eine für Millionen mit Typ‑2‑Diabetes relevante Frage: Verändert Diabetes die Art und Weise, wie die weichen Polster zwischen den Wirbeln degenerieren, und wenn ja, wie? Durch das Heranzoomen an tausende von Proteinen in diesen Scheiben entdecken die Forschenden charakteristische molekulare Muster, die sich zwischen Menschen mit und ohne Diabetes unterscheiden, und liefern damit Hinweise darauf, warum Rückenprobleme bei manchen Patientinnen und Patienten früher oder stärker auftreten können.
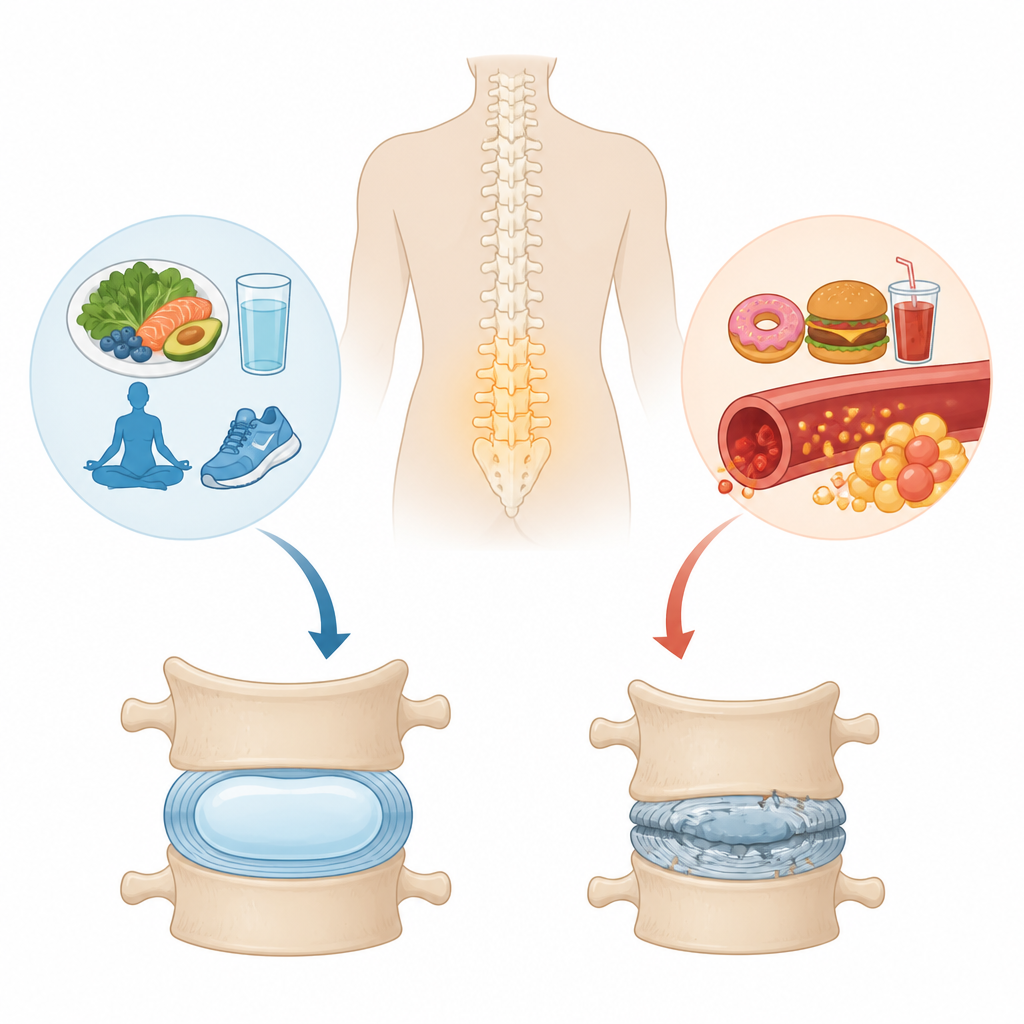
Die Polster, die uns beweglich halten
Zwischen jedem Wirbel sitzt ein kleiner, geleeartiger Polster, die Zwischenwirbelscheibe. Ihr Zentrum, der Nucleus pulposus, ist reich an wasserbindenden Proteinen und wirkt wie ein Stoßdämpfer. Mit der Zeit oder nach Verletzungen kann diese Struktur verschleißen – ein Prozess, der als Bandscheibendegeneration bezeichnet wird und eng mit chronischen Rückenschmerzen verbunden ist. Typ‑2‑Diabetes, eine chronische Erkrankung, die mit hohem Blutzucker und niedriggradiger Entzündung einhergeht, wurde in großen Bevölkerungsstudien mit einem höheren Risiko für Bandscheibenprobleme verknüpft. Bislang hatten Forschende jedoch nicht die detaillierte Protein‑Zusammensetzung von Scheiben von Diabetikern und Nicht‑Diabetikern direkt verglichen.
Den Protein‑Fingerabdruck der Wirbelscheiben lesen
Das Team sammelte Gewebe aus dem Zentrum der Lendenbandscheiben, die bei Operationen von neun Erwachsenen mit schwerer Bandscheibenerkrankung entfernt worden waren – fünf davon mit Typ‑2‑Diabetes und vier ohne. Mithilfe einer Technik namens quantitative Proteomik bestimmten sie die Mengen von fast 3.900 verschiedenen Proteinen in diesen Proben. Beim Vergleich der beiden Gruppen zeigten 221 Proteine deutlich erhöhte und 233 deutlich verringerte Werte in Scheiben von Menschen mit Diabetes. Computergestützte Analysen ergaben, dass die Proteomuster in den Scheiben von Diabetikern klar von denen Nicht‑Diabetiker unterscheiden, was bestätigt, dass Diabetes mit einem anderen inneren Milieu in diesen geschädigten Polstern einhergeht.
Wie Diabetes den Energiehaushalt und die Struktur der Scheibe verschiebt
Ein zentraler Unterschied betraf den Umgang der Zellen mit Energie. In diabetischen Scheiben waren viele Proteine, die mit den Zellkraftwerken, den Mitochondrien, assoziiert sind, erhöht, und ganze Signalwege, die am Brennstoffabbau und an der Energieproduktion beteiligt sind, zeigten eine höhere Aktivität. Dieses Muster weist auf erhöhten oxidativen Stress hin, einen Zustand, in dem reaktive Moleküle Zellen und ihre Umgebung schädigen können. Zugleich waren Proteine, die beim Aufbau und bei der Organisation des unterstützenden Gels und der Fasern der Scheibe helfen, häufig vermindert. Wichtige Strukturkomponenten, wie das große Proteoglykan Versican, sowie mehrere Moleküle der extrazellulären Matrix waren reduziert, was darauf hindeutet, dass das polsternde Gewebe der Scheibe bei Diabetes fragiler ist.
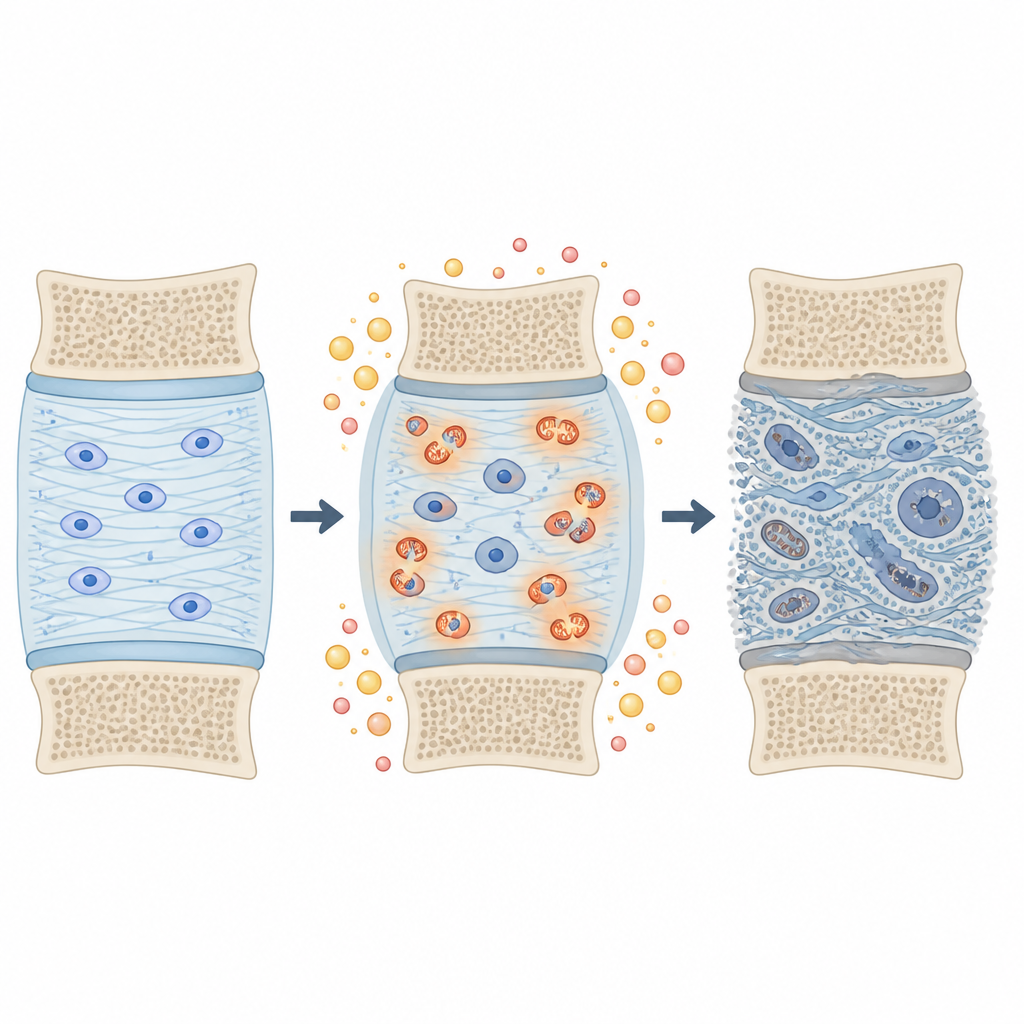
Chemische Modifikationen am Gerüst der Scheibe
Die Forschenden untersuchten außerdem eine subtile chemische Veränderung, die Prolin‑Hydroxylierung genannt wird und besonders häufig in Kollagen vorkommt, dem Hauptfaserprotein des Bindegewebes. Sie fanden mehr als zweitausend dieser modifizierten Stellen in 230 Proteinen, viele davon in Kollagenen und anderen extrazellulären Komponenten. In diabetischen Scheiben waren einige dieser Modifikationen an Kollagenen vermehrt vorhanden und bildeten ein eng verflochtenes Netzwerk veränderter Proteine. Dieses Muster passt zu einem Umfeld mit oxidativem Stress, in dem das Gerüst der Scheibe chemisch so verändert wird, dass es sich versteifen oder schwächen und dadurch anfälliger für Risse oder Einrisse unter Alltagsbelastung werden kann.
Was das für Patientinnen und Patienten und die künftige Versorgung bedeutet
In der Gesamtschau deuten die Befunde darauf hin, dass Typ‑2‑Diabetes nicht einfach nur den normalen Verschleiß der Bandscheiben beschleunigt; er verändert die innere Chemie der Scheibe auf spezifische Weise. Diabetische Scheiben zeigen Anzeichen überarbeiteter Energiesysteme, erhöhten oxidativen Stress und tiefere Schäden an der polsternden Matrix als Scheiben von Nicht‑Diabetikern. Zwar kann diese kleine Studie keine kausalen Zusammenhänge beweisen, doch liefert sie eine detaillierte Landkarte potenzieller Proteine und Signalwege, die eines Tages Bluttests, Bildgebungsmarker oder gezielte Therapien leiten könnten. Für Menschen mit Diabetes und Rückenschmerzen unterstreicht die Arbeit die Bedeutung der Kontrolle des Stoffwechsels als Teil des Schutzes der Wirbelsäule, während Forschende nun eine präzisere molekulare Ausgangsbasis für die Entwicklung künftiger Behandlungen haben.
Zitation: Moinuddin, F.M., Zhong, J., Astudillo Potes, M.D. et al. Proteomic analysis identifies distinct signaling pathways in lumbar intervertebral disc degeneration between type-2 diabetic and non-diabetic patients. Sci Rep 16, 15151 (2026). https://doi.org/10.1038/s41598-026-44970-y
Schlüsselwörter: Rückenschmerzen, Zwischenwirbelscheibe, Typ‑2‑Diabetes, Proteomik, oxidativer Stress