Clear Sky Science · nl
Albumine-op-een-chip: bindingsprofiel van circulerend humaan albumine via selectieve immunocaptatie en realtime SPR-analyse
Een piepkleine chip met grote aanwijzingen over ons bloed
Als artsen een medicijn voorschrijven, vertrouwen ze op hoe het geneesmiddel gewoonlijk in het lichaam werkt. Maar in werkelijkheid verschilt de bloedchemie per persoon, vooral bij aandoeningen zoals diabetes of leverziekte. Deze studie introduceert een kleine lab-on-a-chip die in realtime kan onderzoeken hoe het belangrijkste bloedproteïne van een individu, albumine, daadwerkelijk geneesmiddelen bindt in hun eigen bloed, wat mogelijk de weg opent naar meer op maat gemaakte en veiligere behandelingen.
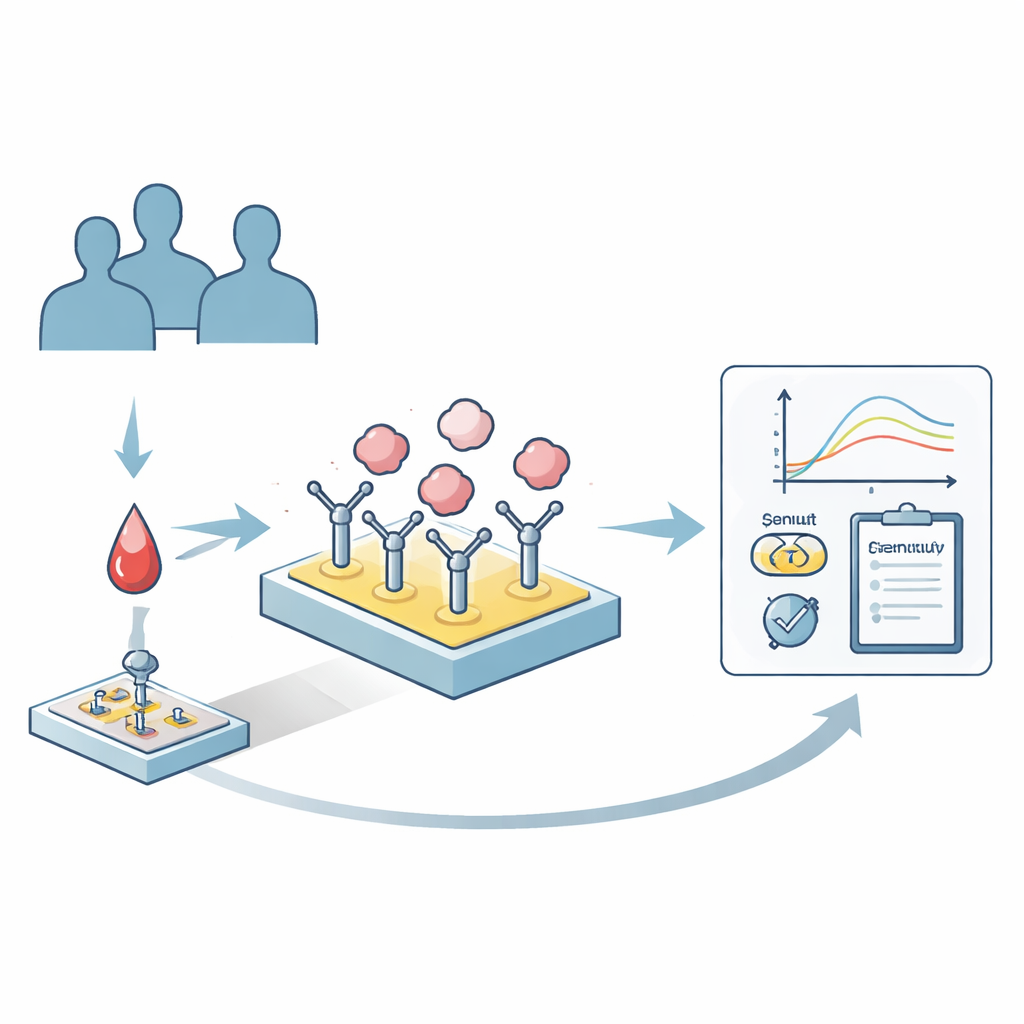
Het werkpaard-eiwit in ons bloed
Humaan serumalbumine is het meest voorkomende eiwit in onze bloedbaan. Het helpt vocht in de vaten te houden, ruimt schadelijke oxidanten op en vervoert een breed scala aan natuurlijke stoffen en geneesmiddelen. Albumine is geen uniform molecuul: bij iedereen komt het voor als een mengsel van licht verschillende vormen, gevormd door dagelijks metabolisme, veroudering, ontsteking en ziekte. Chemische wijzigingen zoals oxidatie en suikerbinding kunnen de structuur subtiel vervormen. Die veranderingen kunnen beïnvloeden hoe sterk albumine aan geneesmiddelen vasthoudt, wat op zijn beurt bepaalt hoeveel actief geneesmiddel beschikbaar is om te werken — en hoe lang het in het lichaam blijft.
Waarom traditionele tests tekortschieten
De meeste eerdere studies naar de bindingsgedrag van albumine gebruikten gezuiverd, commercieel geproduceerd eiwit dat op eenvoudige, kunstmatige manieren was aangepast. Dergelijke modellen vangen de werkelijke complexiteit van albumine in echte patiënten niet, waar veel modificaties tegelijk voorkomen en verschuiven naarmate de ziekte vordert of de behandeling verandert. Andere benaderingen die volledig plasma gebruiken, worden verstoord door vele andere eiwitten die ook geneesmiddelen binden, terwijl nauwkeurigere methoden trage en dure zuiveringsstappen vereisen. Daardoor ontbrak het wetenschappers aan een praktische manier om per patiënt te meten hoe hun eigen circulerende albumine daadwerkelijk met belangrijke medicijnen omgaat.
Albumine-op-een-chip bouwen
De onderzoekers ontwikkelden een detectieplatform gebaseerd op surface plasmon resonance (SPR), een techniek die bindingsgebeurtenissen op een chipoppervlak in realtime detecteert. Eerst coatten ze een standaard sensorchip met antilichamen die specifiek humaan albumine herkennen. Wanneer een kleine hoeveelheid patiëntplasma over de chip stroomt, wordt alleen albumine selectief op het oppervlak “gevangen”, waarbij alle natuurlijke varianten behouden blijven en andere plasmoproteïnen grotendeels worden uitgesloten. Na deze captatiestap wordt de chip blootgesteld aan kandidaat-geneesmiddelen of probenmoleculen, en registreert het systeem hoe sterk en hoe snel deze moleculen aan het geïmmobiliseerde albuminemengsel binden. Een belangrijk kenmerk is dat het albumine vervolgens weggespoeld kan worden zonder de antilichaallaag te beschadigen, zodat dezelfde chip honderden keren hergebruikt kan worden en de kosten sterk dalen.
Het apparaat testen bij echte patiënten
Om te bevestigen dat deze immunocaptatie werkelijk weerspiegelt wat er in de bloedbaan gebeurt, gebruikte het team massaspectrometrie om albuminevarianten voor en na captatie te vergelijken. Ze vonden dat de chip zowel native als gemodificeerde albuminevormen in dezelfde verhoudingen terughaalde als in het oorspronkelijke plasma, terwijl andere eiwitten achterbleven. Vervolgens pasten ze het systeem toe op twee kleine patiëntengroepen waarvan bekend of vermoed wordt dat albumine beschadigd is: mensen met gevorderde levercirrose gecompliceerd door acute-op-chronic leverfalen, en mensen met type 2-diabetes, van wie sommigen ernstige nierfunctiestoornissen hadden. In de levergroep liet de chip zien dat ondanks uitgebreide structurele schade aan albumine de belangrijkste medicijnbindende regio’s grotendeels functioneel bleven, hoewel één belangrijke site licht gewijzigd gedrag vertoonde. Opvallend was dat de binding van het antibioticum teicoplanine bij deze patiënten significant verzwakt was, wat de werkzaamheid van het middel zou kunnen beïnvloeden. In tegenstelling daarmee leek bij de diabetische niergroep, waar albumine slechts matig veranderd was, de teicoplaninebinding grotendeels onveranderd.
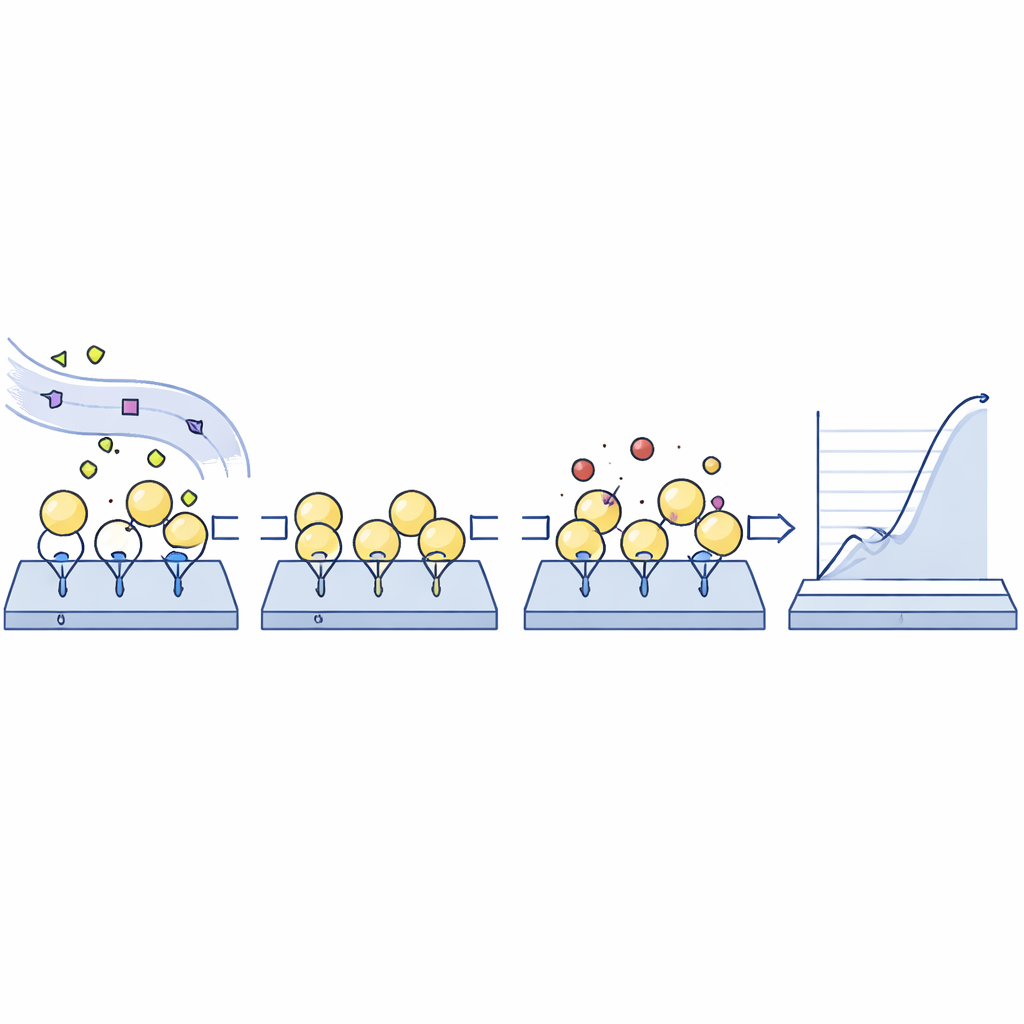
Een stap richting meer gepersonaliseerde dosering
Al met al laat de studie zien dat een herbruikbare, chipgebaseerde sensor kan vastleggen hoe het albumine van een specifieke patiënt geneesmiddelen bindt onder realistische omstandigheden, met slechts kleine plasmamonsters en zonder uitgebreide voorbereiding. Voor niet-specialisten is de kernboodschap dat dezelfde medicijndosis niet bij iedereen identiek werkt, vooral bij ernstige lever- of nierziekte, en dat technologieën zoals albumine-op-een-chip artsen kunnen helpen deze verschillen direct te meten. Op de lange termijn zou dit soort gepersonaliseerde bindingsprofielen veiliger doseren van cruciale geneesmiddelen kunnen ondersteunen en een nieuw venster kunnen bieden op hoe chronische ziekten een van de belangrijkste eiwitten in de bloedbaan hervormen.
Bronvermelding: Nugnes, M., Baldassarre, M., Caraceni, P. et al. Albumin-on-a-chip: binding profiling of circulating human albumin via selective immunocapture and real-time SPR analysis. Sci Rep 16, 10920 (2026). https://doi.org/10.1038/s41598-026-44934-2
Trefwoorden: humaan serumalbumine, medicijnbinding, leverziekte, complicaties van diabetes, biosensorchip