Clear Sky Science · fr
Albumine-sur-puce : profilage des liaisons de l’albumine humaine circulante par immunocapture sélectif et analyse SPR en temps réel
Une petite puce qui en dit long sur notre sang
Lorsque les médecins prescrivent un médicament, ils se fondent sur son comportement moyen dans l’organisme. Mais en réalité, la composition du sang varie légèrement d’une personne à l’autre, surtout en présence de maladies comme le diabète ou les affections hépatiques. Cette étude présente un petit laboratoire sur puce capable de tester, en temps réel, la manière dont la principale protéine sanguine d’un individu, l’albumine, lie effectivement les médicaments dans son propre plasma, ouvrant potentiellement la voie à des traitements plus adaptés et plus sûrs.
La protéine travailleuse de notre sang
L’albumine sérique humaine est la protéine la plus abondante dans notre circulation. Elle aide à maintenir les liquides dans les vaisseaux, neutralise des oxydants nuisibles et transporte une vaste gamme de substances naturelles et de médicaments. L’albumine n’est pas une molécule unique et uniforme : chez chaque individu elle existe comme un mélange de versions légèrement différentes, façonnées par le métabolisme quotidien, le vieillissement, l’inflammation et la maladie. Des modifications chimiques telles que l’oxydation ou la fixation de sucres peuvent altérer subtilement sa structure. Ces changements peuvent modifier l’affinité de l’albumine pour les médicaments, ce qui influe à son tour sur la quantité de principe actif disponible et sur la durée d’action dans l’organisme.
Pourquoi les tests traditionnels sont insuffisants
La plupart des études antérieures sur le comportement de liaison de l’albumine se sont appuyées sur une protéine purifiée, produite commercialement et modifiée de façon simple et artificielle. De tels modèles ne rendent pas compte de la complexité réelle de l’albumine chez des patients, où de nombreuses altérations coexistent et évoluent avec la progression de la maladie ou la modification des traitements. D’autres approches utilisant le plasma entier sont perturbées par de nombreuses protéines qui lient aussi les médicaments, tandis que des méthodes plus précises nécessitent des étapes de purification lentes et coûteuses. En conséquence, les scientifiques manquaient d’un moyen pratique pour mesurer, pour chaque patient, comment son albumine circulante interagit réellement avec des médicaments importants.
Concevoir l’albumine-sur-puce
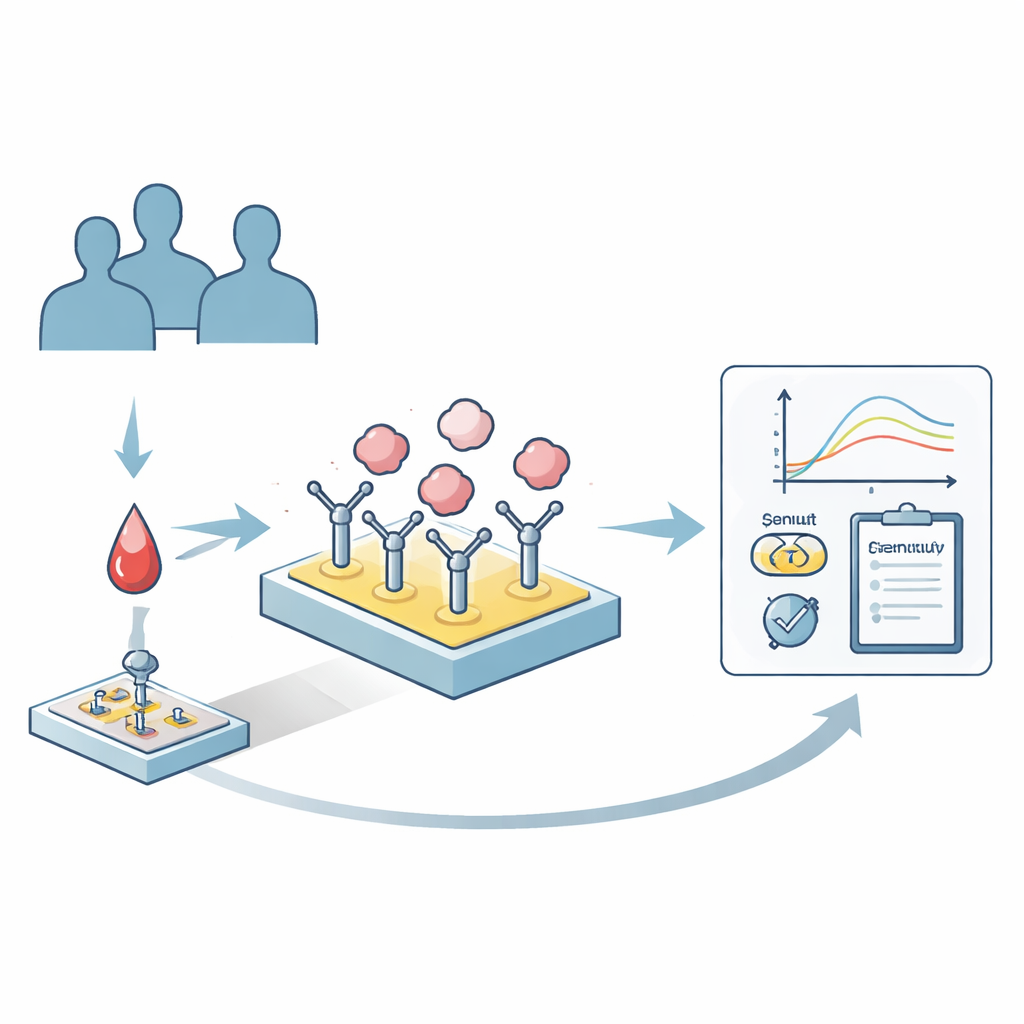
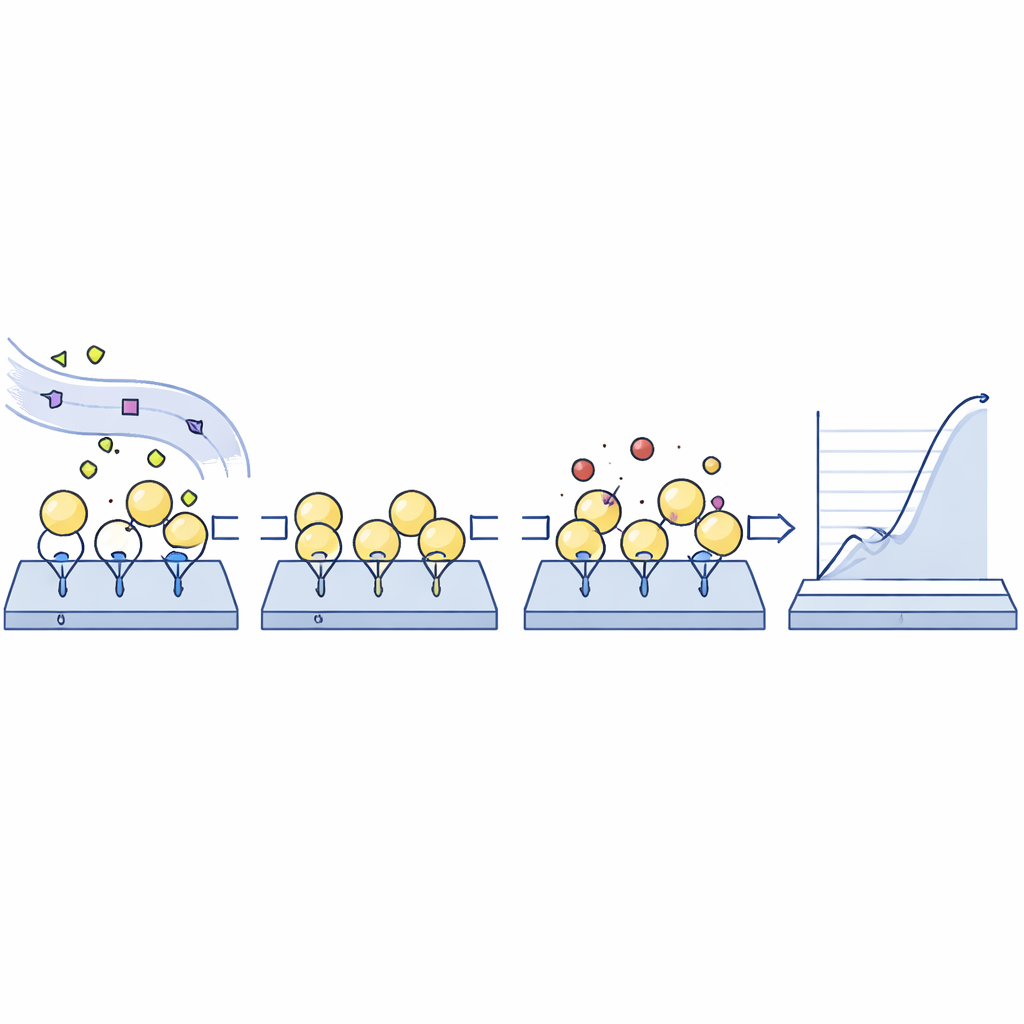
Les chercheurs ont développé une plateforme de détection basée sur la résonance plasmonique de surface (SPR), une technique qui détecte en temps réel les événements de liaison à la surface d’une puce. D’abord, ils ont enrobé une puce capteur standard d’anticorps reconnaissant spécifiquement l’albumine humaine. Lorsqu’une petite quantité de plasma patient circule sur la puce, seule l’albumine est sélectivement « capturée » à la surface, avec toutes ses variantes naturelles préservées et les autres protéines plasmatiques en grande partie exclues. Après cette étape d’immunocapture, la puce est exposée à des médicaments candidats ou à des molécules sonde, et le système enregistre la force et la cinétique de leur liaison au mélange d’albumine immobilisée. Une caractéristique clé est que l’albumine peut ensuite être éliminée sans endommager la couche d’anticorps, de sorte que la même puce peut être réutilisée des centaines de fois, réduisant ainsi considérablement les coûts.
Mettre l’appareil à l’épreuve chez de vrais patients
Pour confirmer que cette immunocapture reflète bien ce qui se passe dans la circulation, l’équipe a utilisé la spectrométrie de masse pour comparer les variantes d’albumine avant et après capture. Ils ont constaté que la puce récupérait les formes natives et modifiées de l’albumine dans les mêmes proportions que dans le plasma initial, tout en laissant les autres protéines en arrière-plan. Ils ont ensuite appliqué le système à deux petits groupes de patients où l’altération de l’albumine est connue ou suspectée : des personnes atteintes d’une cirrhose hépatique avancée compliquée d’une insuffisance hépatique aiguë sur chronique, et des personnes avec un diabète de type 2, dont certaines présentaient une insuffisance rénale grave. Dans le groupe hépatique, la puce a révélé que, malgré des dommages structurels étendus à l’albumine, les principaux sites de liaison aux médicaments restaient pour la plupart fonctionnels, bien qu’un site clé montre un comportement légèrement modifié. De manière notable, la liaison de l’antibiotique téicoplanine était significativement affaiblie chez ces patients, ce qui pourrait affecter l’efficacité du médicament. En revanche, dans le groupe diabétique avec atteinte rénale, où l’albumine était seulement modérément altérée, la liaison à la téicoplanine semblait globalement inchangée.
Une étape vers un dosage plus personnalisé des médicaments
Globalement, l’étude montre qu’un capteur réutilisable sur puce peut profiler la façon dont l’albumine d’un patient particulier lie les médicaments dans des conditions réalistes, en n’utilisant que de petits échantillons de plasma et sans préparation élaborée. Pour le lecteur non spécialiste, le message clé est que la même dose de médicament peut ne pas se comporter de façon identique chez tout le monde, en particulier en cas de maladies hépatiques ou rénales graves, et que des technologies comme l’albumine-sur-puce pourraient aider les médecins à mesurer ces différences directement. À plus long terme, ce type de profil de liaison personnalisé pourrait soutenir un ajustement plus sûr des doses de médicaments critiques et offrir une nouvelle fenêtre sur la manière dont les maladies chroniques remodèlent l’une des protéines les plus importantes du sang.
Citation: Nugnes, M., Baldassarre, M., Caraceni, P. et al. Albumin-on-a-chip: binding profiling of circulating human albumin via selective immunocapture and real-time SPR analysis. Sci Rep 16, 10920 (2026). https://doi.org/10.1038/s41598-026-44934-2
Mots-clés: albumine sérique humaine, liaison aux médicaments, maladie du foie, complications du diabète, puce biosenseur