Clear Sky Science · nl
Progressieve cognitieve achteruitgang en ventriculaire tachycardie bij een jongen met biallele POLG-varianten en een de novo RYR2-verandering
Wanneer twee genetische foutjes samenkomen
De meesten van ons denken bij een ziekte aan één enkele oorzaak, maar artsen ontdekken dat sommige patiënten ziek zijn door meer dan één verborgen fout in hun DNA. Dit artikel vertelt het verhaal van een jongen wiens verslechterende leerproblemen en plotselinge, dodelijke hartritmestoornis uiteindelijk terug te voeren waren op twee afzonderlijke genetische defecten — één die de kleine energiecentrales in cellen aantastte en de ander die het elektrische ritme van het hart verstoorde. Zijn geval laat zien hoe moderne genetische hulpmiddelen en slimme laboratoriummodellen, waaronder gistcellen, zulke medische mysteries kunnen ontwarren en de diagnose voor toekomstige patiënten kunnen verbeteren.
Een raadselachtig verhaal van hersenen en hart
De jongen in dit verslag ontwikkelde zich aanvankelijk normaal, afgezien van vertraagde spraak. Op vijfjarige leeftijd lagen zijn denkvaardigheden nog in het gemiddelde, maar in de daaropvolgende jaren ging zijn schoolprestaties sterk achteruit en op negenjarige leeftijd voldeed hij aan de criteria voor een verstandelijke beperking. Hersenscans en vroege hartonderzoeken waren onopvallend en standaard genetische testen gaven geen verklaring. Toen, op twaalfjarige leeftijd, kreeg hij flauwvallen die verbonden waren met abnormale snelle ritmes in de bovenste kamers van zijn hart. Ondanks medicatie verslechterde zijn hartfunctie en overleed hij op dertienjarige leeftijd plotseling aan een hartstilstand. De combinatie van progressieve cognitieve problemen en gevaarlijke hartritmestoornissen leidde tot een diepere zoektocht in zijn DNA.
Twee afzonderlijke genetische daders gevonden
Met next-generation sequencing, dat honderden genen tegelijk kan doorzoeken, vond het team eerst drie veranderingen in een gen genaamd POLG. Dit gen codeert voor een essentieel onderdeel van het enzym dat mitochondriaal DNA kopieert — de kleine ring van genetisch materiaal in de energiecentrales van de cel. Twee van de veranderingen vormden een bekende schadelijke combinatie op het chromosoom van de vader, eerder gekoppeld aan mitochondriale ziekte. De derde verandering, aangeduid als W113R, kwam van de moeder en was nog nooit eerder gezien, waardoor de medische betekenis onduidelijk was. Later bracht een gerichtere heranalyse van de exoomgegevens van de jongen een aanvullende verandering in een ander gen aan het licht, RYR2, dat helpt bij het regelen van calciumstroom in hartspiercellen. Deze RYR2-variant, Y4725C, was beschreven bij andere patiënten met levensbedreigende snelle hartritmes en was niet aanwezig bij een van beide ouders, wat betekent dat hij nieuw in de jongen was ontstaan.
Gist gebruiken om een nieuwe mutatie te testen
Om te bepalen of de onbekende POLG-variant werkelijk het enzym schaadde, wendden de onderzoekers zich tot een onverwachte bondgenoot: bakkersgist. Gistcellen hebben hun eigen versie van dezelfde mitochondriale DNA-polymerase, Mip1 genoemd. Omdat het betrokken aminozuur tussen soorten geconserveerd is, kopieerde het team de menselijke W113R-verandering naar het overeenkomstige positie in het gistgen. Ze vergeleken gist met normale Mip1 met gist die de gewijzigde versie droeg. Bij normale temperatuur kon de mutant-gist ademen en groeien, maar er waren meer cellen die hun mitochondriale DNA hadden verloren of beschadigd. Bij warmte-stress werden deze problemen dramatisch: bijna alle cellen met het gemuteerde enzym konden niet meer respireren en hun mitochondriale DNA-hoeveelheid daalde sterk. Het gemuteerde enzym veroorzaakte ook iets meer kopieerfouten, hoewel het eiwitniveau zelf niet verlaagd was. Samen tonen deze resultaten aan dat de W113R-verandering het behoud van mitochondriaal DNA belemmert, vooral onder stress.
De puzzel in elkaar zetten
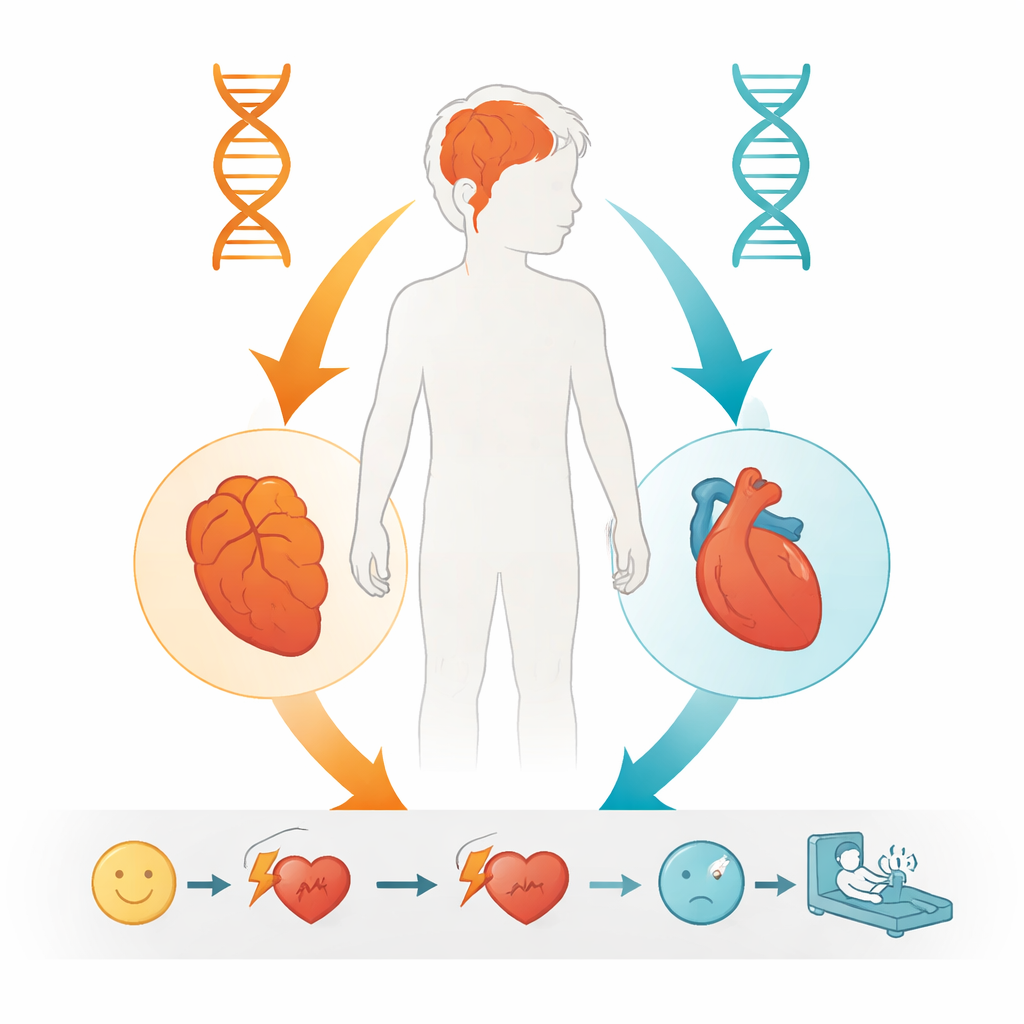
Gezien deze bevindingen concludeerden de auteurs dat de verslechterende cognitieve problemen van de jongen het beste verklaard werden door zijn "dubbele treffer" in POLG: één bekende schadelijke allel van zijn vader en het nieuw aangetoonde schadelijke W113R-allel van zijn moeder. Dit sluit aan bij andere patiënten met twee defecte POLG-kopieën die progressieve neurologische klachten krijgen die in de kinder- of adolescentieperiode beginnen. De hartritmestoornis daarentegen kwam sterk overeen met wat is waargenomen bij personen met de Y4725C-variant in RYR2, een gen dat bekend staat om het veroorzaken van gevaarlijke ventriculaire tachycardie. Hoewel de auteurs een mogelijk samenspel tussen de mitochondriale en hartkanaaldefecten niet volledig kunnen uitsluiten, is het meest duidelijke beeld dat twee grotendeels onafhankelijke genetische problemen het verstand en het hart van de jongen parallel hebben aangetast.
Waarom dit geval belangrijk is
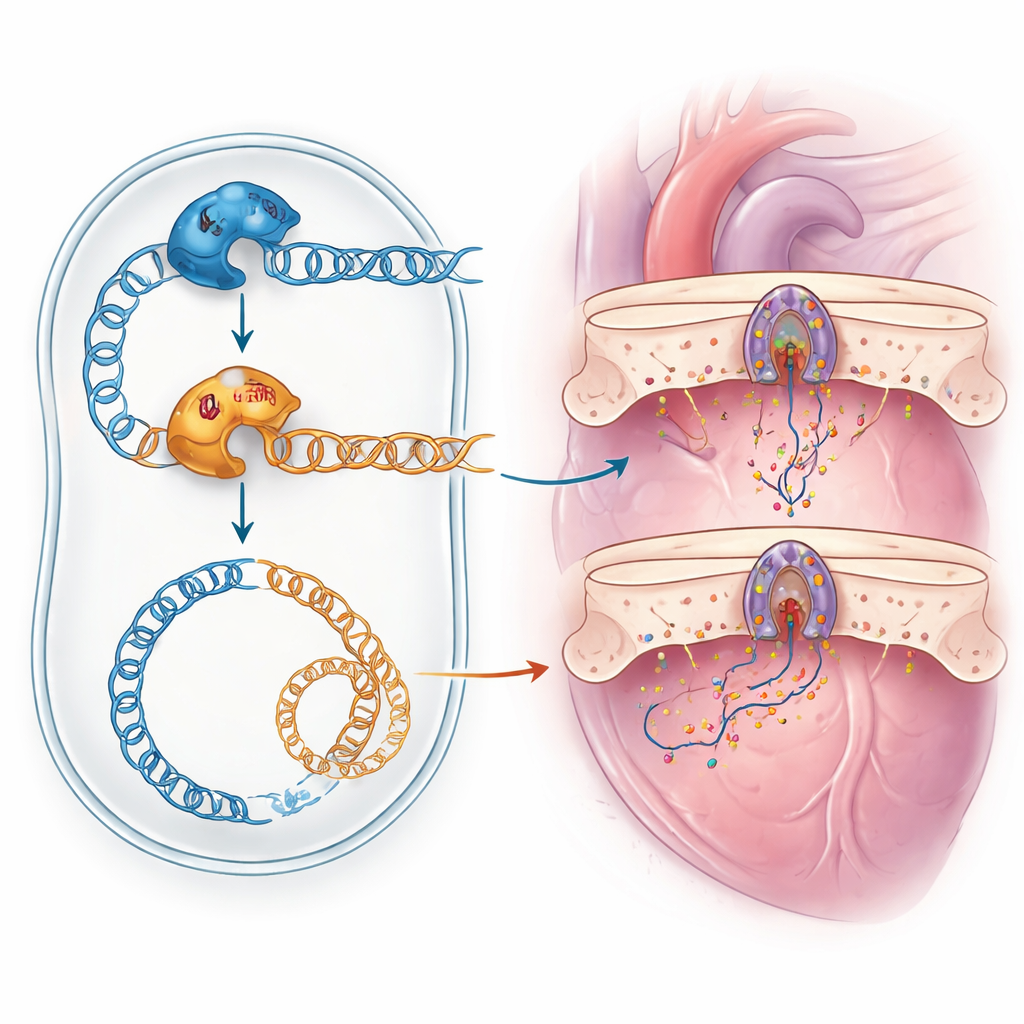
Dit geval benadrukt meerdere lessen voor de moderne geneeskunde. Ten eerste zijn de complexe symptomen van sommige patiënten niet te wijten aan één zeldzame ziekte maar aan "dubbel probleem" door meer dan één genetisch defect, wat gemakkelijk over het hoofd gezien kan worden zonder zorgvuldige heranalyse van sequencinggegevens. Ten tweede kunnen computermodellen alleen niet betrouwbaar beoordelen of een nieuw ontdekte DNA-verandering schadelijk is; functionele tests, zoals het modelleren van de mutatie in gist, kunnen doorslaggevend bewijs leveren. Ten slotte is verduidelijken welk gen welke symptomen veroorzaakt van cruciaal belang voor nauwkeurige voorlichting van families en het koppelen van patiënten aan opkomende behandelingen, zoals experimentele geneesmiddelen die gericht zijn op het herstellen van POLG-gerelateerde mitochondriale defecten. Voor families en clinicians die geconfronteerd worden met onverklaarde multisysteemziekten toont deze studie aan hoe brede genetische testen gecombineerd met slimme laboratoriummodellen uiteindelijk antwoorden kunnen opleveren.
Bronvermelding: Fumini, V., Gilea, A.I., Tacchetto, E. et al. Progressive cognitive impairment and ventricular tachycardia in a boy with biallelic POLG variants and a de novo RYR2 variation. Sci Rep 16, 14289 (2026). https://doi.org/10.1038/s41598-026-44913-7
Trefwoorden: mitochondriale ziekte, genetische aritmie, POLG-mutatie, RYR2-kanaalopathie, gist functionele test