Clear Sky Science · nl
Een contrastief leerraamwerk met adaptieve kenmerkfusie voor classificatie van hersentumoren
Waarom slimmer lezen van hersenscans ertoe doet
Hersentumoren zijn gevaarlijk, niet alleen omdat ze vitaal weefsel binnendringen, maar ook omdat ze op medische scans moeilijk van elkaar te onderscheiden kunnen zijn. Artsen vertrouwen sterk op MRI-beelden om te bepalen hoe ernstig een tumor is en welke behandeling passend is. Toch kunnen tumoren die zich in het lichaam heel verschillend gedragen, op het scherm verrassend gelijk lijken. Deze studie presenteert een nieuwe computermethode die leert subtiele verschillen in MRI-beelden te herkennen, met als doel artsen te ondersteunen bij snellere en betrouwbaardere tumorklassificatie.
De uitdaging binnen de schedel zichtbaar maken
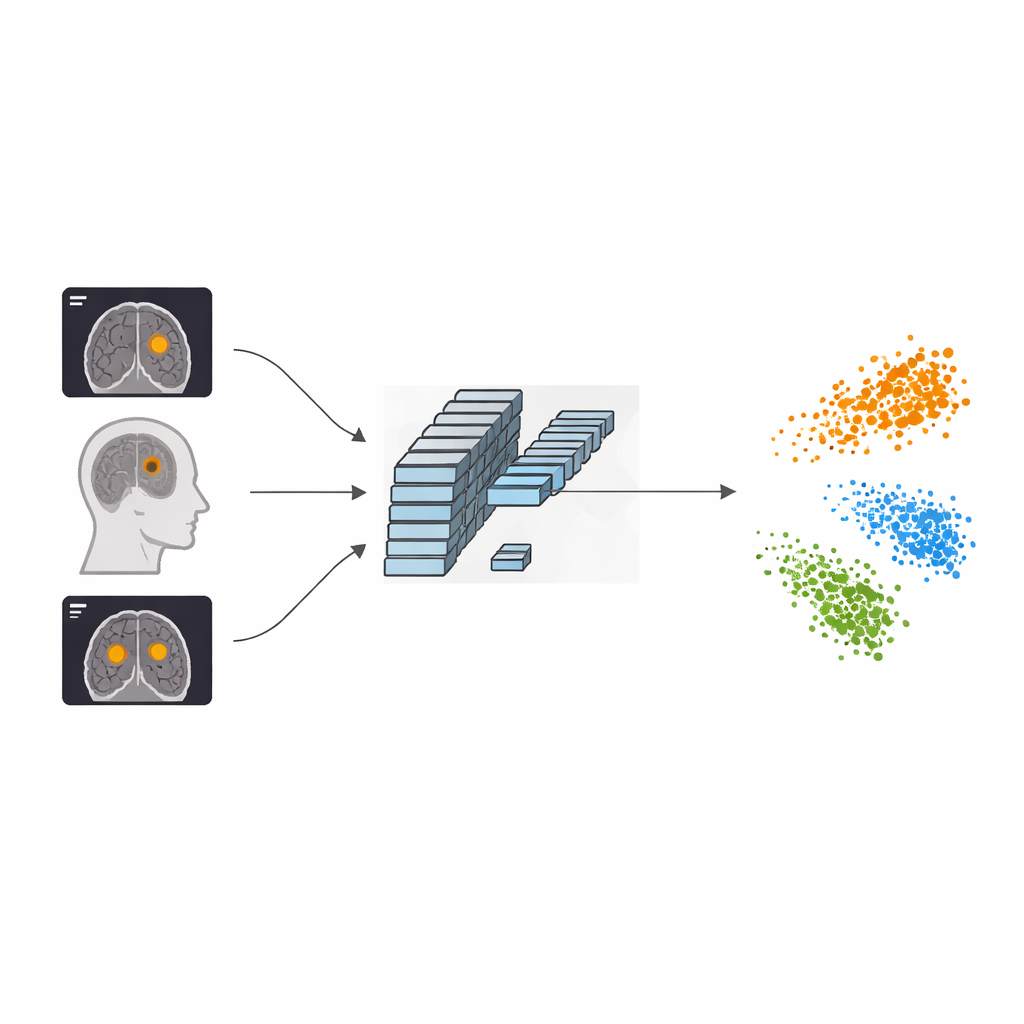
Hersentumoren ontstaan wanneer cellen binnen de schedel ongecontroleerd gaan groeien, waarbij ze op nabijgelegen gebieden drukken en symptomen zoals hoofdpijn, aanvallen of gezichtsproblemen veroorzaken. Op MRI-scans overlappen drie veelvoorkomende tumortypen—meningeoom, glioom en hypofysetumor—vaak in uiterlijk. Om het nog lastiger te maken, maken ziekenhuizen opnames vanuit meerdere richtingen (axiaal, coronair, sagittaal), waardoor dezelfde tumor van de ene slice tot de andere heel verschillend kan lijken. Bestaande deep-learningsystemen herkennen brede patronen in deze beelden, maar missen vaak de zeer fijne details in vorm, begrenzing en textuur die het ene tumortype van het andere onderscheiden.
Een nieuwe manier om computers te leren waar op te letten
De auteurs stellen een raamwerk voor genaamd AFF-CL dat de manier verandert waarop een neuraal netwerk leert van MRI-scans. In plaats van alleen te leren een beeld aan zijn label te koppelen (bijvoorbeeld “glioom”), leert het systeem ook door beelden met elkaar te contrasteren. Het bouwt een soort geheugenwachtrij op die kenmerkvingerafdrukken van vele eerdere beelden opslaat, samen met hun tumortypen. Wanneer een nieuwe scan binnenkomt, vergelijkt het model zijn interne vingerafdruk niet slechts met één partnerbeeld, maar met veel opgeslagen voorbeelden van hetzelfde tumortype en van andere typen. Kenmerken uit dezelfde categorie worden dichter bij elkaar getrokken, terwijl die van verschillende categorieën uit elkaar worden geduwd, waardoor de computer scherpere grenzen kan creëren tussen tumorklassen in zijn interne “kaart” van beelden.
De hersenen zowel in het overzicht als ingezoomd bekijken
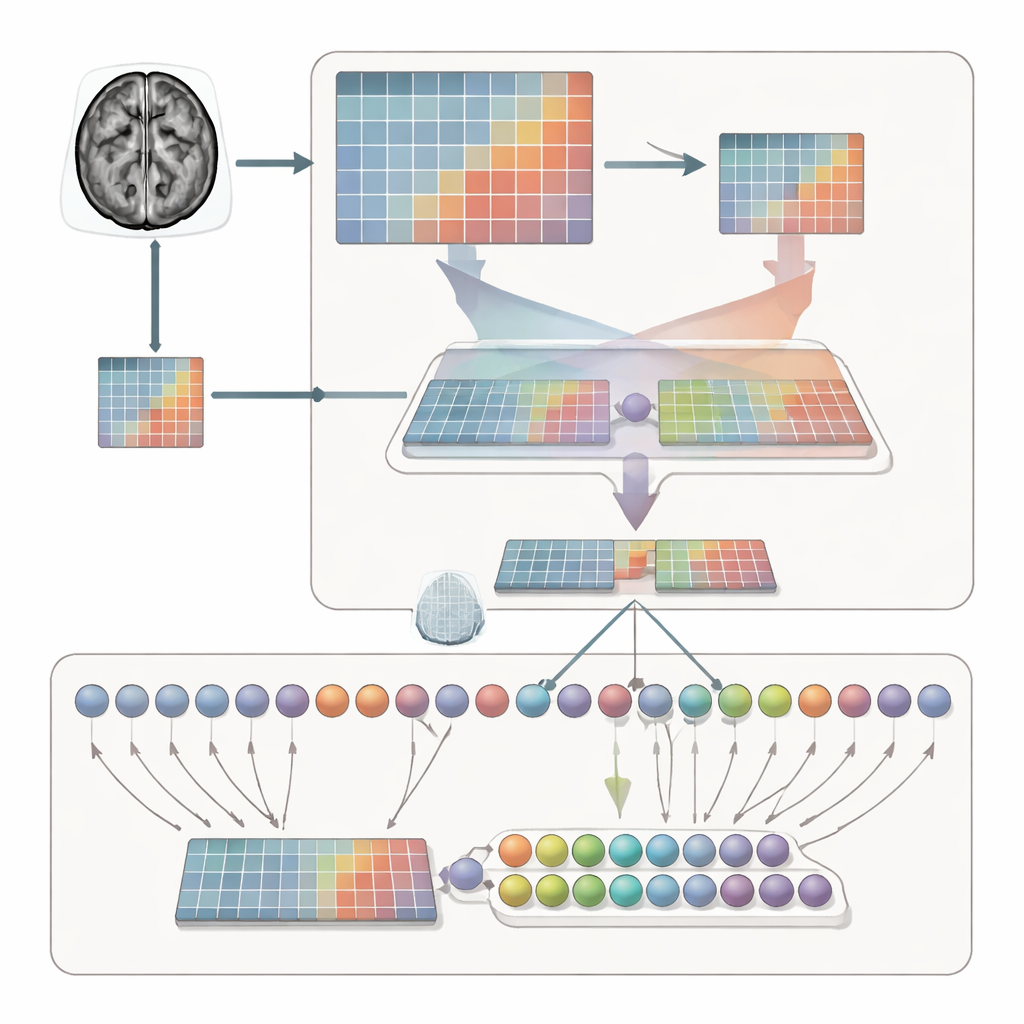
Slechts categorieën scheiden is niet genoeg; het systeem moet ook leren waar binnen elke MRI-slice te kijken. Om dit te bereiken verwerkt het raamwerk elke scan op twee complementaire manieren. De ene tak ziet het hele brein en legt zo de algemene context, grootte en locatie van de tumor vast. De andere tak zoomt in op een bijgesneden regio, waardoor het model gedwongen wordt lokale structuur, randen en texturen te inspecteren. Een adaptieve kenmerkfusie (AFF)-module fungeert vervolgens als een slimme menger die per punt beslist hoeveel vertrouwen te geven aan het brede beeld versus de close-up. Met een ingebouwd attentiemechanisme versterkt het signalen waar lokaal detail cruciaal is en ondersteunt het deze met de bredere anatomische context, wat een rijkere gecombineerde representatie voor de uiteindelijke classificatie oplevert.
De methode op de proef gesteld
De onderzoekers evalueerden AFF-CL op een veelgebruikte openbare dataset van 3.064 hersen-MRI-beelden van 233 patiënten. De dataset bevat de drie belangrijkste tumortypen en beelden die vanuit meerdere gezichtspunten zijn genomen. Na training behaalde de nieuwe methode ongeveer 99,35% nauwkeurigheid, waarmee ze vele recente deep-learningbenaderingen overtrof die vertrouwen op diepere netwerken of conventionele attentie alleen. De auteurs toonden ook aan dat hun aanpak de prestaties verbetert over verschillende backbone-architecturen, van lichtgewicht convolutionele netwerken geschikt voor kleinere klinieken tot geavanceerdere transformermodellen. Visualisaties van de interne activiteit van het netwerk geven aan dat met AFF-CL de aandacht scherper op de daadwerkelijke tumorregio’s concentreert en de drie tumortypen in de kenmerkruimte in goed gedefinieerde clusters worden gescheiden.
Wat dit betekent voor patiënten en klinieken
Voor niet-specialisten is de kernboodschap dat AFF-CL computers helpt hersentumoren in MRI-scans met uitzonderlijke precisie te herkennen door beelden slimmer te vergelijken en “uitgezoomde” en “ingezoomde” beelden van het brein te combineren. Hoewel de methode momenteel meer rekencapaciteit vereist om te trainen en strengere patiëntniveautests nog nodig heeft, overtreft ze al bestaande tools op twee verschillende datasets. Op de lange termijn zouden dergelijke systemen als een tweede paar ogen voor radiologen kunnen dienen, waardoor gemiste diagnoses verminderen, behandelbeslissingen versnellen en geavanceerde analyse van hersentumoren toegankelijker wordt in een breder scala aan ziekenhuizen.
Bronvermelding: Peng, Y., He, S. & Chang, L. A contrastive learning framework with adaptive feature fusion for brain tumor classification. Sci Rep 16, 14504 (2026). https://doi.org/10.1038/s41598-026-44887-6
Trefwoorden: hersentumor MRI, deep learning diagnose, medische beeldanalyse, contrastief leren, kenmerkfusie