Clear Sky Science · nl
Verandering in speekselimmuunrespons blijft bestaan na behandeling van cariës
Waarom je speeksel meer over gaatjes vertelt dan je denkt
Tandartsen beoordelen meestal je risico op nieuwe gaatjes aan de hand van je tanden. Deze studie suggereert dat ze ook naar je speeksel zouden moeten kijken. Door honderden kleine verdedigingsproteïnen in speeksel te volgen vóór en na tandheelkundige behandeling, vonden de onderzoekers dat, zelfs wanneer beschadigde tanden zijn hersteld, het immuunsysteem van de mond niet volledig terugkeert naar een toestand zoals bij iemand die nooit cariës heeft gehad. Die aanhoudende verandering kan helpen verklaren waarom sommige mensen steeds weer nieuwe gaatjes krijgen en kan op den duur leiden tot meer gepersonaliseerde preventie.
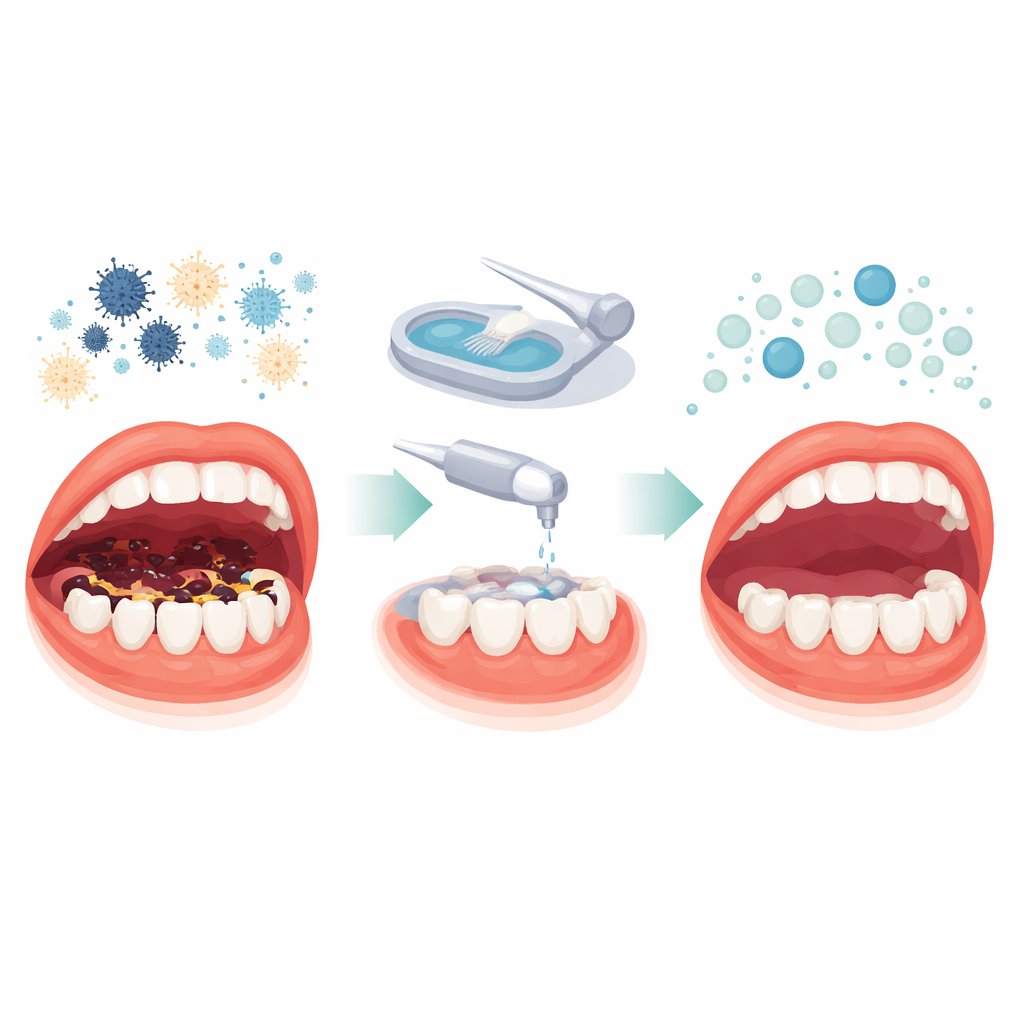
Tandbederf als een verhaal van het hele lichaam in de mond
Tandbederf gaat niet alleen over suiker en ‘slechte bacteriën’. Het is een langdurig getouwtrek tussen microben, dieet en de afweer van het lichaam zelf. Speeksel speelt een centrale rol in deze strijd. Het spoelt voedsel weg, neutraliseert zuren en bevat eiwitten die microben doden of temmen en helpen het glazuur te herstellen. Wanneer de productie of kwaliteit van speeksel afneemt, komen gaatjes vaker voor. Toch weten wetenschappers verrassend weinig over hoe het immuunaspect van speeksel zich gedraagt bij volwassenen met cariës, en wat er met dit interne verdedigingssysteem gebeurt nadat de tandarts heeft schoongemaakt, gesoldeerd en gevuld.
Patiënten en hun speeksel volgen tijdens de behandeling
De onderzoekers volgden 46 gezonde volwassenen, sommige met uitgebreide cariës en sommige met relatief gezonde tanden. Over ongeveer drie maanden kreeg iedereen grondige reiniging, fluorideapplicaties en advies over poetsen en voeding. Alleen de groep met cariës kreeg vullingen voor hun beschadigde tanden. Op drie sleutelpunten—voor de behandeling, na de niet-invasieve zorg en na de vullingen—verzamelde het team zowel rustspeeksel als speeksel gestimuleerd door kauwen. In plaats van slechts een paar stoffen te testen, gebruikten ze geavanceerde massaspectrometrie om meer dan tweeduizend menselijke eiwitten tegelijk te meten en te zien welke ervan verschilden tussen mensen met en zonder cariës. Ze bepaalden ook het bacteriële profiel in geheel speeksel met een andere massaspectrometrie-aanpak.
De afweer in speeksel kalmeert maar vergeet niet helemaal
Bij aanvang toonden mensen met cariës een sterk verstoord patroon van immuunactiviteit in hun speeksel. Bijna 200 eiwitten waren op hogere of lagere niveaus aanwezig dan bij mensen zonder bederf, veel daarvan betrokken bij frontlinieverdediging zoals de aangeboren immuniteit, het complementsysteem en het vrijkomen van antimicrobiële inhoud uit witte bloedcellen. Na reiniging, fluoride en uiteindelijk vullingen nam deze storm geleidelijk af: veel minder eiwitten bleven afwijkend en volledige immuunroutes die aanvankelijk overactief waren, leken veel meer op die in de gezonde groep. Toch bleef één belangrijk pad, gekoppeld aan het vrijkomen van stoffen uit neutrofielen—kortlevende witte bloedcellen die de mond patrouilleren—actief, hoewel de samenstelling van de betrokken eiwitten in de loop van de tijd veranderde. Dit patroon suggereert dat de mond is verschoven van een sterk ontstoken toestand naar een meer gecontroleerde ‘waakzame’ modus in plaats van volledige rust.
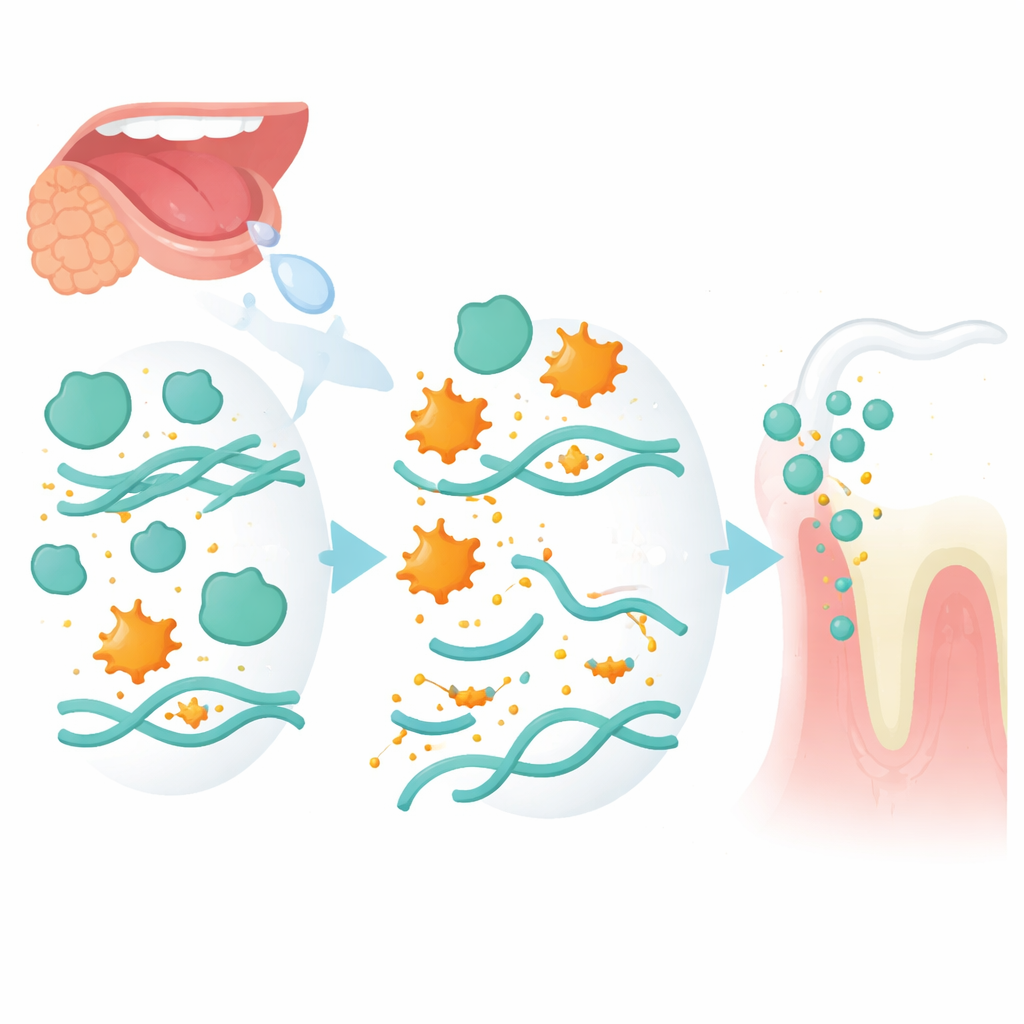
Een blijvend moleculair spoor van eerdere cariës
Zelfs na behandeling bleef een kleine groep eiwitten consistent veranderd bij mensen met een geschiedenis van cariës. Twee sprongen eruit: een beschermende remmer genaamd SLPI en een speekselmucine genaamd MUC7, beide op lagere niveaus in de cariësgroep bij elk tijdstip. SLPI remt normaal krachtige enzymen die door neutrofielen worden vrijgegeven en die weefselcomponenten kunnen afbreken, terwijl MUC7 helpt een gladde barrière op tanden te vormen en de hechting van bacteriën bemoeilijkt. De auteurs stellen dat wanneer SLPI verminderd is, deze enzymen gemakkelijker mucines zoals MUC7 kunnen beschadigen, waardoor de beschermende laag dunner wordt en het voor cariësveroorzakende bacteriën eenvoudiger wordt zich te vestigen. Gezamenlijk lijken deze twee moleculen een regulerend ‘as’-mechanisme te vormen dat bepaalt hoe goed speeksel zowel ontsteking onder controle houdt als microben in toom houdt. Opmerkelijk is dat, terwijl deze gastheerverdedigingen verschoven, de algemene bacteriële diversiteit in speeksel verrassend stabiel bleef, wat benadrukt dat veranderingen in de reactie van het lichaam mogelijk meer zeggen dan brede verschuivingen in welke soorten aanwezig zijn.
Wat dit betekent voor toekomstige tandzorg
De studie suggereert dat het herstellen van zichtbare gaatjes in tanden de interne afweer van de mond niet volledig terugzet naar een werkelijk gezonde basislijn. In plaats daarvan kunnen mensen die ernstige cariës hebben gehad een blijende moleculaire vingerafdruk in hun speeksel dragen—een mengeling van aanhoudende immuunactiviteit en verzwakte beschermende lagen—die hen vatbaarder kan maken voor toekomstige problemen, zelfs wanneer hun vullingen er perfect uitzien. Als dit wordt bevestigd in grotere, op individuen gerichte studies, zou het meten van eiwitten zoals SLPI en MUC7 in speeksel een eenvoudige manier kunnen worden om degenen met verhoogd risico te identificeren en extra preventie op maat aan te bieden, zoals vaker controles of gerichte therapieën, voordat nieuwe gaatjes ontstaan.
Bronvermelding: Huerta-García, E.X., Camargo-Ayala, P.A., Dias, N.B. et al. Salivary immune alteration persists after caries treatment. Sci Rep 16, 13963 (2026). https://doi.org/10.1038/s41598-026-43748-6
Trefwoorden: speeksel, tandbederf, speekseleiwitten, orale immuniteit, massaspectrometrie