Clear Sky Science · nl
miR-320a verhoogt radiosensitiviteit bij niet-kleincellig longkanker door RAD51 te richten en ferroptose te moduleren via GPX4
Waarom het verbeteren van bestraling telt
Radiotherapie is een van de belangrijkste behandelingen voor niet-kleincellig longkanker, de meest voorkomende vorm van longkanker. Toch leren veel tumoren na verloop van tijd te overleven ondanks bestraling, waardoor het moeilijker wordt de ziekte onder controle te houden. Deze studie onderzoekt een klein genetisch regelaarstapeltje, miR-320a, en laat zien hoe het de balans kan verschuiven tussen overleving en celdood na bestraling. Door een keten van moleculaire gebeurtenissen in longkankercellen te volgen, identificeren de onderzoekers een potentiële kwetsbaarheid die gebruikt zou kunnen worden om radiotherapie effectiever en beter op de individuele patiënt af te stemmen.
Een klein molecuul met veel invloed op behandelingsreactie
Het team begon met het vergelijken van tumormonsters van mensen met niet-kleincellig longkanker met naburig niet-kankerachtig longweefsel en met normale luchtwegcellen gekweekt in het laboratorium. Ze vonden dat de niveaus van miR-320a consequent lager waren in tumoren. Patiënten van wie de tumoren minder van dit molecuul hadden, deden het doorgaans slechter na radiotherapie, wat suggereert dat miR-320a als een ingebouwde hulp voor bestraling kan fungeren. In celkweekexperimenten maakte het blokkeren van miR-320a kankercellen beter in het overleven en migreren na bestraling, terwijl het verhogen van miR-320a ze kwetsbaarder maakte en trager liet herstellen. Samen wezen deze patronen op miR-320a als een natuurlijke versterker van radiosensitiviteit—de mate waarin bestraling kankercellen kan doden.
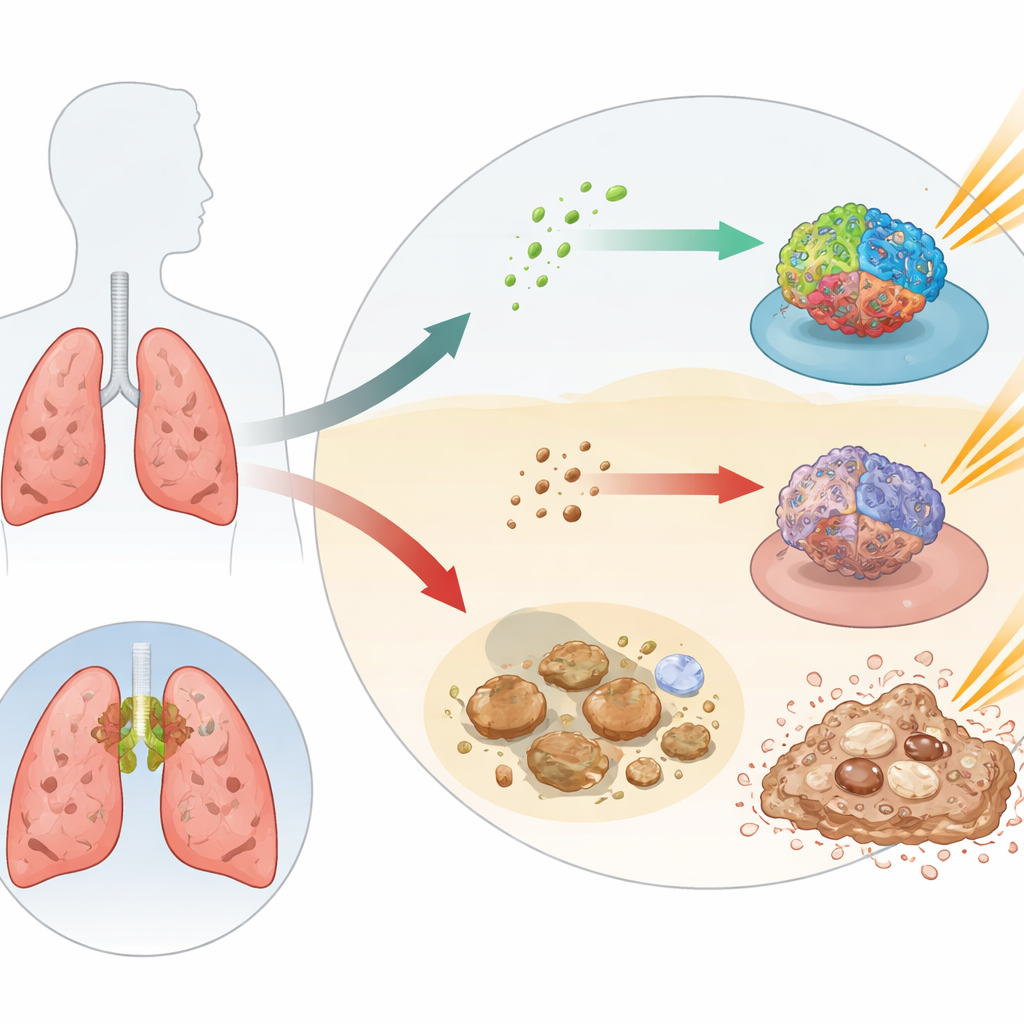
Het uitschakelen van de DNA-reparatieploeg van kanker
Om te begrijpen hoe miR-320a deze invloed uitoefent, zochten de onderzoekers naar zijn moleculaire doelen—eiwitten waarvan de productie het naar beneden kan bijstellen. Computationele tools wezen herhaaldelijk op RAD51, een sleutelspeler bij het repareren van gebroken DNA-strengen na bestraling. In patiëntgegevens en in longkankercellijnen gingen hogere miR-320a-niveaus gepaard met lagere hoeveelheden RAD51. Wanneer de wetenschappers miR-320a kunstmatig verminderden, steeg RAD51; wanneer ze miR-320a verhoogden, daalden de RAD51-eiwitniveaus. Een gespecialiseerde reporter-test bevestigde dat miR-320a kan binden aan het genetische bericht voor RAD51 en de vertaling naar eiwit kan blokkeren. Functioneel maakte het omlaag brengen van RAD51 cellen gevoeliger voor bestraling, terwijl hoge RAD51-niveaus samenhingen met slechtere overleving bij patiënten en grotere resistentie in het laboratorium.
Van DNA-reparatie naar een speciale vorm van celdood
Het werk stopte niet bij DNA-reparatie. De auteurs onderzochten vervolgens ferroptose, een recent beschreven vorm van celdood die wordt aangedreven door ijzer en de ophoping van beschadigde vetten in celmembranen. Ze concentreerden zich op GPX4, een beschermend enzym dat cellen tegen dit type schade afschermt. Wanneer de RAD51-activiteit in longkankercellen werd geblokkeerd, daalden de GPX4-niveaus; wanneer RAD51 werd verhoogd, steeg GPX4, vooral bij een matige bestralingsdosis. Dit toonde aan dat de DNA-reparatiefactor meer doet dan genetische breuken herstellen—hij helpt ook de verdediging van de cel tegen ferroptose in stand te houden. Onder bestraling overleefden cellen met meer GPX4 beter, terwijl het verlagen van GPX4 ze kwetsbaarder maakte. Op deze manier lijkt RAD51 radioresistentie deels te bevorderen door ferroptotische celdood in toom te houden.
Een driedelig pad dat de balans doet doorslaan
Ten slotte koppelden de onderzoekers de punten tussen miR-320a, RAD51 en GPX4. Wanneer miR-320a werd geremd, daalden lipide-gebaseerde reactieve zuurstofsoorten—een kenmerk van ferroptose—en stegen GPX4-niveaus, wat wijst op verminderde ferroptotische dood en grotere radioresistentie. Gelijktijdig het stilleggen van RAD51 keerde deze effecten om: GPX4 daalde, lipideschade nam toe en de cellen werden weer gevoeliger voor bestraling. Analyses van menselijke longtumordatasets ondersteunden deze keten, waarbij miR-320a negatieve verbanden liet zien met zowel RAD51 als GPX4. Al met al schetst de studie een regulatoir as waarin miR-320a RAD51 dempt, RAD51 GPX4 ondersteunt, en GPX4 cellen tegen ferroptose beschermt, wat gezamenlijk bepaalt hoe longtumoren reageren op radiotherapie.
Wat dit kan betekenen voor mensen met longkanker
Voor patiënten suggereren deze bevindingen dat een klein RNA-molecuul en twee downstream-eiwitten meebeslissen of bestraling een longkankercel doodt of het herstel en verspreiding toestaat. Hoog miR-320a, laag RAD51 en geremde GPX4-activiteit begunstigen het succes van bestraling door meer membraanschade en ferroptotische celdood toe te staan; de tegenovergestelde combinatie helpt tumoren resistent te worden tegen behandeling. Hoewel dit werk voornamelijk in gekweekte cellen is uitgevoerd en nog bevestigd moet worden in diermodellen en grotere patiëntengroepen, wijst het op meerdere praktische mogelijkheden: het gebruik van miR-320a- of RAD51-niveaus om te voorspellen wie het meest van radiotherapie zal profiteren, en uiteindelijk het ontwerpen van geneesmiddelen die miR-320a versterken of het RAD51–GPX4-signaal remmen om standaardbestraling effectiever te maken zonder noodzakelijkerwijs de dosis te verhogen.
Bronvermelding: Lv, J., Zhang, C., Ren, X. et al. miR-320a enhances radiosensitivity in non-small cell lung cancer by targeting RAD51 and modulating ferroptosis via GPX4. Sci Rep 16, 11397 (2026). https://doi.org/10.1038/s41598-026-41692-z
Trefwoorden: niet-kleincellig longkanker, radiotherapie-resistentie, microRNA-320a, DNA-reparatie RAD51, ferroptose GPX4