Clear Sky Science · ar
miR-320a يعزز الحساسية للإشعاع في سرطان الرئة غير صغير الخلايا عبر استهداف RAD51 وتعديل الفيروبتوز عبر GPX4
لماذا تحسين فاعلية الإشعاع أمر مهم
العلاج الإشعاعي هو أحد العلاجات الرئيسية لسرطان الرئة غير صغير الخلايا، وهو أكثر أشكال سرطان الرئة شيوعًا. ومع ذلك، تتعلم العديد من الأورام مع مرور الوقت كيفية الصمود أمام الإشعاع، مما يصعّب السيطرة على المرض. تستكشف هذه الدراسة منظمًا جينيًا صغيرًا يُدعى miR-320a وتوضح كيف يمكنه أن يغيّر التوازن بين نجاة خلية السرطان وموتها بعد التعرض للإشعاع. من خلال تتبع سلسلة من الأحداث الجزيئية داخل خلايا سرطان الرئة، يحدد الباحثون نقطة ضعف محتملة يمكن استغلالها لجعل العلاج الإشعاعي أكثر فعالية ومصممًا بدقة أكبر لكل مريض.
جزيء صغير له أثر كبير على استجابة العلاج
بدأ الفريق بالمقارنة بين عينات الأورام من مرضى سرطان الرئة غير صغير الخلايا والأنسجة الرئوية المجاورة غير السرطانية، بالإضافة إلى خلايا مجاري الهواء الطبيعية التي نمت في المختبر. وجدوا أن مستويات miR-320a كانت أقل باستمرار في الأورام. ويميل المرضى الذين تحتوي أورامهم على مستويات منخفضة من هذا الجزيء إلى نتائج أسوأ بعد العلاج الإشعاعي، ما يشير إلى أن miR-320a قد يعمل كمساعد مدمج للعلاج بالإشعاع. في تجارب زراعة الخلايا، أدى حجب miR-320a إلى جعل خلايا السرطان أكثر قدرة على البقاء والحركة بعد التعرض للإشعاع، بينما جعل تعزيز miR-320a هذه الخلايا أكثر عرضة للتلف وأبطأ في التعافي. مجتمعة، أشارت هذه الأنماط إلى أن miR-320a يعمل كمُعزّز طبيعي للحساسية للإشعاع — أي سهولة قتل الإشعاع لخلايا السرطان.
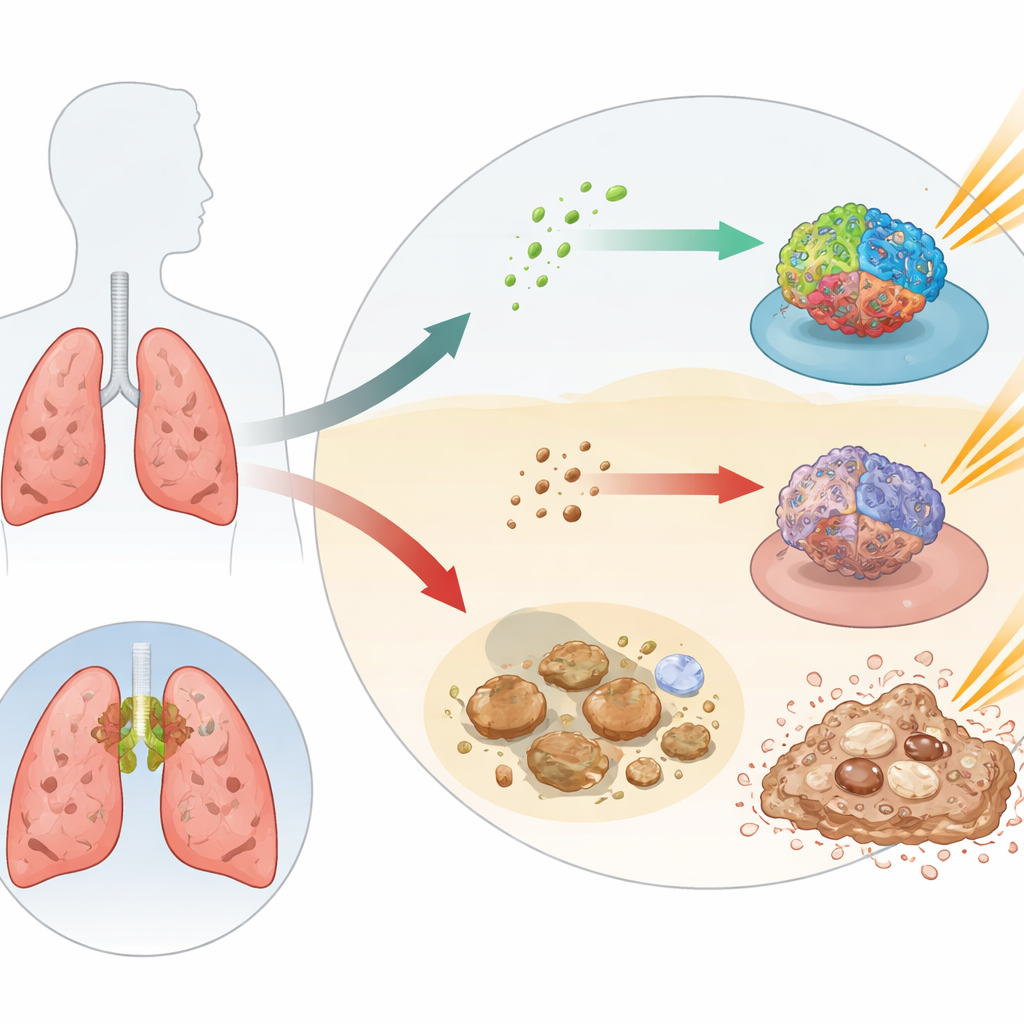
إبطال طاقم إصلاح الحمض النووي لدى السرطان
لفهم كيفية تأثير miR-320a، بحث الباحثون عن أهدافه الجزيئية — البروتينات التي يمكنه تقليل إنتاجها. أشارت الأدوات الحاسوبية مرارًا إلى RAD51، وهو عنصر أساسي في إصلاح شقوق الحمض النووي الناتجة عن الإشعاع. في بيانات المرضى وخطوط خلايا سرطان الرئة، ارتبطت مستويات أعلى من miR-320a بكميات أقل من RAD51. عندما خفّض العلماء miR-320a اصطناعيًا، ارتفعت مستويات RAD51؛ وعندما زادوا miR-320a، انخفضت مستويات بروتين RAD51. وأكد اختبار مراسل متخصص أن miR-320a يمكنه الالتحام برسالة RAD51 الجينية ومنع ترجمتها إلى بروتين. وظيفيًا، جعل خفض RAD51 الخلايا أكثر عرضة للإشعاع، بينما ارتبطت مستويات RAD51 العالية ببقاء أسوأ لدى المرضى ومقاومة أكبر في المختبر.
من إصلاح الحمض النووي إلى شكل خاص من الموت الخلوي
لم يتوقف العمل عند إصلاح الحمض النووي. فحص المؤلفون بعد ذلك الفِيروبتوز، وهو شكل من أشكال الموت الخلوي وُصف مؤخرًا ويعتمد على الحديد وتراكم الدهون المتأذية في أغشية الخلايا. ركزوا على GPX4، إنزيم وقائي يحمي الخلايا من هذا النوع من التلف. عندما تم تعطيل نشاط RAD51 في خلايا سرطان الرئة، انخفضت مستويات GPX4؛ وعندما زاد RAD51، ارتفعت مستويات GPX4، لا سيما تحت جرعة إشعاع معتدلة. أظهر ذلك أن عامل إصلاح الحمض النووي يقوم بأكثر من مجرد إصلاح الشروخ الجينية — فهو أيضًا يساعد في المحافظة على دفاعات الخلية ضد الفِيروبتوز. تحت الإشعاع، نجت الخلايا ذات مستويات GPX4 الأعلى بشكل أفضل، بينما جعل خفض GPX4 الخلايا أكثر هشاشة. بهذه الطريقة، يبدو أن RAD51 يعزز المقاومة للإشعاع جزئيًا من خلال كبح موت الخلايا الفِيروبتوزي.
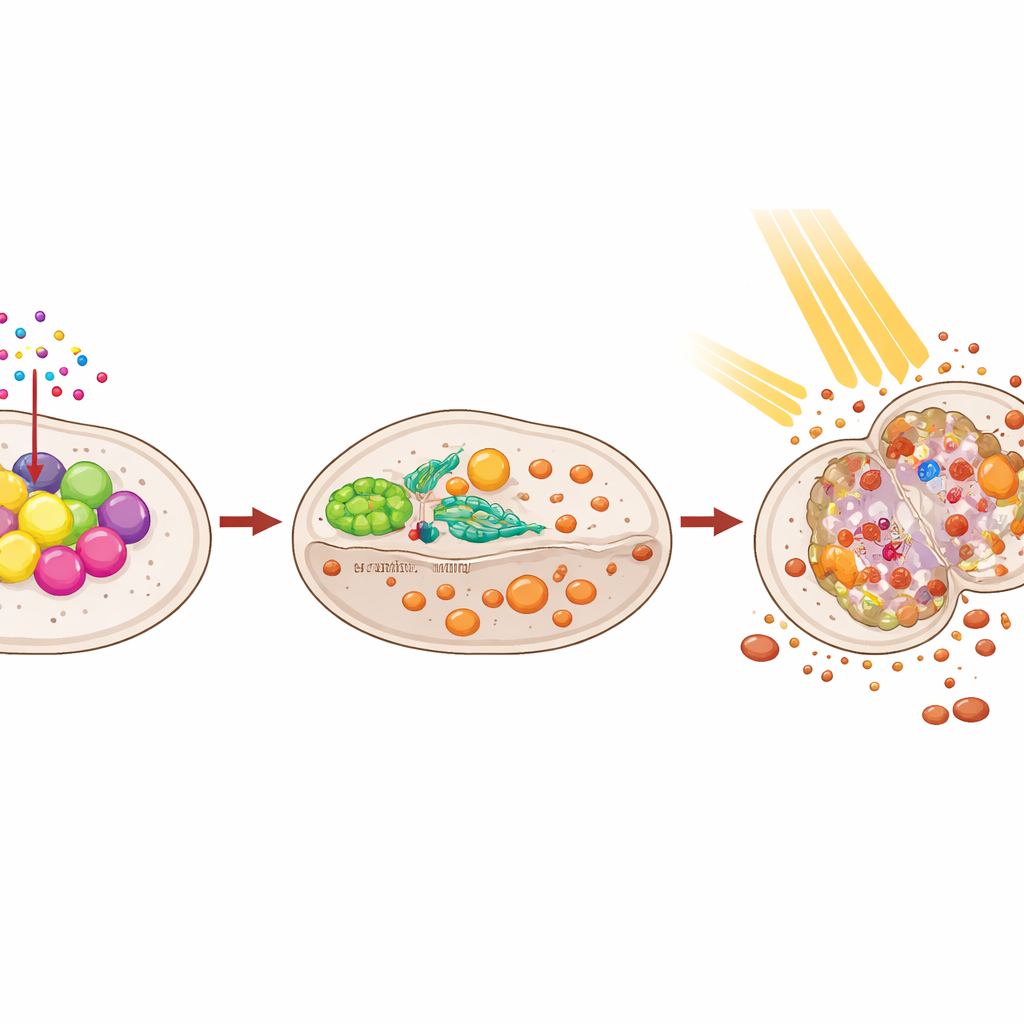
مسار ثلاثي المراحل يميّل الميزان
أخيرًا، ربط الباحثون النقاط بين miR-320a وRAD51 وGPX4. عندما تم تثبيط miR-320a، انخفضت أنواع الأكسجين التفاعلية القائمة على الدهون — وهي علامة مميزة للفِيروبتوز — وارتفعت مستويات GPX4، مما يدل على انخفاض الموت الفِيروبتوزي وزيادة المقاومة للإشعاع. وأدى إسكات RAD51 في الوقت نفسه إلى عكس هذه التأثيرات: هبطت مستويات GPX4، ازداد تلف الدهون، وأصبحت الخلايا مرة أخرى أكثر حساسية للإشعاع. دعمت تحليلات مجموعات بيانات أورام الرئة البشرية هذه السلسلة، حيث أظهر miR-320a روابط سلبية مع كل من RAD51 وGPX4. مجتمعة، تحدد الدراسة محورًا تنظيميًا حيث يخفّض miR-320a من RAD51، يدعم RAD51 مستوى GPX4، ويحمي GPX4 الخلايا من الفِيروبتوز، مما يشكل طريقة استجابة أورام الرئة للعلاج الإشعاعي.
ما الذي قد يعنيه هذا لمرضى سرطان الرئة
بالنسبة للمرضى، تشير هذه النتائج إلى أن جزيئًا رنينيًا صغيرًا وبروتينين تابعين لهما دور في تحديد ما إذا كان الإشعاع سيقضي على خلية سرطان الرئة أو يسمح لها بالتعافي والانتشار. مستويات عالية من miR-320a، ومستويات منخفضة من RAD51، ونشاط منخفض لـ GPX4 تفضّل نجاح الإشعاع عن طريق السماح بمزيد من تلف الأغشية وموت فِيروبتوزي؛ في حين أن المزيج المعاكس يساعد الأورام على مقاومة العلاج. وعلى الرغم من أن هذا العمل أُجري بشكل أساسي في خلايا مزروعة ويتطلّب تأكيدًا في نماذج حيوانية ومجموعات مرضى أكبر، فإنه يشير إلى عدة إمكانات عملية: استخدام مستويات miR-320a أو RAD51 للتنبؤ بمن سيستفيد أكثر من العلاج الإشعاعي، وتصميم أدوية في المستقبل تعزز miR-320a أو تثبط محور RAD51–GPX4 لجعل الإشعاع القياسي أكثر فعالية دون زيادة الجرعة بالضرورة.
الاستشهاد: Lv, J., Zhang, C., Ren, X. et al. miR-320a enhances radiosensitivity in non-small cell lung cancer by targeting RAD51 and modulating ferroptosis via GPX4. Sci Rep 16, 11397 (2026). https://doi.org/10.1038/s41598-026-41692-z
الكلمات المفتاحية: سرطان الرئة غير صغير الخلايا, مقاومة العلاج الإشعاعي, الميكروRNA-320a, إصلاح الحمض النووي RAD51, الفِيروبتوز GPX4