Clear Sky Science · nl
Een gezamenlijke CNN-Bi-LSTM-transformerarchitectuur met SHAP-verklaringen voor multi-label ritmestoornisdetectie uit 12‑lead ECG's
Waarom het scannen van hartritme iedereen raakt
Hartritmestoornissen, of aritmieën, zijn een belangrijke oorzaak van plotselinge hartdood, maar de belangrijkste test om ze te detecteren — het 12‑lead elektrocardiogram (ECG) — berust nog steeds grotendeels op tijdgebonden menselijke experts. Deze studie introduceert een kunstmatig-intelligentiesysteem dat standaard-ECG's tegelijk op veel verschillende ritmestoornissen kan doorzoeken, uitlegt wat het vond in termen die artsen begrijpen, en snel genoeg werkt om in draagbare apparaten of telemedicine-platforms te passen. Voor patiënten kan dat eerder waarschuwen voor gevaarlijke ritmes betekenen; voor clinici belooft het een onvermoeibare assistent die niet alleen problemen markeert, maar ook toont waarom.
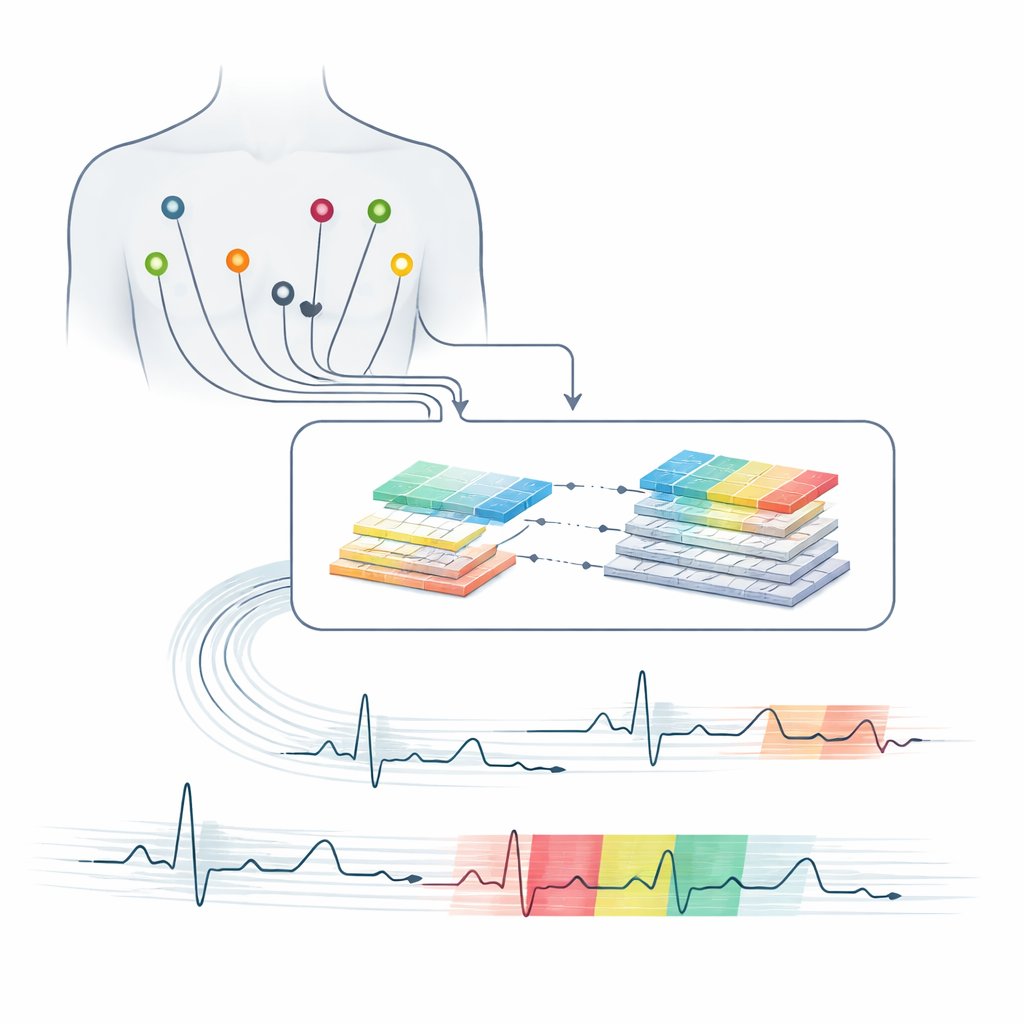
Het hart beluisteren met veel oren
Een 12‑lead ECG legt de elektrische activiteit van het hart vast vanuit meerdere gezichtspunten met elektroden op de borst en ledematen. Elke hartslag produceert een karakteristiek golfpatroon dat onthult hoe signalen door de hartkamers reizen. Kleine vervormingen in deze patronen kunnen wijzen op aandoeningen variërend van onschuldige variaties tot levensbedreigende verstoringen. Het interpreteren van deze subtiele veranderingen over veel leads en lange opnames is veeleisend, en menselijke interpretaties kunnen per expert verschillen. Tegelijkertijd steunt moderne zorg steeds meer op continue monitoring in ziekenhuizen, thuis en in wearables, wat meer gegevens oplevert dan clinici realistisch handmatig kunnen beoordelen.
Een digitale assistent leren complexe hartsignalen te lezen
De onderzoekers bouwden een deep-learningmodel dat ruwe 12‑lead ECG-segmenten als invoer neemt en leert 27 klinisch belangrijke ritme- en geleidingsproblemen te herkennen. Eerst verwerkten ze meer dan 43.000 deskundig gelabelde opnames uit de grote PhysioNet/Computing in Cardiology 2020-collectie. Signalensets van verschillende ziekenhuizen gebruikten verschillende bemonsteringsfrequenties en bevatten ruis, ontbrekende waarden en incidentele uitbijters. Het team bracht alle ECG's naar een gemeenschappelijke samplingrate, verwijderde basislijnslope en elektrische interferentie, vulde gaten op met statistisch verantwoorde regels en segmenteerde de gegevens in overlappende vensters van vier seconden. Deze vensterlengte bleek lang genoeg om belangrijke ritmepatronen vast te leggen en tegelijk kort en efficiënt te zijn voor realtime-analyse.
Hoe het gelaagde model ruimte, tijd en context ziet
De kern van het systeem is een keten van drie complementaire neurale netwerkmodule. Convolutionele lagen fungeren als patroondetectoren en scannen elke ECG-lead op vormen zoals scherpe pieken, verbrede complexes of vervormde segmenten. Vervolgens volgen bidirectionele long short‑term memory-lagen hoe deze kenmerken zich in de tijd ontwikkelen, waarbij het ritme effectief zowel vooruit als achteruit wordt gevolgd om onregelmatige intervallen en overgangen tussen slagen te vangen. Ten slotte past een transformerblok een attention-mechanisme toe dat zich op tegelijk verre maar gerelateerde signaalfragmenten over alle leads kan richten, verbindingen leggen die op overlappende aandoeningen kunnen wijzen. Samen zetten deze lagen elk kort ECG-venster om in een compacte representatie waarvan het netwerk de aanwezigheid van elk van de 27 aritmie- en geleidingscategorieën in een multi-label manier schat.
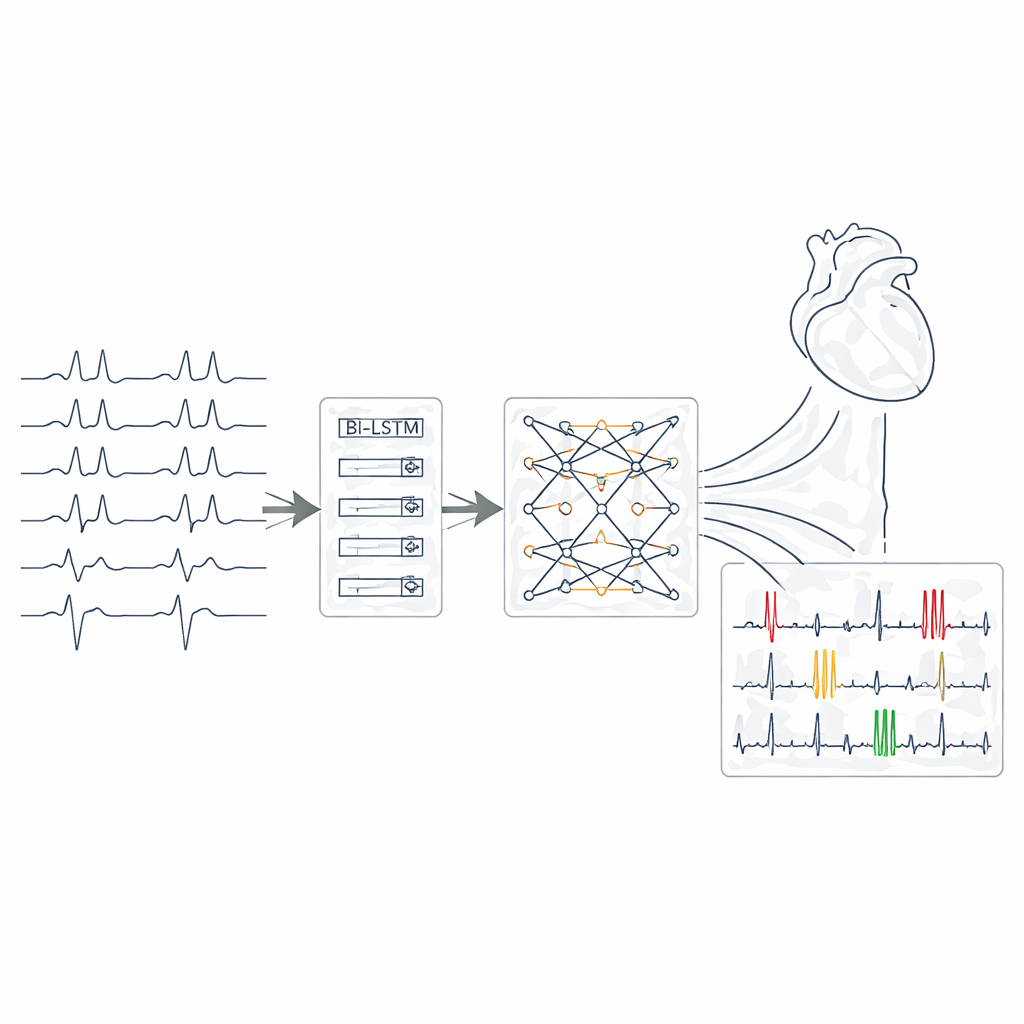
De zwarte doos openen met betekenisvolle markeringen
Om de beslissingen van het systeem inzichtelijk te maken, integreerden de auteurs een techniek genaamd SHAP, die berekent hoeveel elk deel van het ECG aan een bepaalde voorspelling heeft bijgedragen. Na het trainen gebruikten ze SHAP om visuele "belangkaarten" te genereren die specifieke golfsegmenten en leads benadrukken waarop het model in elk geval was afgestemd. Deze kaarten kwamen vaak overeen met standaard cardiologische redenering: bijvoorbeeld, het systeem benadrukte afwezige P‑golven en onregelmatige slagintervallen bij het identificeren van atriumfibrilleren, of verbrede QRS-complexen en compenserende pauzes bij het herkennen van premature ventrikelcomplexen. Deze overeenkomst suggereert dat de AI niet louter patronen uit het hoofd leert, maar zich richt op dezelfde fysiologische aanwijzingen die menselijke experts gebruiken.
Prestaties in de praktijk en toekomstige belofte
Op een onafhankelijke testgroep van patiënten classificeerde het model ritmes correct met een totale nauwkeurigheid van ongeveer 91% en behield het een sterke balans tussen het opsporen van echte problemen en het vermijden van valse alarmen, zowel voor veelvoorkomende als zeldzame aandoeningen. Voor gevaarlijke aritmieën zoals premature ventrikelcomplexen en atriumfibrilleren was het onderscheid tussen abnormaal en normaal uitzonderlijk hoog. Opmerkelijk is dat het volledige model minder dan twee megabyte geheugen inneemt en een ECG-venster in minder dan tien milliseconden kan analyseren, waardoor het geschikt is voor inzet in bedmonitoren, ambulante recorders of zelfs slimme wearables. Eenvoudig gezegd laat dit werk zien dat een compact, uitlegbaar AI-systeem kan helpen bij het lezen van standaard ECG's voor een breed scala aan hartritmestoornissen, clinicians duidelijke visuele rechtvaardigingen biedt en de weg vrijmaakt voor veiliger, beter toegankelijke hartbewaking.
Bronvermelding: Al-Bairmani, M.T., Yazdchi, M. & Nasimi, F. A joint CNN-Bi-LSTM-transformer architecture with SHAP explanations for multi-label arrhythmia detection from 12-lead ECGs. Sci Rep 16, 11123 (2026). https://doi.org/10.1038/s41598-026-40925-5
Trefwoorden: elektrocardiogram, hartritmestoornis, deep learning, uitlegbare AI, cardiale bewaking