Clear Sky Science · it
Un’architettura congiunta CNN‑Bi‑LSTM‑transformer con spiegazioni SHAP per la rilevazione multi‑etichetta delle aritmie da ECG a 12 derivazioni
Perché la scansione del ritmo cardiaco riguarda tutti
I problemi del ritmo cardiaco, o aritmie, sono una delle principali cause di morte cardiaca improvvisa, eppure il test principale usato per individuarle — l’elettrocardiogramma (ECG) a 12 derivazioni — dipende ancora fortemente da esperti umani sotto pressione di tempo. Questo studio introduce un sistema di intelligenza artificiale in grado di analizzare gli ECG standard per numerosi problemi di ritmo contemporaneamente, spiegare quanto rilevato in termini comprensibili ai medici e funzionare abbastanza velocemente da poter essere integrato in dispositivi indossabili o piattaforme di telemedicina. Per i pazienti, ciò potrebbe significare un avvertimento precoce di ritmi pericolosi; per i clinici, promette un assistente instancabile che non solo segnala anomalie ma mostra anche il perché.
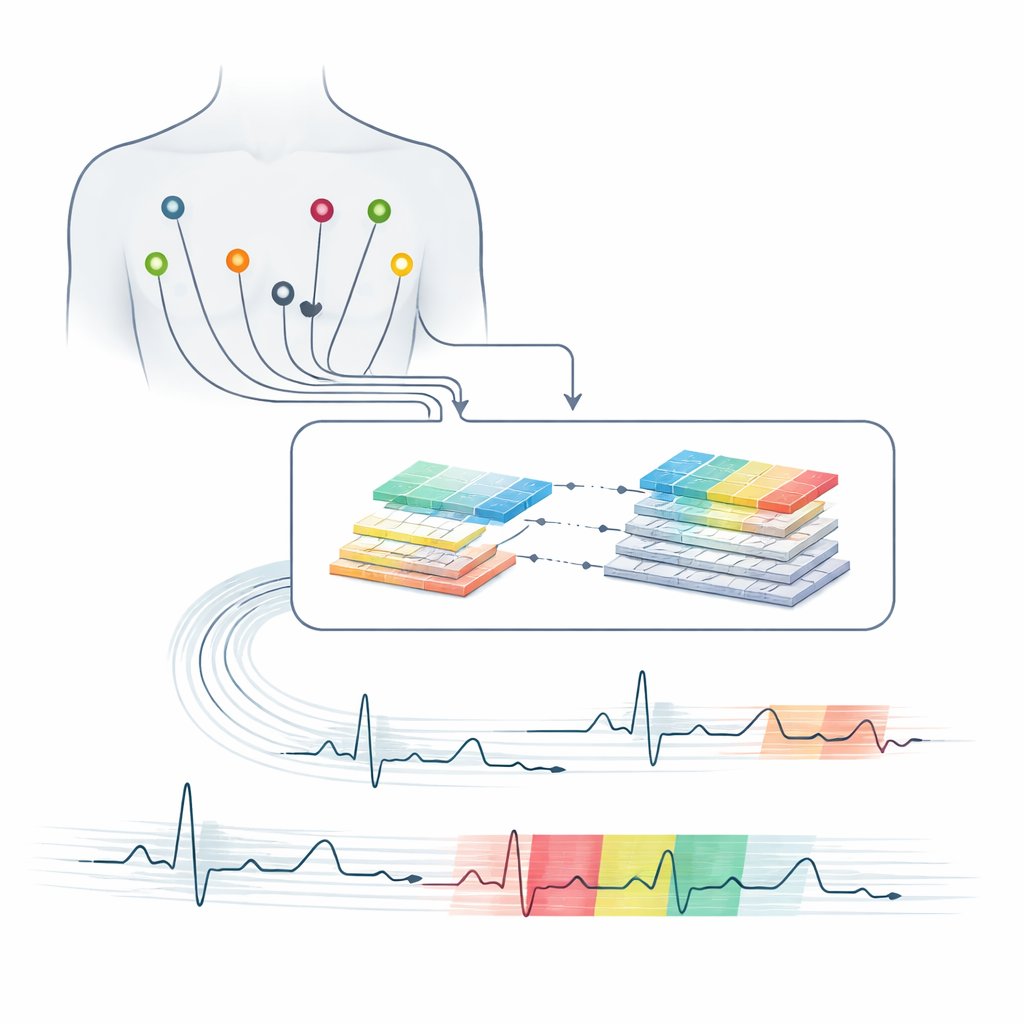
Ascoltare il cuore con molte «orecchie»
Un ECG a 12 derivazioni cattura l’attività elettrica del cuore da molteplici punti di osservazione mediante elettrodi su torace e arti. Ogni battito produce uno schema caratteristico di onde che rivelano come i segnali si propagano nelle camere cardiache. Piccole distorsioni in questi schemi possono indicare condizioni che vanno da variazioni benigne a interruzioni potenzialmente letali. Interpretare questi cambiamenti sottili attraverso molte derivazioni e in registrazioni prolungate è impegnativo, e le letture umane possono variare da un esperto all’altro. Allo stesso tempo, la cura moderna si basa sempre più sul monitoraggio continuo in ospedale, a domicilio e nei dispositivi indossabili, generando più dati di quanti i clinici possano realisticamente esaminare visivamente.
Insegnare a un assistente digitale a leggere segnali cardiaci complessi
I ricercatori hanno costruito un modello di deep learning che prende in input segmenti grezzi di ECG a 12 derivazioni e impara a riconoscere 27 problemi clinicamente rilevanti di ritmo e conduzione. Innanzitutto, hanno pre‑processato oltre 43.000 registrazioni etichettate da esperti provenienti dalla vasta raccolta PhysioNet/Computing in Cardiology 2020. I segnali provenienti da diversi ospedali avevano frequenze di campionamento differenti e contenevano rumore, valori mancanti e occasionali outlier. Il team ha ricampionionato tutti gli ECG a una frequenza comune, rimosso la deriva di linea di base e le interferenze elettriche, riempito i gap usando regole statisticamente valide e segmentato i dati in finestre sovrapposte di quattro secondi. Questa lunghezza di finestra si è dimostrata sufficiente a catturare i principali schemi di ritmo rimanendo breve ed efficiente per l’analisi in tempo reale.
Come il modello stratificato vede spazio, tempo e contesto
Il nucleo del sistema è una catena di tre moduli di rete neurale complementari. I layer convoluzionali agiscono come rivelatori di pattern, scansionando ogni derivazione dell’ECG alla ricerca di forme come picchi acuti, complessi allargati o segmenti distorti. Successivamente, i layer bidirezionali Long Short‑Term Memory seguono come queste caratteristiche evolvono nel tempo, osservando il ritmo sia in avanti sia all’indietro per cogliere intervalli irregolari e transizioni tra battiti. Infine, un blocco transformer applica un meccanismo di attenzione in grado di concentrarsi su frammenti di segnale lontani ma correlati attraverso tutte le derivazioni contemporaneamente, stabilendo connessioni che possono indicare condizioni sovrapposte. Insieme, questi strati convertono ogni breve finestra di ECG in una rappresentazione compatta dalla quale la rete stima la presenza di ciascuna delle 27 categorie di aritmia e disturbi di conduzione in modo multi‑etichetta.
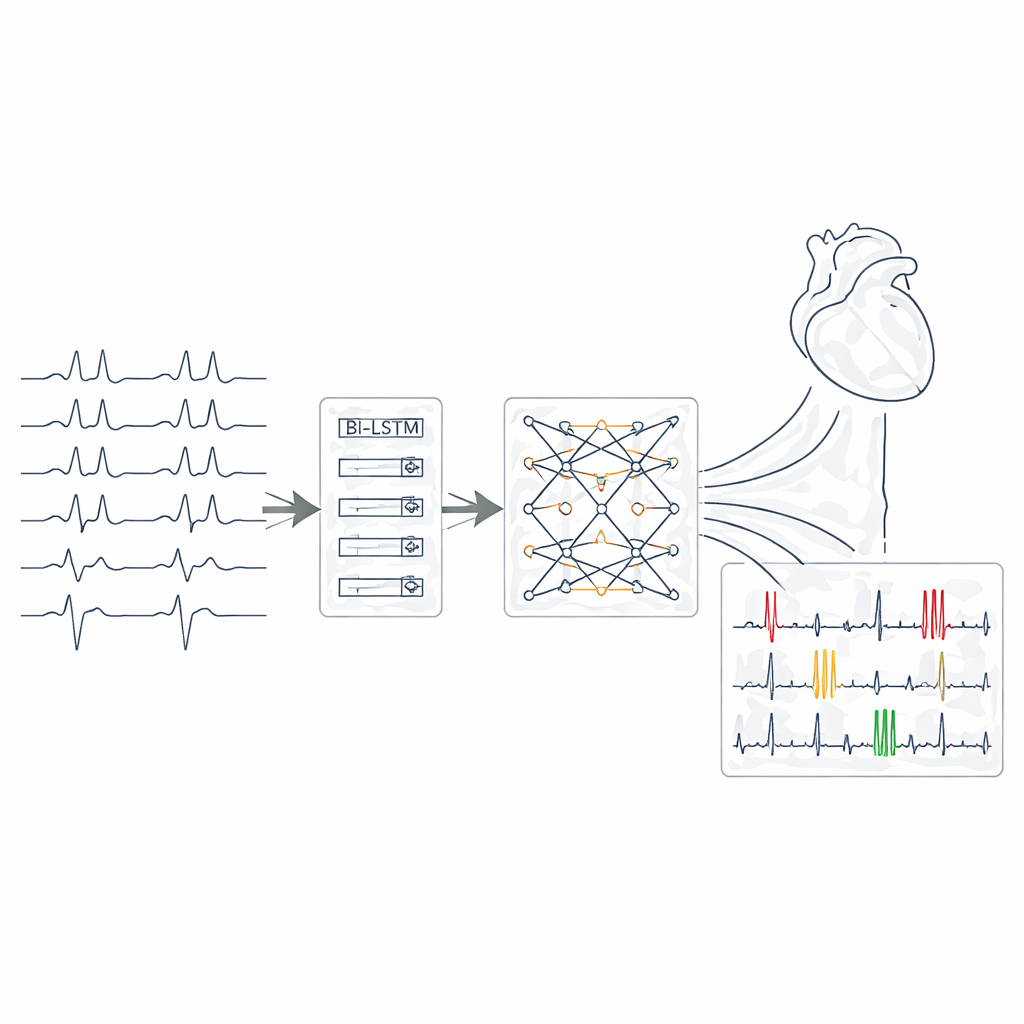
Aprire la scatola nera con evidenziazioni significative
Per rendere le decisioni del sistema comprensibili, gli autori hanno integrato una tecnica chiamata SHAP, che calcola quanto ogni porzione dell’ECG ha contribuito a una particolare predizione. Dopo l’addestramento, hanno utilizzato SHAP per generare «mappe di importanza» visive che evidenziano specifici segmenti d’onda e derivazioni su cui il modello si è basato in ciascun caso. Queste mappe spesso coincidevano con il ragionamento cardiologico standard: per esempio, il sistema enfatizzava l’assenza delle onde P e gli intervalli di battito irregolari nell’identificazione della fibrillazione atriale, o complessi QRS allargati e pause compensatorie nel riconoscimento di battiti ventricolari prematuri. Questo allineamento suggerisce che l’IA non si limita a memorizzare pattern, ma si concentra sugli stessi indizi fisiologici che gli esperti umani utilizzano.
Prestazioni nel mondo reale e prospettive future
Su un gruppo di test indipendente di pazienti, il modello ha classificato correttamente i ritmi con un’accuratezza complessiva di circa il 91% e ha mantenuto un forte equilibrio tra intercettare problemi veri ed evitare falsi allarmi sia nelle condizioni comuni sia in quelle rare. Per aritmie pericolose come i battiti ventricolari prematuri e la fibrillazione atriale, la sua capacità di distinguere anomalo da normale è risultata estremamente elevata. Notevolmente, il modello completo occupa meno di due megabyte di memoria e può analizzare una finestra di ECG in meno di dieci millisecondi, rendendolo adatto al dispiegamento in monitor a letto, registratori ambulatoriali o persino dispositivi indossabili intelligenti. In termini semplici, questo lavoro dimostra che un’IA compatta e spiegabile può aiutare a leggere gli ECG standard su un’ampia gamma di problemi del ritmo cardiaco, offrendo ai clinici giustificazioni visive chiare e aprendo la strada a un monitoraggio cardiaco più sicuro e accessibile.
Citazione: Al-Bairmani, M.T., Yazdchi, M. & Nasimi, F. A joint CNN-Bi-LSTM-transformer architecture with SHAP explanations for multi-label arrhythmia detection from 12-lead ECGs. Sci Rep 16, 11123 (2026). https://doi.org/10.1038/s41598-026-40925-5
Parole chiave: elettrocardiogramma, aritmia cardiaca, deep learning, IA spiegabile, monitoraggio cardiaco