Clear Sky Science · fr
Une architecture conjointe CNN-Bi-LSTM-transformer avec explications SHAP pour la détection multi-étiquettes d’arythmies à partir d’ECG 12 dérivations
Pourquoi le dépistage du rythme cardiaque concerne tout le monde
Les troubles du rythme cardiaque, ou arythmies, sont une cause majeure de mort subite, et pourtant le principal examen utilisé pour les détecter — l’électrocardiogramme à 12 dérivations (ECG) — dépend encore largement d’experts humains soumis à la pression du temps. Cette étude présente un système d’intelligence artificielle capable d’analyser des ECG standard pour détecter simultanément de nombreux troubles du rythme, d’expliquer ses résultats en termes compréhensibles pour les médecins et de fonctionner assez rapidement pour être intégré à des dispositifs portables ou des plateformes de télémédecine. Pour les patients, cela pourrait signifier une alerte plus précoce sur des rythmes dangereux ; pour les cliniciens, c’est l’espoir d’un assistant infatigable qui non seulement signale les anomalies mais montre aussi pourquoi.
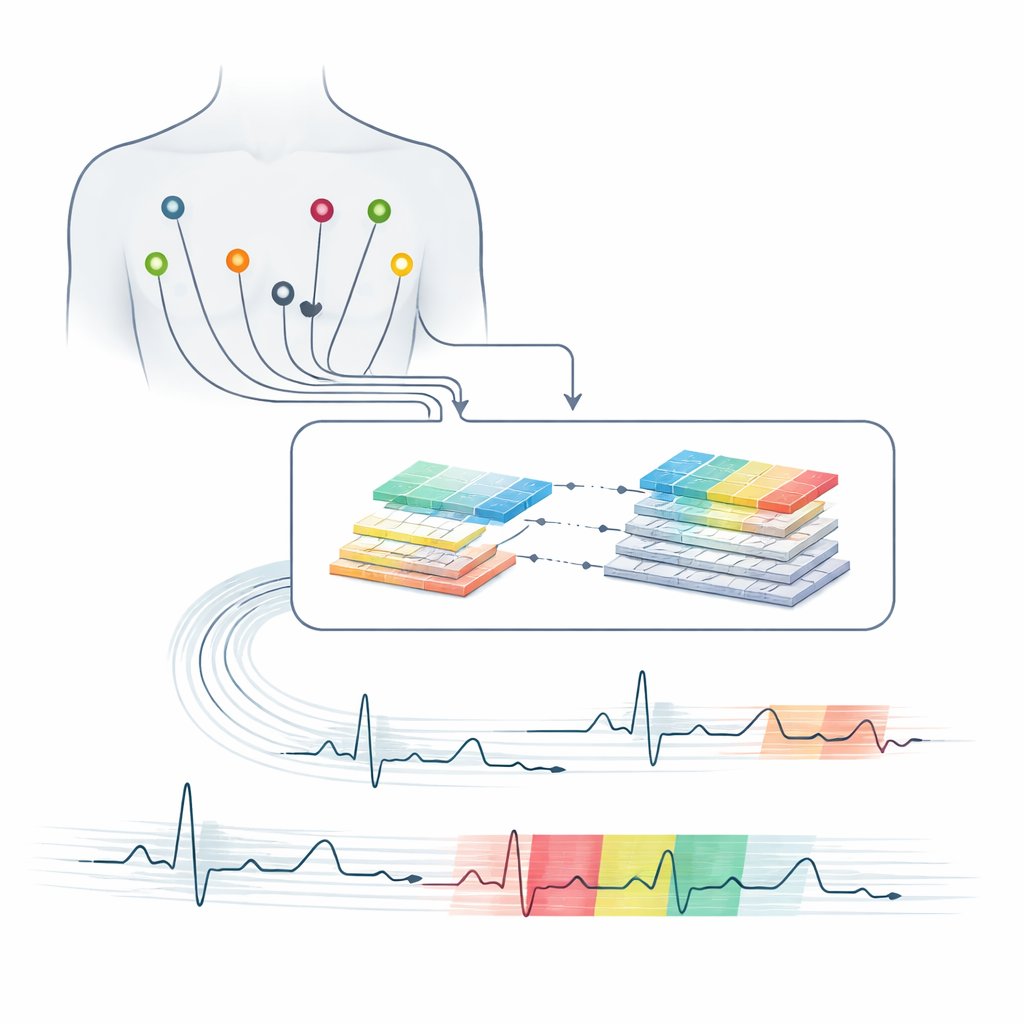
Écouter le cœur avec de nombreuses « oreilles »
Un ECG 12 dérivations capture l’activité électrique du cœur depuis plusieurs points de vue en plaçant des électrodes sur le thorax et les membres. Chaque battement produit un motif caractéristique d’ondes qui révèle la façon dont les signaux circulent dans les cavités cardiaques. De petites déformations de ces motifs peuvent indiquer des conditions allant de variations bénignes à des perturbations potentiellement mortelles. Interpréter ces changements subtils à travers de nombreuses dérivations et sur de longs enregistrements est exigeant, et les lectures humaines peuvent varier d’un expert à l’autre. Parallèlement, les soins modernes reposent de plus en plus sur une surveillance continue à l’hôpital, à domicile et dans les dispositifs portables, générant plus de données que les cliniciens ne peuvent raisonnablement examiner à l’œil nu.
Apprendre à un assistant numérique à lire des signaux cardiaques complexes
Les chercheurs ont construit un modèle d’apprentissage profond qui prend en entrée des segments bruts d’ECG 12 dérivations et apprend à reconnaître 27 problèmes cliniquement importants de rythme et de conduction. D’abord, ils ont prétraité plus de 43 000 enregistrements annotés par des experts issus de la vaste collection PhysioNet/Computing in Cardiology 2020. Les signaux provenant d’hôpitaux différents avaient des fréquences d’échantillonnage variées et contenaient du bruit, des valeurs manquantes et des valeurs aberrantes occasionnelles. L’équipe a rééchantillonné tous les ECG à une fréquence commune, supprimé la dérive de la ligne de base et les interférences électriques, comblé les lacunes selon des règles statistiques appropriées et segmenté les données en fenêtres qui se chevauchent de quatre secondes. Cette longueur de fenêtre s’est avérée suffisante pour capturer les motifs rythmiques clés tout en restant courte et efficace pour une analyse en temps réel.
Comment le modèle en couches perçoit l’espace, le temps et le contexte
Le noyau du système est une chaîne de trois modules de réseau neuronal complémentaires. Les couches convolutionnelles agissent comme des détecteurs de motifs, balayant chaque dérivation de l’ECG à la recherche de formes telles que des pointes nettes, des complexes élargis ou des segments déformés. Ensuite, des couches LSTM bidirectionnelles suivent l’évolution de ces caractéristiques dans le temps, observant effectivement le rythme à la fois vers l’avant et vers l’arrière pour capturer les intervalles irréguliers et les transitions entre battements. Enfin, un bloc transformer applique un mécanisme d’attention capable de se concentrer sur des fragments de signal distants mais liés à travers toutes les dérivations simultanément, établissant des connexions qui peuvent indiquer des conditions qui se chevauchent. Ensemble, ces couches convertissent chaque fenêtre courte d’ECG en une représentation compacte à partir de laquelle le réseau estime la présence de chacune des 27 catégories d’arythmie et de troubles de conduction selon un mode multi‑étiquette.
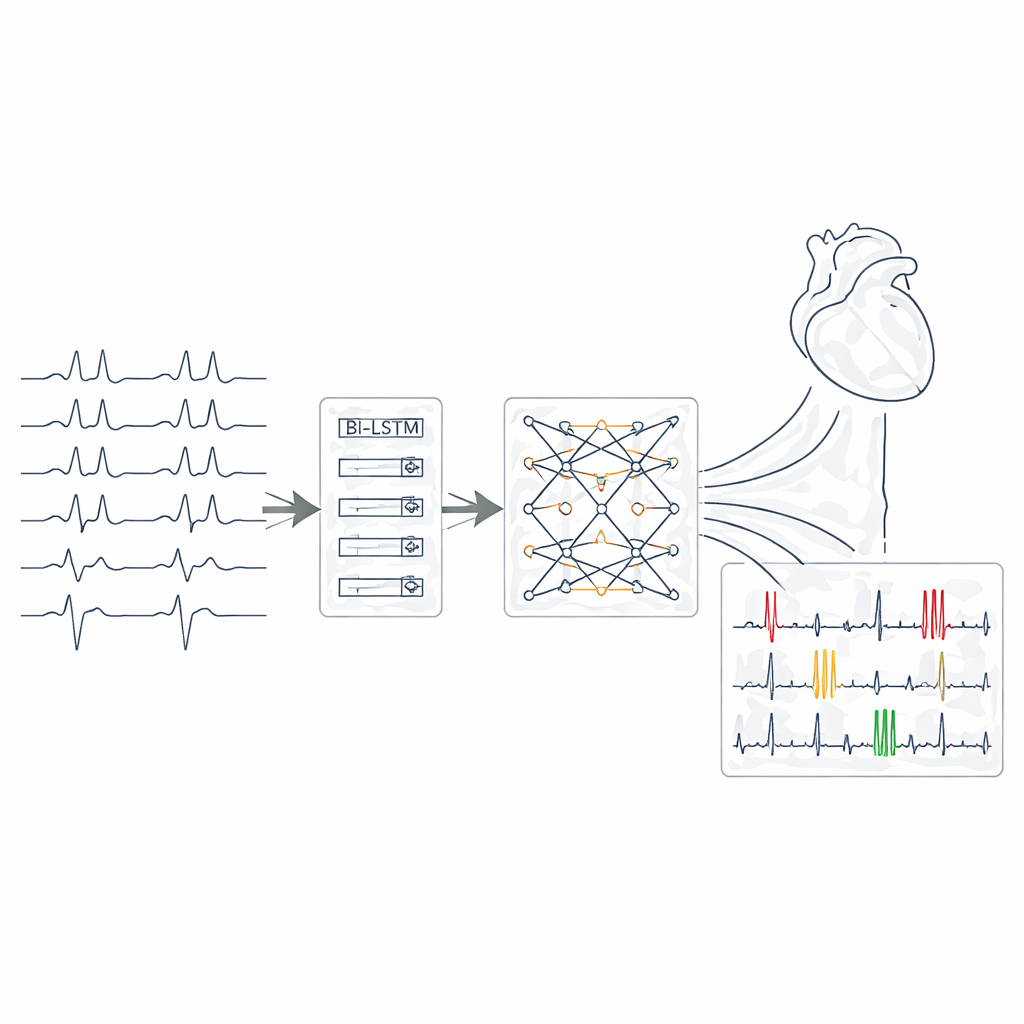
Ouvrir la boîte noire avec des mises en évidence signifiantes
Pour rendre les décisions du système compréhensibles, les auteurs ont intégré une technique appelée SHAP, qui calcule la contribution de chaque portion de l’ECG à une prédiction donnée. Après l’entraînement, ils ont utilisé SHAP pour générer des « cartes d’importance » visuelles mettant en évidence des segments d’onde et des dérivations spécifiques sur lesquels le modèle s’est appuyé pour chaque cas. Ces cartes correspondaient souvent au raisonnement cardiologique standard : par exemple, le système mettait en avant l’absence d’ondes P et l’irrégularité des intervalles lors de l’identification de la fibrillation auriculaire, ou des complexes QRS élargis et des pauses compensatoires pour reconnaître des extrasystoles ventriculaires. Cet alignement suggère que l’IA ne se contente pas de mémoriser des motifs, mais qu’elle se base sur les mêmes indices physiologiques que les experts humains.
Performance en conditions réelles et promesse future
Sur un groupe de test indépendant de patients, le modèle a correctement classé les rythmes avec une précision globale d’environ 91 % et a maintenu un bon équilibre entre la détection des vrais problèmes et l’évitement des fausses alertes, tant pour les conditions fréquentes que rares. Pour les arythmies dangereuses comme les extrasystoles ventriculaires et la fibrillation auriculaire, sa capacité à distinguer l’anormal du normal était extrêmement élevée. Remarquablement, le modèle complet occupe moins de deux mégaoctets de mémoire et peut analyser une fenêtre d’ECG en moins de dix millisecondes, ce qui le rend adapté à un déploiement dans des moniteurs de chevet, des enregistreurs ambulatoires ou même des appareils portables intelligents. En termes simples, ce travail montre qu’une IA compacte et explicable peut aider à lire des ECG standard pour une large gamme de troubles du rythme cardiaque, en offrant aux cliniciens des justifications visuelles claires tout en ouvrant la voie à une surveillance cardiaque plus sûre et plus accessible.
Citation: Al-Bairmani, M.T., Yazdchi, M. & Nasimi, F. A joint CNN-Bi-LSTM-transformer architecture with SHAP explanations for multi-label arrhythmia detection from 12-lead ECGs. Sci Rep 16, 11123 (2026). https://doi.org/10.1038/s41598-026-40925-5
Mots-clés: électrocardiogramme, arythmie cardiaque, apprentissage profond, IA explicable, surveillance cardiaque