Clear Sky Science · nl
Elektrochemisch geoptimaliseerde multi-component polyacrylonitril-nanovezel-saffolds als platform voor driedimensionale glioblastoomcelkweek
Waarom een nieuw labmodel voor hersenkanker ertoe doet
Glioblastoom is een van de dodelijkste hersentumoren, en veel behandelingen die veelbelovend lijken in het laboratorium falen bij patiënten. Een belangrijke reden is dat de meeste labtests kankercellen laten groeien als een platte laag in een schaaltje, wat sterk verschilt van de verwarde, driedimensionale structuur van een echte tumor in de hersenen. Deze studie introduceert een nieuw laboratoriumplatform waarmee glioblastoomcellen in 3D kunnen groeien op een web van ultradunne vezels terwijl hun gedrag in realtime elektrisch wordt gemonitord, wat laboratoriumexperimenten mogelijk dichter bij wat in patiënten gebeurt brengt.
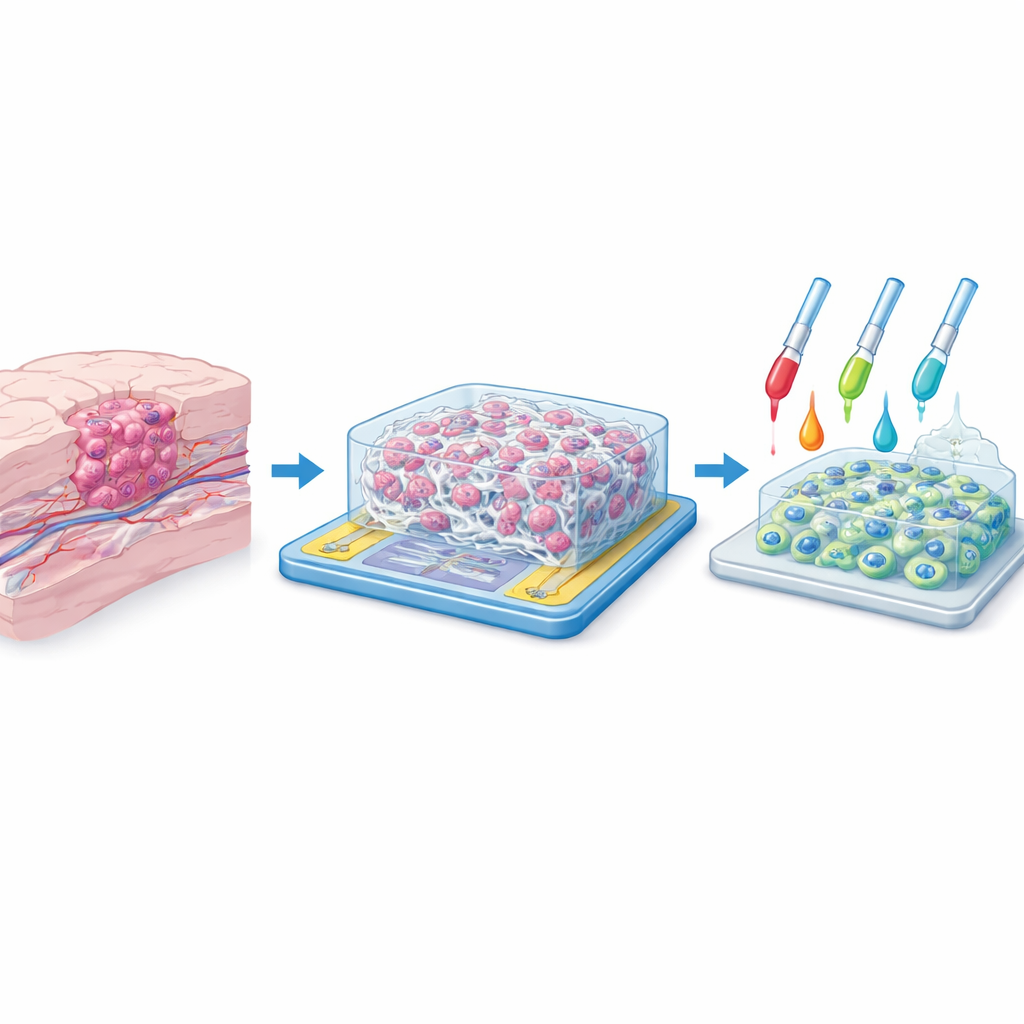
Het thuis van de tumor nabootsen
In de hersenen leven tumorcellen niet op een vlakke ondergrond. Ze weven zich tussen ondersteunend weefsel, hechten zich aan kleine proteïnevezels en voelen signalen van naburige cellen vanuit alle richtingen. Traditionele tweedimensionale kweekmodellen vereenvoudigen deze complexiteit en leveren vaak misleidende resultaten op bij het testen van nieuwe medicijnen. De onderzoekers wilden een realistischer "thuis" voor glioblastoomcellen bouwen: een driedimensionale scaffold van synthetische vezels, met poriën groot genoeg zodat cellen erin kunnen kruipen en zich eromheen kunnen bewegen. Hun doel was het fysieke gevoel van hersenweefsel na te bootsen terwijl ze wetenschappers tegelijk in staat stelden het celgedrag te volgen zonder het te verstoren.
Een miniforest van vezels spinnen
Om deze kunstmatige microomgeving te creëren, gebruikte het team een techniek genaamd electrospinning, waarmee vloeibare polymeren worden uitgetrokken tot continue strengen dunner dan duizendsten van een millimeter. Het basismateriaal was polyacrylonitril, een sterke, stabiele kunststof die bekendstaat om het vormen van uniforme nanovezels. Door zorgvuldig spanning, afstand en debiet te regelen, produceerden ze matten van overlappende vezels met diameters rond 400–500 nanometer en porieopeningen van ongeveer 9–10 micrometer — net breed genoeg zodat individuele kankercellen driedimensionaal kunnen infiltreren. Microscopen toonden gladde, continue vezels zonder parelvormige defecten en een consistent, sterk poreus netwerk, wat suggereert dat cellen een realistische, doolhofachtige omgeving zouden aantreffen die lijkt op het natuurlijke weefsel rond een tumor.
Meerdere ingrediënten combineren in één slimme scaffold
De innovatie in dit werk gaat verder dan het basale vezelmatje. De auteurs voegden meerdere functionele ingrediënten toe aan de vezels om zowel celgedrag als elektrische signalering bij te sturen. Ze testten zes combinaties op transparant geleidend glas: gewone vezels; vezels met een lichtgevoelig coumarinedye (C500); vezels met grafeenoxide, een velachtig koolstofmateriaal; vezels met een holmium-gebaseerd metaal–orgaanframework; en twee mengsels die grafeenoxide combineerden met respectievelijk C500 of het metaal–orgaanframework. Deze additieven werden gekozen om de vezels te versterken, de oppervlakchemie te verfijnen en hun vermogen te verbeteren kleine elektrische signalen te geleiden. Geavanceerde elektrische tests lieten zien dat sommige mengsels, met name die met zowel grafeenoxide als het metaal–orgaanframework, elektronen zeer gemakkelijk door het systeem lieten bewegen.
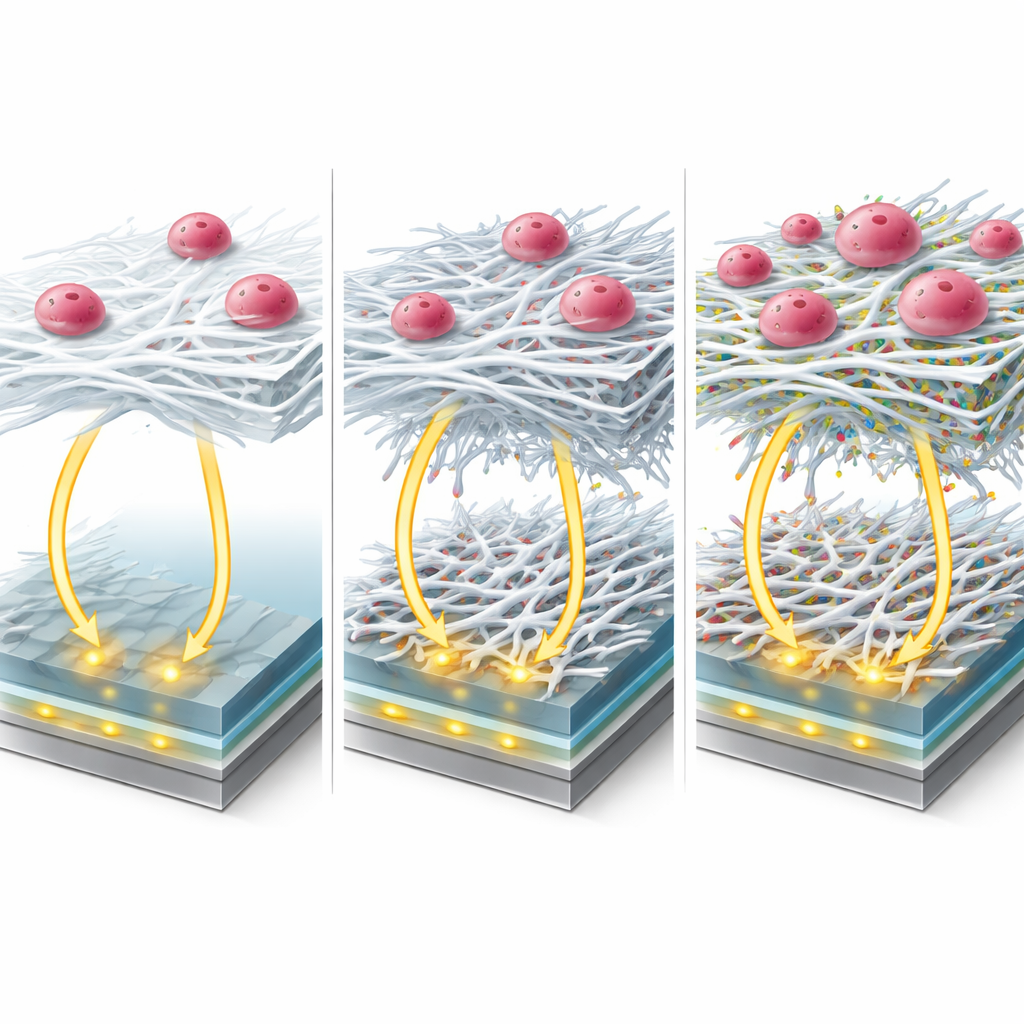
Wanneer goede elektronica botst met slechte biologie
Wat elektrisch gezien het beste lijkt, is echter niet altijd het beste voor levende cellen. Toen de onderzoekers twee humane glioblastoomcellijnen lieten groeien op de verschillende vezelbeklede elektroden, vonden ze een opvallende mismatch. De configuratie met grafeenoxide en het metaal–orgaanframework had de laagste elektrische weerstand maar faalde vrijwel volledig in het ondersteunen van celhechting. In tegenstelling daarmee boden vezels met de coumarinedye C500 zowel lage weerstand als uitstekende celgezondheid: meer dan 95 procent van de cellen bleef levensvatbaar, en fluorescentiekleuring toonde een dichte, goed georganiseerde driedimensionale verspreiding van kernen door de scaffold heen. Metingen van elektrische impedantie voor en na het enten van cellen veranderden duidelijk naarmate cellen de vezels koloniseerden, wat bevestigt dat het platform celgroei kan volgen zonder ze telkens te hoeven verwijderen of kleuren.
Wat dit betekent voor toekomstig onderzoek naar hersenkanker
De studie toont aan dat het mogelijk is een realistische driedimensionale groeicomfort voor glioblastoomcellen te combineren met een ingebouwde "stethoscoop" die elektrisch luistert naar wat de cellen doen. Van de geteste recepten bood het met C500 verrijkte vezelscaffold de beste balans tussen cellenvriendelijkheid en gevoeligheid voor kleine elektrische veranderingen. Voor niet-specialisten is de kernboodschap dat dit platform hersentumorcellen kan huisvesten op een manier die meer lijkt op echte tumoren, terwijl wetenschappers in realtime kunnen volgen hoe ze groeien en reageren op potentiële geneesmiddelen. Zo’n systeem kan helpen de kloof te overbruggen tussen te sterk vereenvoudigde laboratoriumschalen en de complexe realiteit van het menselijk brein, en daarmee de kans vergroten dat hier bewezen therapieën patiënten daadwerkelijk ten goede komen.
Bronvermelding: Kurt, Ş., Bal Altuntaş, D., Sevim Nalkıran, H. et al. Electrochemically optimized multi-component polyacrylonitrile nanofiber scaffolds as a platform for three-dimensional glioblastoma cell culture. Sci Rep 16, 12644 (2026). https://doi.org/10.1038/s41598-026-39640-y
Trefwoorden: glioblastoom, 3D-celkweek, nanovezel-saffold, tumormicro-omgeving, elektrochemische monitoring