Clear Sky Science · fr
Échafaudages nanofibreux en polyacrylonitrile multicomposants optimisés électrochimiquement comme plateforme pour la culture tridimensionnelle de cellules de glioblastome
Pourquoi un nouveau modèle de laboratoire pour le cancer du cerveau est important
Le glioblastome est l’un des cancers cérébraux les plus mortels, et de nombreux traitements prometteurs en laboratoire échouent chez les patients. Une raison majeure est que la plupart des essais en laboratoire cultivent les cellules cancéreuses sous forme de couches plates dans une boîte, ce qui diffère fortement de la structure tridimensionnelle complexe d’une tumeur réelle dans le cerveau. Cette étude présente une nouvelle plateforme de laboratoire qui permet aux cellules de glioblastome de croître en 3D sur un réseau de fibres ultrafines tout en surveillant leur comportement électriquement en temps réel, rapprochant potentiellement les expériences de laboratoire de ce qui se passe chez les patients.
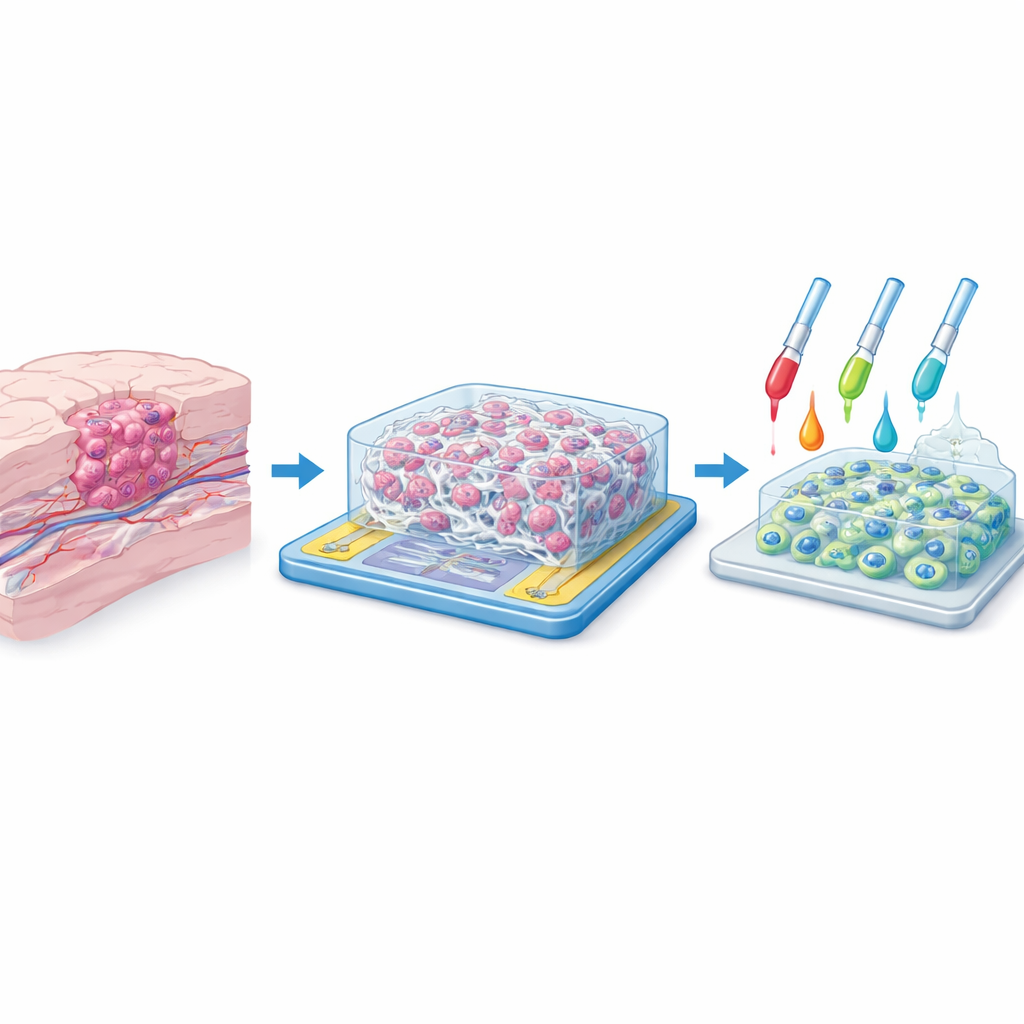
Recréer le « chez‑soi » de la tumeur
Dans le cerveau, les cellules tumorales ne vivent pas sur une surface plate. Elles s’insinuent entre les tissus de soutien, s’accrochent à de minuscules fibres protéiques et perçoivent des signaux de cellules voisines dans toutes les directions. Les cultures bidimensionnelles traditionnelles aplatissent cette complexité, donnant souvent des résultats trompeurs lors des tests de nouveaux médicaments. Les auteurs ont cherché à construire un « chez‑soi » plus réaliste pour les cellules de glioblastome : un échafaudage tridimensionnel constitué de fibres synthétiques, avec des pores assez larges pour que les cellules puissent y pénétrer et s’y déplacer. Leur objectif était d’imiter la sensation physique du tissu cérébral tout en permettant aux chercheurs d’observer le comportement des cellules sans les perturber.
Tourner une miniforêt de fibres
Pour créer cet microenvironnement artificiel, l’équipe a utilisé une technique appelée électrofilage, qui étire un polymère liquide en fils continus plus fins qu’un millième de millimètre. Le matériau de base était le polyacrylonitrile, un plastique résistant et stable connu pour former des nanofibres uniformes. En contrôlant soigneusement la tension, la distance et le débit, ils ont produit des tapis de fibres superposées d’un diamètre d’environ 400–500 nanomètres et des ouvertures de pores d’environ 9–10 micromètres — juste assez larges pour que des cellules cancéreuses individuelles s’y infiltrent en trois dimensions. La microscopie a montré des fibres lisses et continues sans défauts en perles et un réseau constant et très poreux, suggérant que les cellules rencontreraient un environnement labyrinthique réaliste similaire au tissu naturel entourant une tumeur.
Mélanger plusieurs ingrédients en un échafaudage intelligent
L’innovation de ce travail va au‑delà du simple tapis de fibres. Les auteurs ont intégré plusieurs ingrédients fonctionnels dans les fibres pour ajuster à la fois le comportement cellulaire et la lecture électrique. Ils ont testé six combinaisons sur du verre conducteur transparent : fibres simples ; fibres avec un colorant coumarinique photo‑réactif (C500) ; fibres avec de l’oxyde de graphène, un matériau carboné en feuillets ; fibres avec un cadre métal‑organique à base d’holmium ; et deux mélanges combinant l’oxyde de graphène soit avec C500 soit avec le cadre métal‑organique. Ces additifs ont été choisis pour renforcer les fibres, modifier la chimie de surface et améliorer leur capacité à conduire de faibles signaux électriques. Des tests électriques sophistiqués ont montré que certaines compositions, en particulier celles contenant à la fois l’oxyde de graphène et le cadre métal‑organique, permettaient aux électrons de circuler très facilement dans le système.
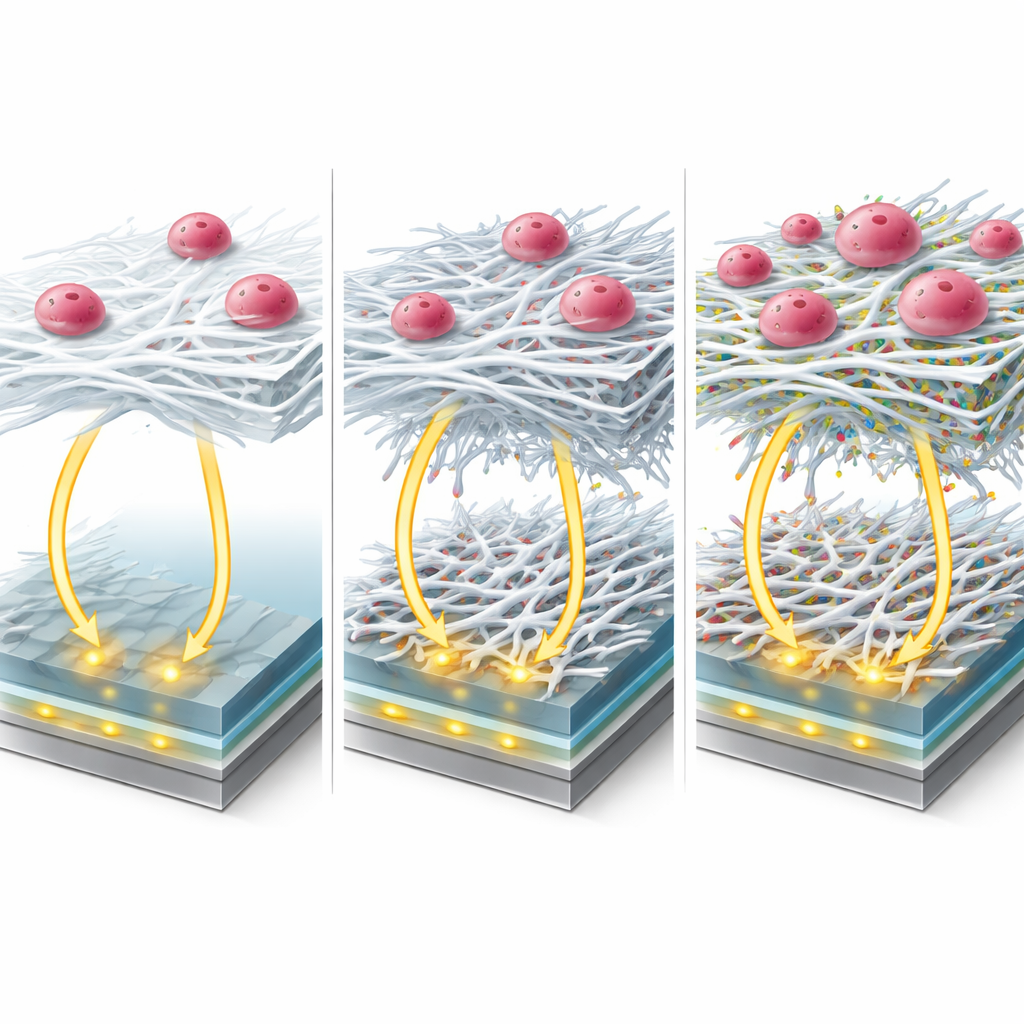
Quand une bonne conductivité ne rime pas avec bonne biologie
Cependant, ce qui est optimal électriquement n’est pas toujours idéal pour les cellules vivantes. Lorsque les chercheurs ont cultivé deux lignées humaines de glioblastome sur les électrodes recouvertes des différentes fibres, ils ont constaté un contraste frappant. La configuration avec l’oxyde de graphène et le cadre métal‑organique présentait la résistance électrique la plus faible mais échouait presque complètement à soutenir l’adhésion cellulaire. En revanche, les fibres contenant le colorant coumarinique C500 offraient à la fois une faible résistance et une excellente viabilité cellulaire : plus de 95 % des cellules restaient viables, et le marquage fluorescent révélait une répartition tridimensionnelle dense et bien organisée des noyaux dans tout l’échafaudage. Les mesures d’impédance électrique avant et après l’ensemencement cellulaire évoluaient clairement au fur et à mesure que les cellules colonisaient les fibres, confirmant que la plateforme pouvait suivre la croissance cellulaire sans nécessiter de retrait ou de marquage systématique à chaque fois.
Ce que cela signifie pour la recherche future sur le cancer du cerveau
L’étude montre qu’il est possible de combiner un environnement de croissance tridimensionnel réaliste pour les cellules de glioblastome avec un « stéthoscope » intégré qui écoute électriquement ce que font les cellules. Parmi les recettes testées, l’échafaudage enrichi en C500 a trouvé le meilleur compromis entre compatibilité cellulaire et sensibilité aux faibles variations électriques. Pour un public non spécialisé, le message clé est que cette plateforme peut héberger des cellules tumorales cérébrales d’une manière se rapprochant davantage des tumeurs réelles, tout en permettant aux chercheurs de surveiller en temps réel leur croissance et leur réponse à des médicaments potentiels. Un tel système peut aider à combler le fossé entre des boîtes de laboratoire trop simplifiées et la complexité du cerveau humain, augmentant les chances que des thérapies efficaces en laboratoire profitent réellement aux patients.
Citation: Kurt, Ş., Bal Altuntaş, D., Sevim Nalkıran, H. et al. Electrochemically optimized multi-component polyacrylonitrile nanofiber scaffolds as a platform for three-dimensional glioblastoma cell culture. Sci Rep 16, 12644 (2026). https://doi.org/10.1038/s41598-026-39640-y
Mots-clés: glioblastome, culture cellulaire 3D, échafaudage nanofibreux, microenvironnement tumoral, suivi électrochimique