Clear Sky Science · nl
Systematische analyse van snRNA-genen onthult frequente RNU2-2-varianten bij dominante en recessieve ontwikkelings- en epileptische encefalopathieën
Waarom piepkleine RNA-stukjes belangrijk zijn voor de hersenen van kinderen
Artsen kunnen nu bijna elk lettertje van het DNA van een kind lezen, maar toch verlaten veel kinderen met ernstige ontwikkelingsachterstand en epilepsie de kliniek zonder duidelijke diagnose. Deze studie richt de schijnwerpers op een verrassend klein en vaak over het hoofd gezien deel van onze genetische code: miniatuurgenen voor RNA die cellen helpen berichten in te korten en samen te voegen voordat ze in eiwitten worden omgezet. De auteurs tonen aan dat veranderingen in één van deze genen, RNU2-2 genoemd, een veelvoorkomende oorzaak zijn van ernstige neuro-ontwikkelingsstoornissen en tot wel 1 op 300 kinderen met deze aandoeningen kunnen treffen.
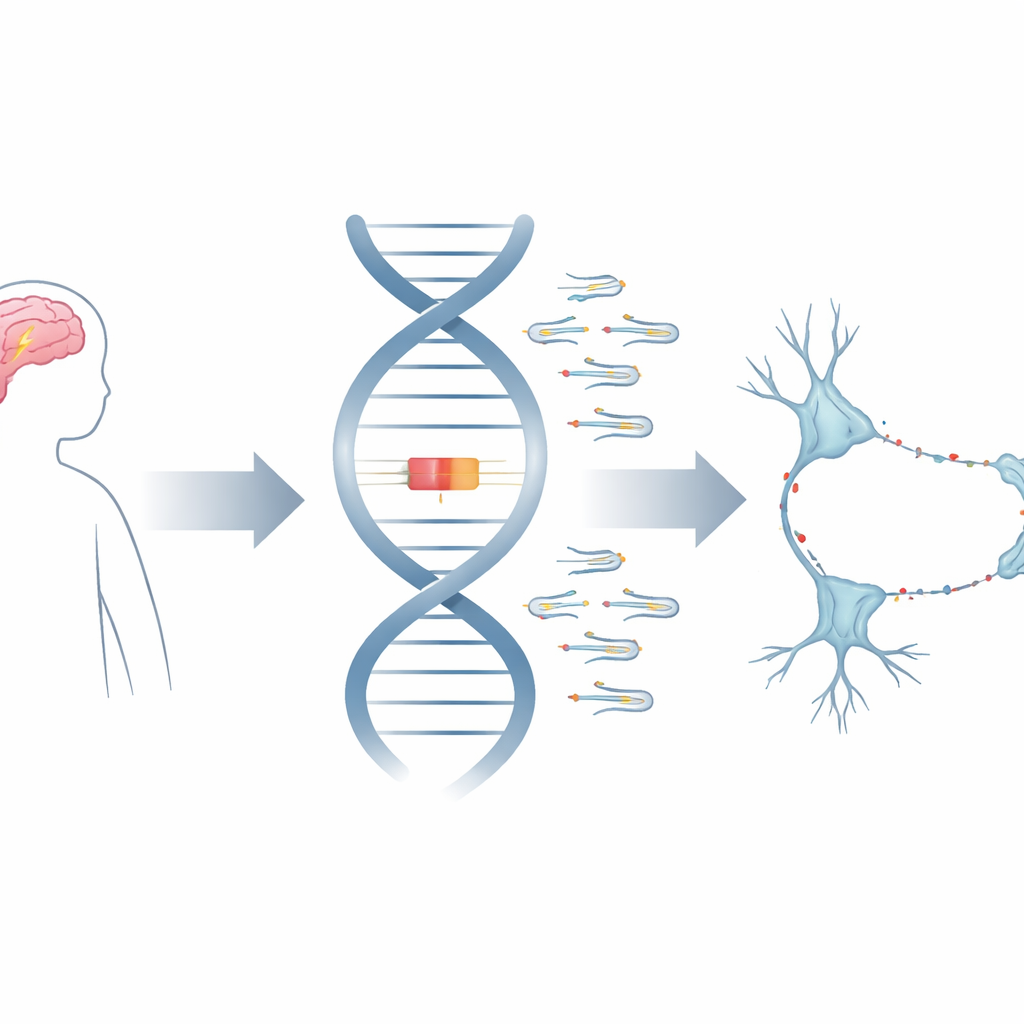
Een verborgen laag van de genetische gebruiksaanwijzing
De meeste genetische tests richten zich op eiwit-coderende genen, maar onze cellen vertrouwen ook op vele korte RNA-moleculen die nooit eiwitten worden. Tot deze groep behoren kleine nucleaire RNA’s, of snRNA’s, die de kern vormen van het spliceosoom—de moleculaire machine die ruwe RNA-berichten bijsnijdt en de nuttige stukjes aan elkaar zet. Het RNU2-2-gen maakt één variant van het U2-snRNA, een cruciaal onderdeel dat helpt het exacte knippunt in RNA te bepalen. Omdat er veel kopieën van snRNA-genen bestaan die erg op elkaar lijken, waren ze moeilijk te bestuderen en werden ze vaak afgedaan als inactieve “pseudogenen.”
Duizenden genomen scannen op actieve snRNA-genen
Het team doorzocht eerst meer dan 2.000 geannoteerde snRNA-genen in het menselijk genoom en gebruikte beschikbare hersen-RNA-data en regelgevende kaarten om waarschijnlijke werkende genen te onderscheiden van inactieve relikten. Deze inspanning identificeerde 200 snRNA-genen die functioneel lijken te zijn, waarvan vele eerder als pseudogenen waren bestempeld. De onderzoekers doorzochten vervolgens genoomdata van meer dan 34.000 mensen met zeldzame aandoeningen in Frankrijk, waarbij ze zich richtten op ongebruikelijke nieuwe mutaties die alleen bij een kind voorkomen, evenals op paren mutaties die van beide ouders worden geërfd. Opvallend waren varianten in RNU2-2 in beide analyses prominent aanwezig, vooral bij personen met neuro-ontwikkelingsstoornissen.
Een veelvoorkomende oorzaak van ontwikkelingsachterstand en epilepsie
Door gegevens uit Frankrijk en internationale samenwerkingsverbanden te bundelen, stelden de auteurs 141 patiënten uit 122 families samen met veranderingen in RNU2-2. Vijfendertig kinderen droegen één van twee terugkerende mutaties die dominant werken, wat betekent dat één veranderde kopie van het gen voldoende is om ziekte te veroorzaken. Een nog grotere groep—91 aangedane personen uit 73 families—droeg schadelijke varianten op beide kopieën van het gen, wat een recessieve vorm van de aandoening onthult die minstens twee keer zo frequent is als de dominante vorm. Ongeacht de overerving hadden bijna alle aangedane personen ontwikkelingsachterstand en verstandelijke beperking, en ongeveer 85% ervoer epilepsie, meestal beginnend voor de leeftijd van drie jaar. Veel patiënten toonden ook autistische kenmerken, bewegingsproblemen en subtiele maar terugkerende gelaatstrekken.
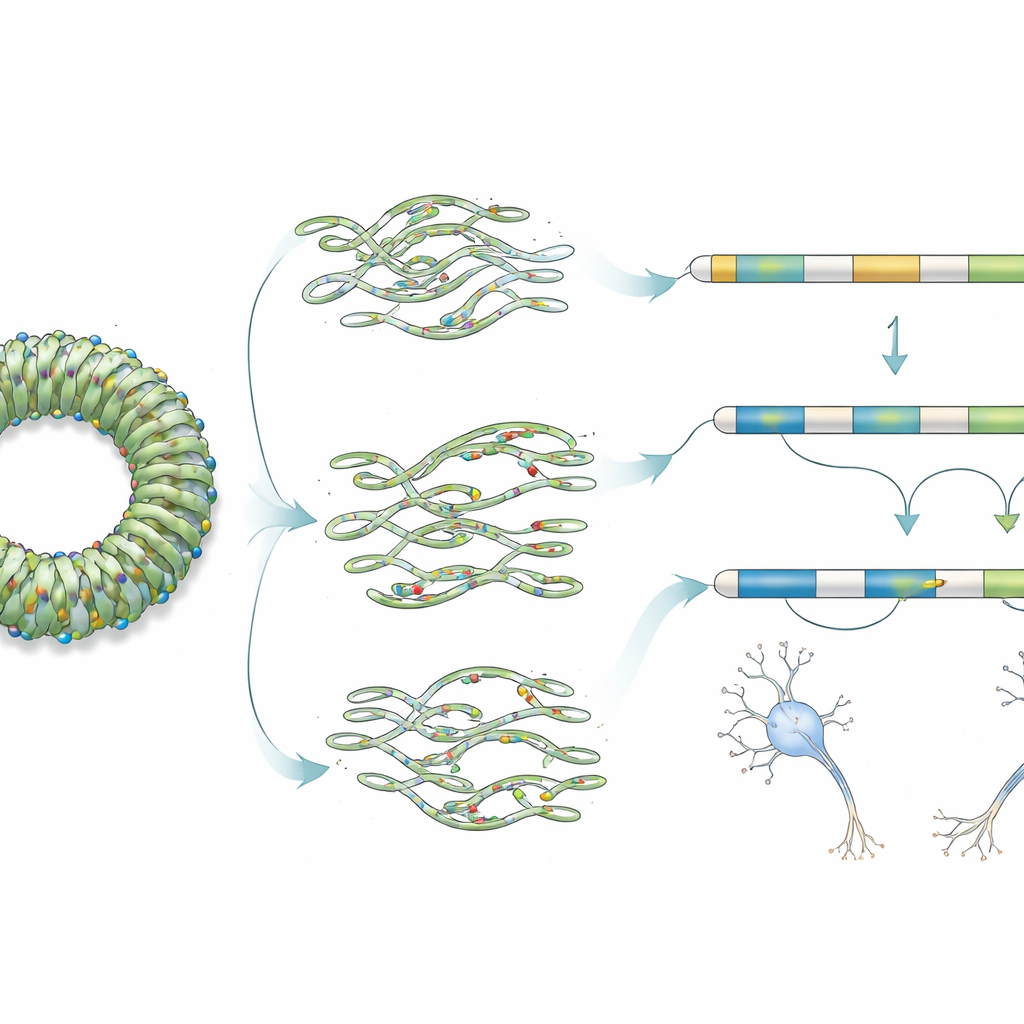
Hoe kleine RNA-veranderingen de hersenfunctie verstoren
Om te begrijpen hoe RNU2-2-varianten cellen schaden, plaatsten de onderzoekers elke mutatie op gedetailleerde driedimensionale modellen van het U2-RNA binnen het spliceosoom. Sommige veranderingen liggen in regio’s die U2 helpen het juiste “branch point” in RNA te herkennen, terwijl andere structurele elementen raken die nodig zijn om het RNA samen te stellen en in de kern te importeren. De auteurs tonen aan dat bepaalde varianten waarschijnlijk de U2-functie volledig vernietigen, terwijl andere deze gedeeltelijk verzwakken. Toen ze bloedcellen van patiënten onderzochten, zagen ze slechts subtiele verschuivingen: sommige exonen werden iets vaker overgeslagen en DNA-methyleringspatronen—een chemisch markeersysteem op DNA—waren mild aangepast op variantspecifieke manieren. Deze bescheiden signalen passen bij het idee dat RNU2-2-mutaties de RNA-verwerking van veel genen licht verstoren, met bijzonder sterke gevolgen in de ontwikkelende hersenen waar RNU2-2 actiever is.
Een continuüm tussen dominante en recessieve ziekte
Een van de meest intrigerende bevindingen is dat dominante en recessieve vormen van de RNU2-2-aandoening klinisch opvallend op elkaar lijken. In plaats van twee afzonderlijke ziekten stellen de auteurs een ‘gradient-of-impact’-model voor. Zeer ingrijpende varianten op sleutelplaatsen kunnen op zichzelf ziekte veroorzaken en dominant werken. Mildere veranderingen hebben mogelijk weinig effect tenzij een kind een tweede schadelijke variant op de andere kopie van het gen erft, wat een recessieve ziekte veroorzaakt. Andere combinaties—zoals één sterke en één zwakke variant—kunnen bepalen hoe ernstig de symptomen worden. Omdat snRNA-genen zoals RNU2-2 nieuwe mutaties in een uitzonderlijk hoog tempo accumuleren, ontstaan deze verschillende genetische scenario’s vaak in de bevolking.
Wat dit betekent voor gezinnen en toekomstig onderzoek
Voor gezinnen die antwoorden zoeken, laat dit werk zien dat RNU2-2-varianten samen ongeveer 0,35% van alle neuro-ontwikkelingsstoornissen verklaren—waardoor dit piepkleine RNA-gen een van de meest frequent betrokken niet-coderende genen in kinderhersenziekten is, vergelijkbaar in impact met het recent ontdekte ReNU-syndroomgen RNU4-2. De studie waarschuwt clinici er ook voor om zorgvuldig te zoeken naar een tweede verborgen variant wanneer zij een nieuwe mutatie in RNU2-2 of aanverwante snRNA-genen zien, in plaats van te veronderstellen dat het altijd om een puur dominant effect gaat. Breder gezien suggereren de bevindingen dat veel andere “niet-coderende” RNA-genen stilletjes ten grondslag kunnen liggen aan onverklaarde ontwikkelingsstoornissen. Naarmate genoomsequencing en long-read-technologieën verbeteren, kan het systematisch verkennen van deze over het hoofd geziene regio’s een nieuwe klasse onthullen van veelvoorkomende maar eerder onzichtbare genetische oorzaken van ernstige kinder-epilepsie en verstandelijke beperking.
Bronvermelding: Leitão, E., Santini, A., Cogne, B. et al. Systematic analysis of snRNA genes reveals frequent RNU2-2 variants in dominant and recessive developmental and epileptic encephalopathies. Nat Genet 58, 782–797 (2026). https://doi.org/10.1038/s41588-026-02547-5
Trefwoorden: neuro-ontwikkelingsstoornissen, epileptische encefalopathie, spliceosoom, niet-coderend RNA, RNU2-2-varianten