Clear Sky Science · nl
Hyperpyramidaliseerde alkenen met bindingsorders rond 1,5 als synthetische bouwstenen
Waarom het buigen van bindingen in de praktijk uitmaakt
Synthesecollegen leren meestal dat een dubbele binding tussen twee koolstofatomen een vlakke, stevige verbinding is, een beetje als een starre plank in een constructie. Dit artikel onderzoekt wat er gebeurt wanneer die plank wordt gedwongen te buigen en te knikken binnen kleine koolstofkooien. Het werk onthult nieuwe typen "veerbelaste" moleculen waarvan de ingebouwde spanning ze uitzonderlijk geneigd maakt om met andere delen samen te klikken, en zo nieuwe wegen opent om compacte, driedimensionale structuren te ontwerpen die nuttig kunnen zijn in geneesmiddelenonderzoek en energiewetenschap.
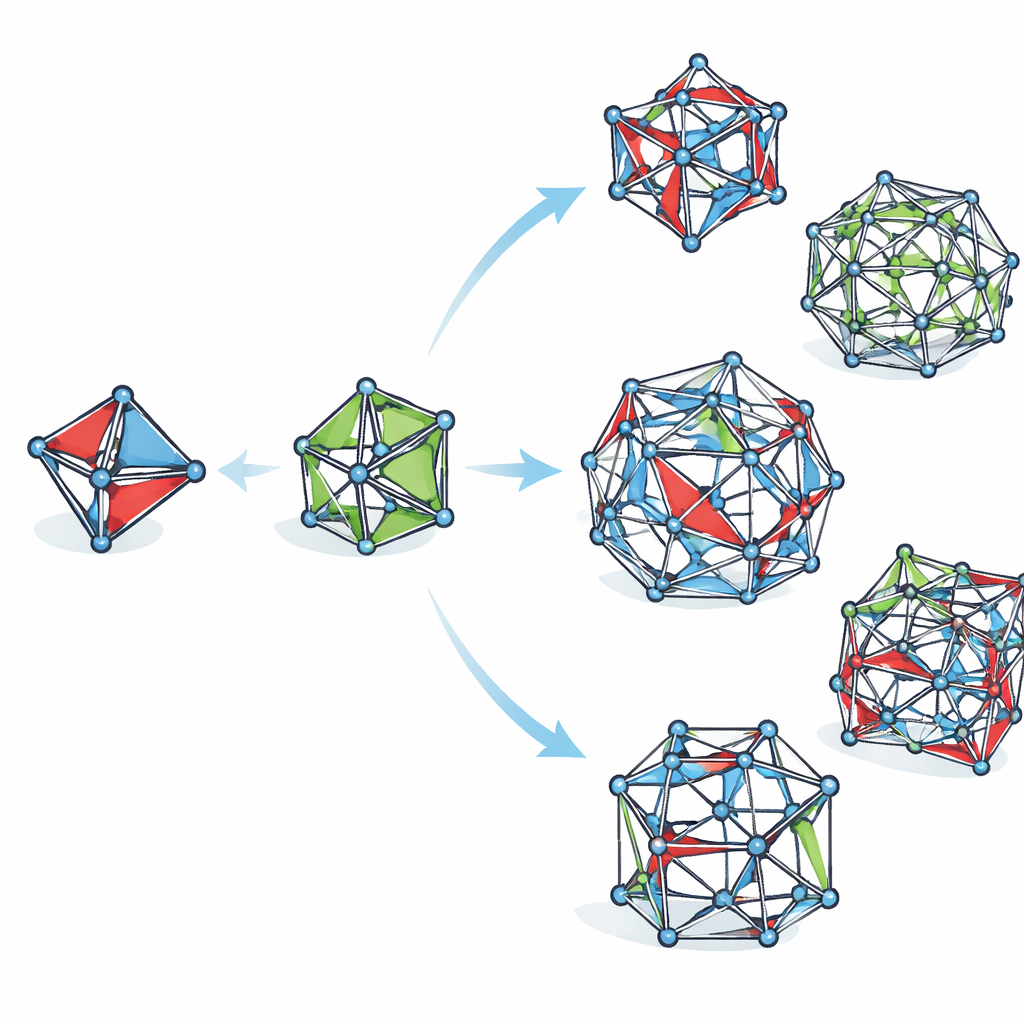
Van gewone dubbele bindingen naar gebogen bindingen
In bekende moleculen houdt een koolstof–koolstof dubbele binding de gebonden atomen in een vlakke opstelling, wat het delen van elektronen maximaliseert en de binding een sterkte geeft die overeenkomt met een "bindingsorde" van ongeveer twee. Chemici weten al lang dat deze geometrie kan worden vervormd als de dubbele binding gevangen zit in een kleine ring, waardoor de atomen uit het gebruikelijke vlak kantelen. Dit kantelen, pyramidalizatie genoemd, verzwakt een deel van de binding en duwt de bindingsorde onder twee. Tot nu toe waren zulke vervormde dubbele bindingen vooral curiositeiten, met slechts een paar praktische toepassingen.
Introductie van ultra‑gebogen kooi‑moleculen
De auteurs heronderzoeken twee opvallende maar verwaarloosde moleculen, cubeen en 1,7‑quadricycleen. Elk verbergt een dubbele binding binnen een stijve kooi van koolstofatomen, waardoor de binding in een extreem gebogen vorm wordt gedwongen die het team hyperpyramidalizatie noemt. Berekeningen tonen aan dat in deze kooien de hoeken rond de dubbele binding ver van normaal worden geduwd, en dat de elektronen die gewoonlijk een sterke "pi"-koppeling vormen, uit lijn raken en deels opnieuw gericht worden. Daardoor daalt de effectieve bindingsorde naar ongeveer 1,5, halverwege tussen een enkele en een dubbele binding, en wordt de binding zowel zwakker als reactiever dan in standaardmoleculen.
Praktische routes naar deze kooien opbouwen
Eerdere pogingen om cubeen en 1,7‑quadricycleen te maken vereisten harde omstandigheden en leverden beperkte opbrengsten. De onderzoekers ontwikkelen nu mildere, flexibeler routes met zogeheten Kobayashi‑type voorlopers. Deze voorlopers dragen een siliciumgroep naast een goede leaving group. Wanneer fluoride wordt toegevoegd, verschijnt de kooi‑achtige reactieve soort kortstondig en kan ter plekke door een ander molecuul worden gevangen. Deze strategie stelt het team in staat om beide typen kooien onder milde condities te genereren en ze onmiddellijk in reacties te vangen voordat ze uiteenvallen.
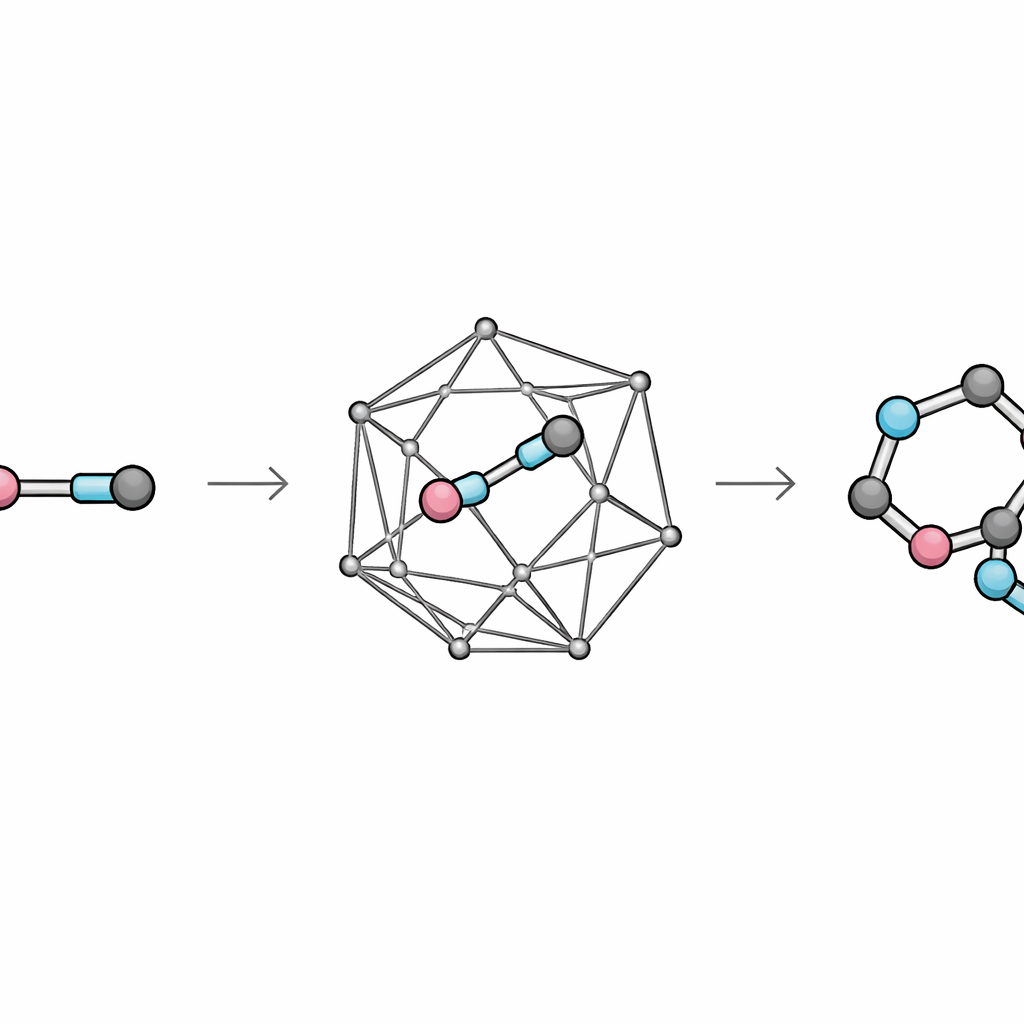
Kooien in elkaar klikken om complexe vormen te vormen
Zodra de reactieve kooien op aanvraag beschikbaar zijn, zet het team ze in als "verbinders" in bindingsvormende reacties die cycloaddities worden genoemd. In deze processen klikt de vervormde dubbele binding in de kooi samen met een partner, zoals een plat aromatisch ringstelsel of een kleine elektronenrijke ring, en vormt nieuwe gefuseerde kaders. Opmerkelijk is dat veel van de resulterende producten vier nieuwgevormde, dichte koolstofcentra in een rij bevatten, allemaal verankerd aan de stijve kooi. Door de vangpartners te variëren bouwen de chemici een reeks van vijf- en zesringige ringen gefuseerd op de kooien, evenals meer uitgewerkte bicycli en gebruggde systemen die op andere manieren zeer moeilijk te construeren zouden zijn.
Hoe vervorming de reactiviteit versterkt
Computersimulaties helpen verklaren waarom de gebogen dubbele bindingen zulke krachtige bouwstenen zijn. Wanneer de binding uit het vlak wordt geduwd, draaien en mengen de elektronenorbitalen op een manier die het pi‑gedeelte van de binding verzwakt en de energie ervan verhoogt. Tegelijkertijd is de hele kooi-structuur sterk gespannen, als een samengeperde veer. Wanneer de kooi reageert in een cycloadditie, wordt deze opgeslagen spanning vrijgegeven, waardoor de reactie sterk exotherm wordt en de barrière voor reactie lager ligt vergeleken met een normale vlakke dubbele binding. De auteurs tonen aan dat deze effecten samen maken dat cubeen en 1,7‑quadricycleen snel reageren met partners zoals antraceen om ingewikkelde producten te geven.
Waarom deze kleine kooien ertoe doen
De studie toont aan dat het opzettelijk buigen van een dubbele binding binnen een star kader geen loutere geometrische curiositeit is, maar een krachtig ontwerpprincipe. Hyperpyramidaliseerde bindingen fungeren als bestuurbare hotspots die dicht opeengepakte, driedimensionale vormen aan elkaar kunnen naaien, vol nabijgelegen koolstofatomen. Dergelijke structuren zijn aantrekkelijk in de medicinale chemie, waar compacte, verzadigde kaders kunnen verbeteren hoe kandidaat‑geneesmiddelen zich in het lichaam gedragen, en in toepassingen zoals opslag van zonne-energie die vertrouwen op gespannen moleculen. Door in kaart te brengen hoe vervorming de bindingsorde verlaagt en de reactiviteit verhoogt, wijst het werk de weg naar veel andere "veerbelaste" moleculen die chemici mogelijk kunnen ontwerpen en gebruiken als veelzijdige synthetische bouwstenen.
Bronvermelding: Ding, J., French, S.A., Rivera, C.A. et al. Hyperpyramidalized alkenes with bond orders near 1.5 as synthetic building blocks. Nat. Chem. 18, 913–922 (2026). https://doi.org/10.1038/s41557-025-02055-9
Trefwoorden: gespannen moleculen, hyperpyramidaliseerde alkenen, cubeen, 1,7‑quadricycleen, cycloadditiechemie