Clear Sky Science · de
Hyperpyramidalisierte Alkene mit Bindungsordnungen nahe 1,5 als synthetische Bausteine
Warum das Biegen von Bindungen im echten Leben wichtig sein kann
Chemiker lernen normalerweise, dass eine Doppelbindung zwischen zwei Kohlenstoffatomen eine flache, stabile Verbindung ist, ein wenig wie ein starrer Balken in einem Bauwerk. Dieser Artikel untersucht, was passiert, wenn dieser Balken in winzigen Kohlenstoffkäfigen zum Biegen und Ausbeulen gezwungen wird. Die Arbeit zeigt neue Arten von „vorspannenden“ Molekülen, deren eingebaute Spannung sie ungewöhnlich bereitwillig macht, sich mit anderen Bausteinen zusammenzuschließen. Das eröffnet frische Wege, kompakte, dreidimensionale Strukturen zu entwerfen, die in der Arzneimittelentwicklung und der Energieforschung nützlich sein könnten.
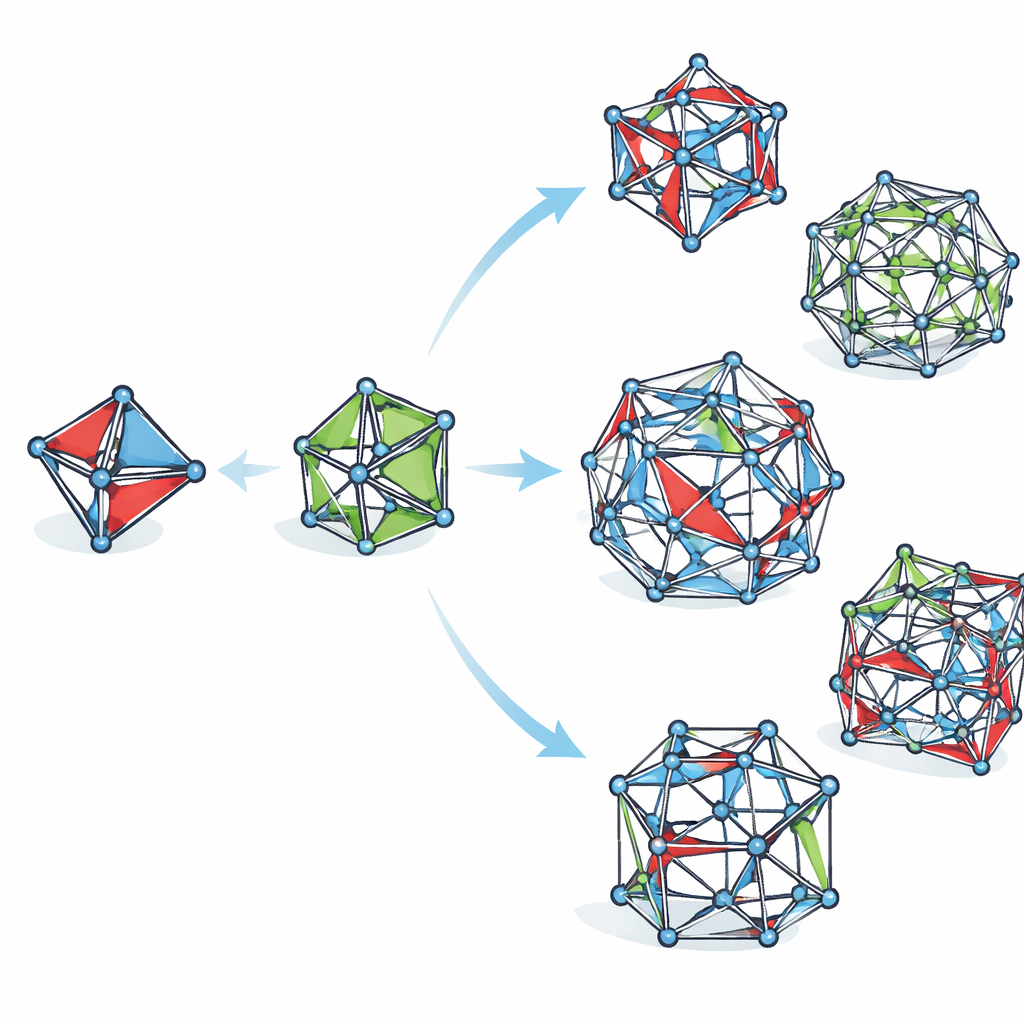
Von gewöhnlichen Doppelbindungen zu gekrümmten
In vertrauten Molekülen hält eine Kohlenstoff–Kohlenstoff-Doppelbindung die gebundenen Atome in einer flachen Anordnung, was die Elektronenteilung maximiert und der Bindung eine Stärke verleiht, die einer „Bindungsordnung“ von etwa zwei entspricht. Chemiker wissen seit langem, dass diese Geometrie verzerrt werden kann, wenn die Doppelbindung in einem kleinen Ring eingeschlossen ist und die Atome aus der üblichen Ebene kippen. Dieses Kippen, Pyramidalisation genannt, schwächt Teile der Bindung und drückt die Bindungsordnung unter zwei. Bislang waren derartige verzerrte Doppelbindungen meist Kuriositäten mit nur wenigen praktischen Anwendungen.
Vorstellung ultra-gekrümmter Käfigmoleküle
Die Autoren beleben zwei auffällige, aber vernachlässigte Moleküle neu, genannt Cubene und 1,7‑Quadricyclen. Jeweils verbergen sie eine Doppelbindung in einem starren Kohlenstoffkäfig und zwingen die Bindung in eine extrem gekrümmte Form, die das Team als Hyperpyramidalisation bezeichnet. Rechnungen zeigen, dass in diesen Käfigen die Winkel um die Doppelbindung stark aus der Norm gedrängt werden und die Elektronen, die sonst eine starke π‑Bindung bilden, fehl ausgerichtet und teilweise umorientiert werden. Infolgedessen sinkt die effektive Bindungsordnung auf etwa 1,5, also auf halbem Weg zwischen Einfach- und Doppelbindung, und die Bindung wird schwächer und reaktiver als in normalen Molekülen.
Praktische Zugänge zu diesen Käfigen aufbauen
Frühere Versuche, Cubene und 1,7‑Quadricyclen herzustellen, erforderten harte Bedingungen und lieferten nur begrenzte Ausbeuten. Die Forscher entwickeln nun schonendere, flexiblere Wege unter Verwendung sogenannter Kobayashi‑Typ‑Vorläufer. Diese Vorläufer tragen eine Siliziumgruppe neben einer guten Abgangsgruppe. Sobald Fluorid zugegeben wird, erscheint kurzzeitig die käfigartige reaktive Spezies und kann von einem anderen Molekül eingefangen werden. Diese Strategie erlaubt es dem Team, beide Arten von Käfigen unter milden Bedingungen zu generieren und sie sofort in Reaktionen zu fangen, bevor sie zerfallen.
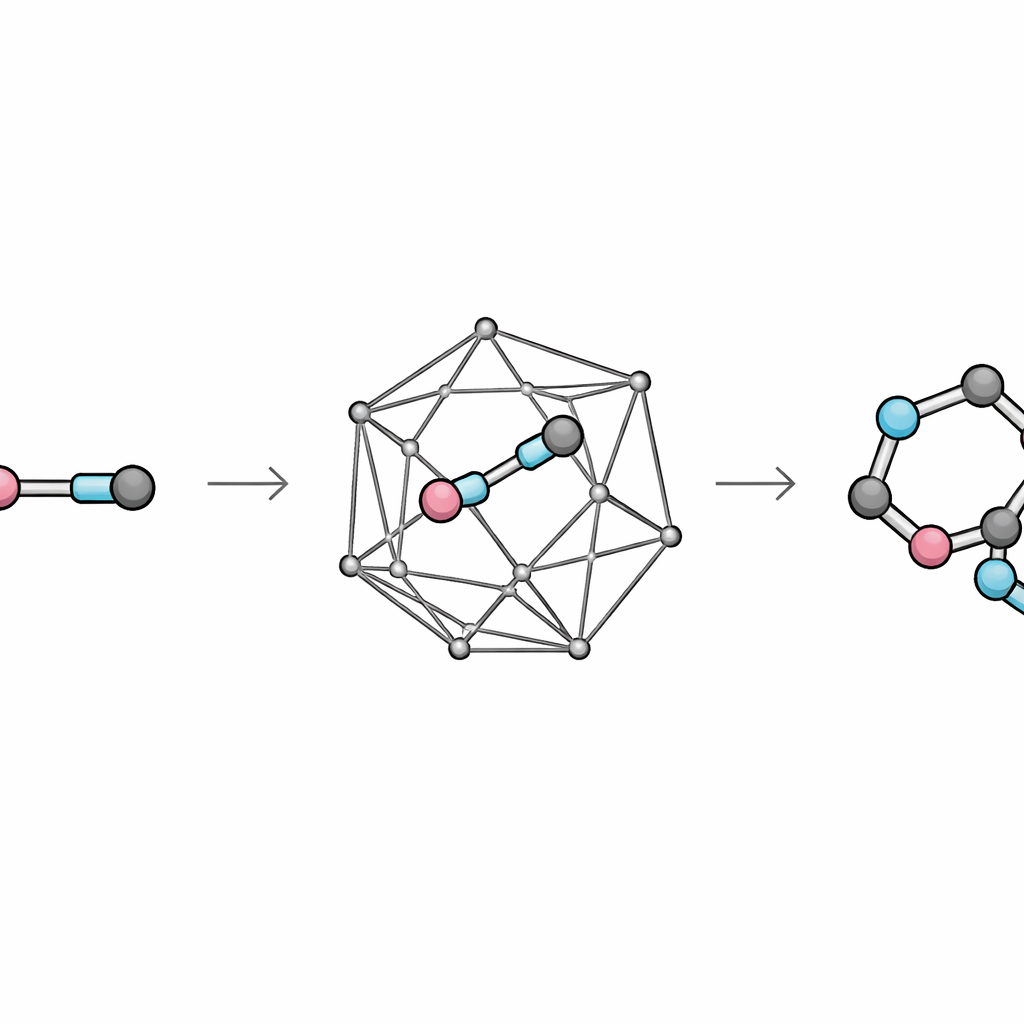
Käfige zusammenschnappen lassen, um komplexe Formen zu bilden
Sobald die reaktiven Käfige auf Abruf verfügbar sind, setzen die Forscher sie als „Verbindungsstücke“ in Bindungsbildungen namens Cycloadditionen ein. Bei diesen Prozessen schnappen die verzerrten Doppelbindungen im Käfig mit einem Partner wie einem flachen aromatischen Ring oder einem elektronendichten kleinen Ring zusammen und bilden neue verschmolzene Gerüste. Bemerkenswerterweise enthalten viele der entstehenden Produkte vier neu gebildete, beengte Kohlenstoffzentren in Folge, alle am starren Käfig verankert. Durch Variation der Fängermoleküle bauen die Chemiker eine Auswahl an fünf‑ und sechsgliedrigen Ringen auf den Käfigen auf sowie komplexere Bicycle und Brückensysteme, die sich auf anderem Wege nur schwer herstellen ließen.
Wie Verzerrung die Reaktivität steigert
Computersimulationen helfen zu erklären, warum die gekrümmten Doppelbindungen so potente Bausteine sind. Wenn die Bindung aus der Ebene gedrängt wird, verdrehen und mischen sich ihre Elektronenorbitale so, dass der π‑Anteil der Bindung geschwächt und energetisch angehoben wird. Gleichzeitig ist die gesamte Käfigstruktur stark gespannt, ähnlich einer komprimierten Feder. Wenn der Käfig in einer Cycloaddition reagiert, wird diese gespeicherte Spannung freigesetzt, wodurch die Reaktion stark energieabgebend wird und die Aktivierungsbarriere im Vergleich zu einer normalen flachen Doppelbindung sinkt. Die Autoren zeigen, dass diese Effekte zusammen dazu führen, dass Cubene und 1,7‑Quadricyclen rasch mit Partnern wie Anthracen reagieren und komplexe Produkte liefern.
Warum diese winzigen Käfige wichtig sind
Die Studie demonstriert, dass das gezielte Biegen einer Doppelbindung in einem starren Gerüst nicht nur eine geometrische Kuriosität ist, sondern ein kraftvolles Gestaltungsprinzip. Hyperpyramidalisierte Bindungen fungieren als steuerbare Hotspots, die dichte, dreidimensionale Formen aus eng gepackten Kohlenstoffatomen zusammenheften können. Solche Formen sind in der medizinischen Chemie attraktiv, wo kompakte, gesättigte Gerüste das Verhalten von Wirkstoffkandidaten im Körper verbessern können, und in Bereichen wie der solarenergetischen Speicherung, die auf gespannte Moleküle angewiesen sind. Indem gezeigt wird, wie Verzerrung die Bindungsordnung senkt und die Reaktivität erhöht, weist die Arbeit den Weg zu vielen weiteren „vorspannenden“ Molekülen, die Chemiker als vielseitige synthetische Bausteine entwerfen und nutzen könnten.
Zitation: Ding, J., French, S.A., Rivera, C.A. et al. Hyperpyramidalized alkenes with bond orders near 1.5 as synthetic building blocks. Nat. Chem. 18, 913–922 (2026). https://doi.org/10.1038/s41557-025-02055-9
Schlüsselwörter: gespannte Moleküle, hyperpyramidalisierte Alkene, Cubene, Quadricyclen, Cycloadditionschemie