Clear Sky Science · nl
Duale deconvolutie in multiphoton-gestructureerde-illuminatie-microscopie voor superresolutiebeelden in diep weefsel
Dieper kijken in levend weefsel
De moderne biologie is vaak afhankelijk van het zien van de kleinste details in dikke weefselstukken, zoals hersenplakjes of ontwikkelende embryo’s. Helaas wordt licht dat door zulke drukke omgevingen reist afgebogen en verstoord, waardoor beelden wazig worden precies wanneer onderzoekers scherpe waarnemingen het meest nodig hebben. Dit artikel introduceert een manier om die beelden digitaal te "ontvlekken", zodat een standaard geavanceerde microscoop uiterst fijne structuren diep in weefsel kan onthullen zonder dure, complexe hardware toe te voegen.
Waarom diep beeldvorming zo moeilijk is
Fluorescentiemicroscopen maken het mogelijk om specifieke moleculen te labelen en te observeren hoe cellen en weefsels zijn opgebouwd en zich gedragen. In de afgelopen decennia hebben verschillende "superresolutie"-methoden de traditionele scherptegrenzen doorbroken en details onthuld ver beneden 200 nanometer. De meeste van deze methoden werken echter alleen goed dicht bij het monsteroppervlak. In dikke weefsels, zoals muizenhersenen, worden zowel het licht dat fluorescentielabels exciteert als het licht dat terug naar de detector wordt uitgezonden, vervormd door kleine variaties in de weefselstructuur. Deze vervormingen, aberraties genoemd, vervagen de scherpte van de microscoop en wissen hoge-resolutie-informatie, vooral op dieptes groter dan enkele tientallen micrometers.
Van hardwareoplossingen naar een softwareaanpak
Een gangbare manier om aberraties tegen te gaan is adaptieve optiek in hardware, waarbij beweegbare spiegels of andere elementen het lichtgolffront hervormen om de focus te herstellen. Hoewel krachtig, zijn deze systemen duur, technisch veeleisend en corrigeren ze vaak alleen vervormingen voor één kleur of één richting van licht tegelijk. De auteurs stellen daarentegen een computationele aanpak voor die werkt met een type microscoop dat al in veel laboratoria staat: een laser‑scannende multiphotonmicroscoop. Door de gebruikelijke enkele detector te vervangen door een camera, nemen ze een rijke stapel gescande beelden op die coderen hoe zowel het inkomende excitatie licht als de uitgaande fluorescentie door het weefsel zijn vervormd.
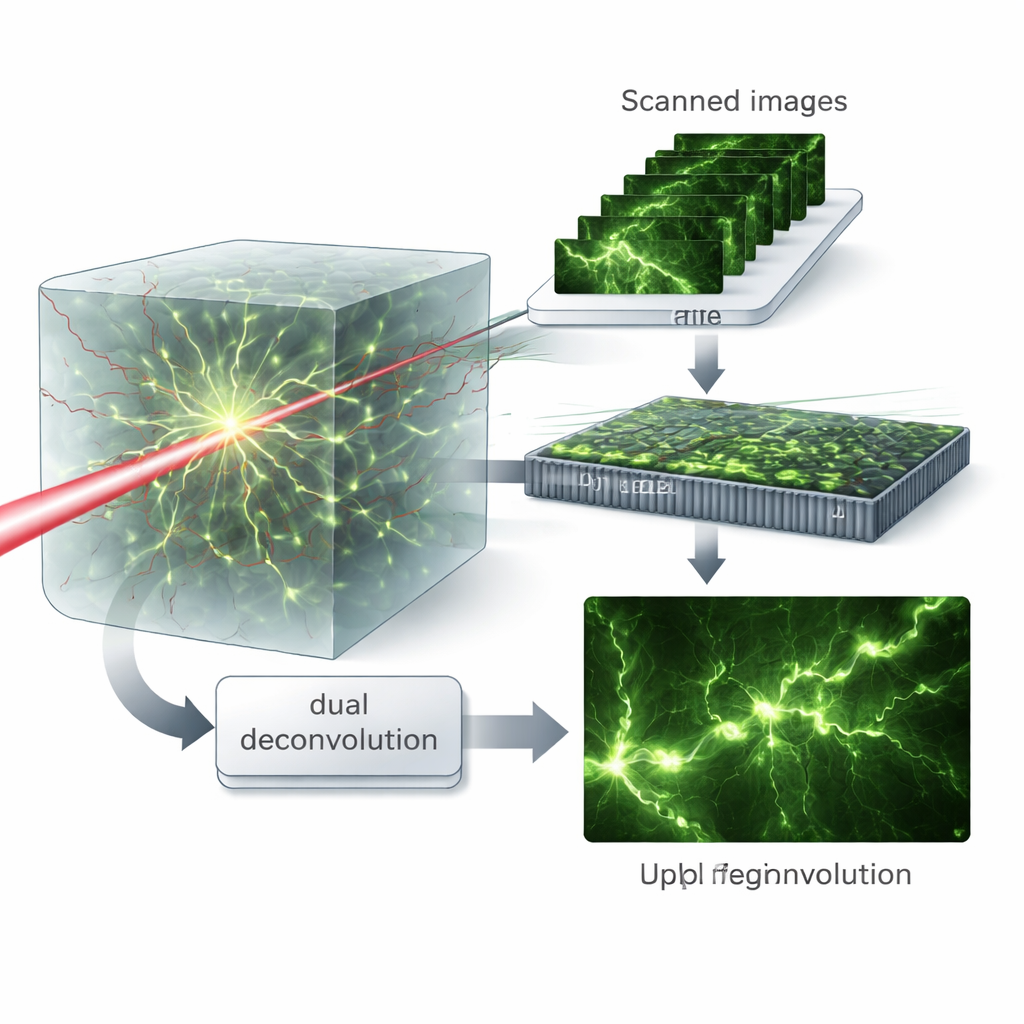
Virtuele patronen en dubbele opschoning
De kerninzichten is om de gescande beelden te behandelen alsof het monster was belicht met veel verschillende fijne lichtpatronen, een concept dat de auteurs virtuele gestructureerde illuminatie noemen. Door deze gegevens wiskundig te hercombineren in het frequentiedomein kunnen ze de rollen van excitatie- en emissieprocessen scheiden. Vervolgens introduceren ze een "duale deconvolutie"-algoritme dat afwisselend de vervaging aan iedere kant schat en corrigeert — het licht dat naar binnen gaat en het licht dat naar buiten komt — in plaats van ze samen te voegen tot één enkele effectieve vervaging. Deze matrixgebaseerde behandeling behoudt meer hoogfrequente details en stelt het algoritme in staat fijne structuren te herstellen, zelfs wanneer aberraties sterk zijn.
Schermere beelden in simulaties en echte monsters
Om hun methode te testen gebruikte het team eerst computersimulaties van twee‑fotonmicroscopie, een diepbeeldvormingstechniek die paartjes van lagere-energie fotonen gebruikt om fluorescentie alleen in het focuspunt te excitere n. Onder zwaar gesimuleerde vervormingen leverden conventionele twee‑foton- en standaard gestructureerde-illuminatie-reconstructies merkbaar vage beelden op. In contrast herstelde duale deconvolutie scherpe patronen met een resolutie die dicht in de buurt kwam van een kwart van de fluorescente golflengte — ongeveer 130 nanometer — wat overeenkomt met theoretische verwachtingen. De auteurs bouwden vervolgens een aangepaste twee‑fotonopstelling met een wetenschappelijke camera en pasten hun algoritme toe op echte monsters, waaronder fluorescerende parels, testpatronen verborgen achter verstrooiende lagen, gekweekte cellen, muizenhersweefsel en volledige zebravispreparaten. Steeds weer toonden structuren die in conventionele beelden vervormd of gedubbeld leken, na verwerking duidelijk gescheiden kenmerken, en fijne neuronale elementen zoals dendritische stekels bleven resolvabel tot dieptes tot 180 micrometer in muizenhersenen.
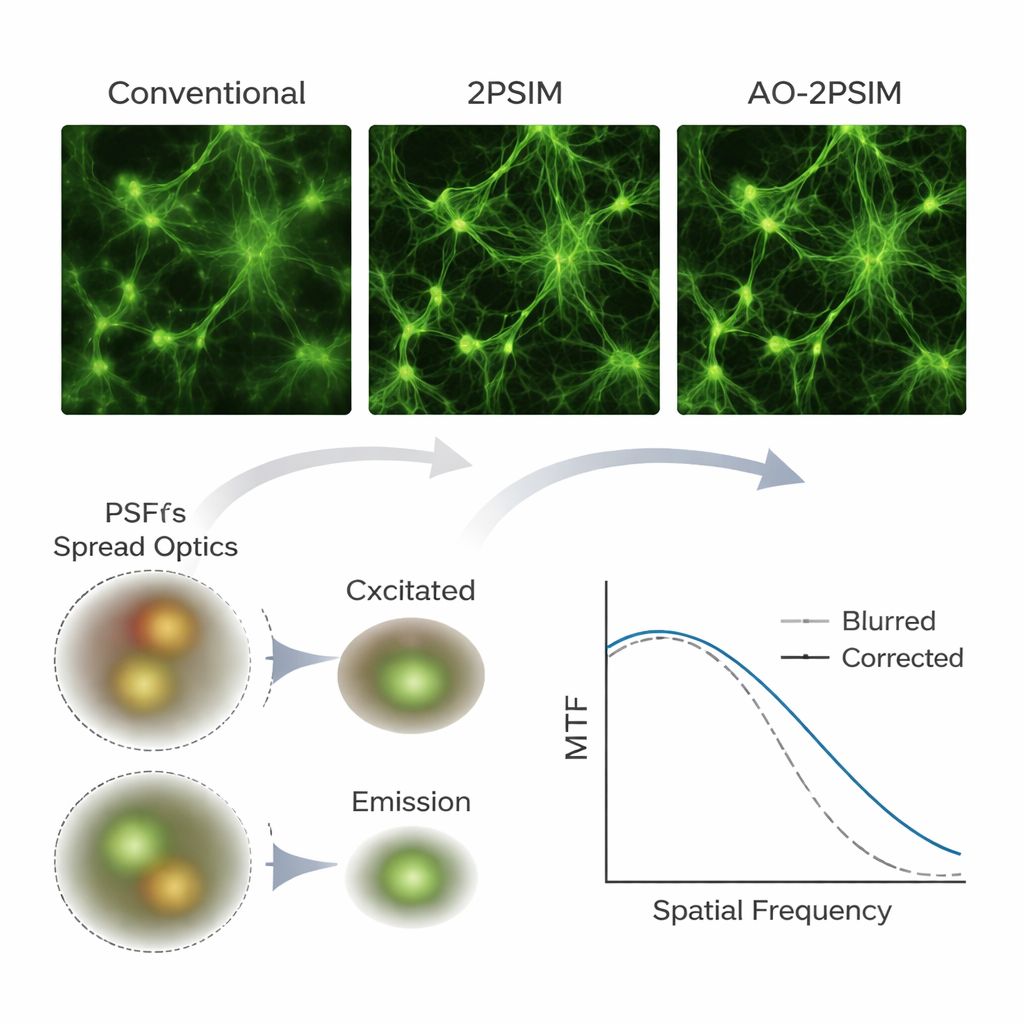
Wat dit betekent voor biologische beeldvorming
Voor niet‑specialisten is de kernboodschap dat de auteurs hebben laten zien hoe bestaande multiphotonmicroscopen met voornamelijk software en een camera‑upgrade veel krachtigere hulpmiddelen voor diepweefselbeeldvorming kunnen worden. Door zorgvuldig te modelleren en te corrigeren hoe weefsels licht zowel op de heen- als terugweg buigen, verdubbelt hun duale deconvolutie‑aanpak de gebruikelijke resolutielimiet in veeleisende, dikke monsters zonder te vertrouwen op complexe adaptieve spiegels. Hoewel de methode nog steeds afhankelijk is van voldoende signaal en momenteel relatief langzaam scannen vereist, biedt ze een praktische, kosteneffectieve route naar routinematige, uiterst scherpe driedimensionale beelden van de hersenen en andere organen, en opent ze de deur naar gedetailleerdere studies naar hoe biologische structuren zijn georganiseerd en veranderen in de tijd.
Bronvermelding: Lim, S., Kang, S., Hong, J.H. et al. Dual deconvolution in multiphoton structured illumination microscopy for deep-tissue super-resolution imaging. Nat Commun 17, 2123 (2026). https://doi.org/10.1038/s41467-026-69798-y
Trefwoorden: superresolutiemicroscopie, twee-foton imaging, adaptieve optiek, diepweefselimaging, computationele beeldvorming