Clear Sky Science · nl
Chemogenetische modulatie van de baan van de prelimbische cortex naar de nucleus accumbens core vermindert door cocaïne veroorzaakte toename van risicovoorkeur
Waarom risicovolle keuzes ertoe doen
Waarom glijden sommige individuen in risicovolle gewoonten zoals intens drugsgebruik of problematisch gokken, terwijl anderen er vanaf blijven, zelfs bij dezelfde verleidingen? Deze studie gebruikt ratten om die vraag te onderzoeken, met de focus op hoe een specifieke hersenbaan risicovol beslissen vormgeeft na blootstelling aan cocaïne en hoe het terugschakelen van die baan keuzes weer richting veiligere opties kan duwen. 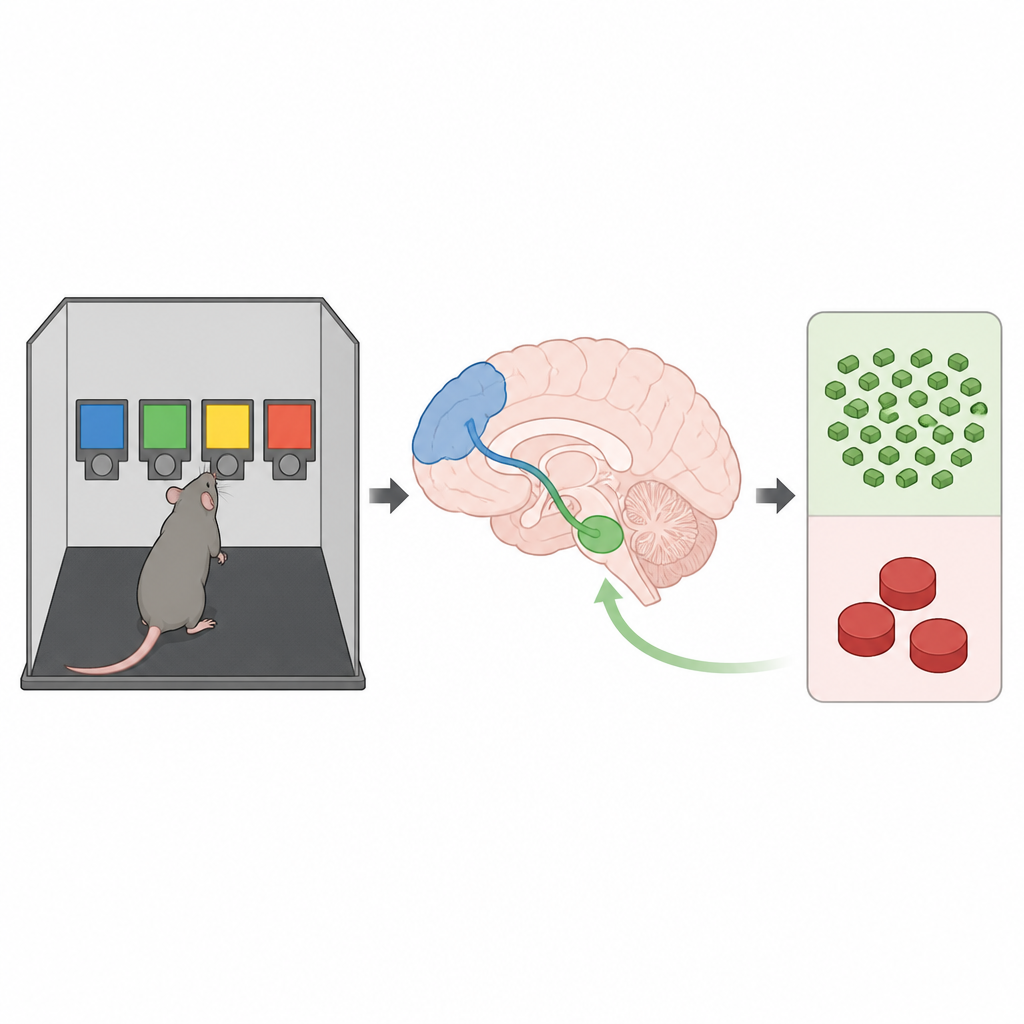
Een gokspel voor ratten
Om keuzes uit de echte wereld na te bootsen, gebruikten de onderzoekers een ratten-goktaak die mensen in casino-achtige beslissingen weerspiegelt. Ratten kozen uit vier opties, die elk verschillende aantallen zoete pellets en verschillende kansen op een time-outstraf boden. Eén optie gaf op de lange termijn de beste opbrengst en telde als de “veilige” maar nog steeds belonende keuze, terwijl de andere opties op korte termijn verleidelijker waren maar op lange termijn slechter. Op basis van hoe sterk ratten de beste optie preferentiëerden, werden ze voor elke drugsblootstelling ingedeeld als risicomijdend of risicogericht.
Cocaïne kantelt de balans
Na deze basislijnmeting kregen sommige ratten een week lang cocainetoedieningen en werden ze later opnieuw uitgedaagd met cocaïne vlak voor de goktaak. Bij eerder risicomijdende ratten duwde cocaïne de keuzes weg van de op lange termijn beste optie richting grotere maar risicovollere beloningen, wat weerklank vindt met hoe stimulerend middelengebruik bij mensen slechte beslissingen kan bevorderen. Interessant genoeg veranderden ratten die al risicogericht waren weinig door cocaïne, wat suggereert dat hun beslissingsstijl meer vastligt. De onderzoekers volgden ook aandachtsgerelateerde maatstaven, zoals hoe vaak een rat niet reageerde, en vonden dat cocaïne deze lapsen vergrootte.
Een sleutelbaan stilleggen
De studie zoomde in op een baan die de prelimbische cortex verbindt — een deel van de frontale hersenen betrokken bij plannen en controle — met de nucleus accumbens core, een beloningshub die helpt kosten en baten af te wegen. Met behulp van chemogenetica, een methode waarmee wetenschappers specifieke neuronen met een designerdrugs kunnen dempen of activeren, dempten of versterkten ze selectief de activiteit in deze baan. Het activeren van de remmende “Gi”-schakelaar in prelimbische neuronen die naar de nucleus accumbens projecteren, verminderde bij risicomijdende ratten de door cocaïne veroorzaakte toename van risicovolle keuzes en verlaagde hun aandachtsfalen. Daarentegen corrigeerde het activeren van een exciterende “Gq”-schakelaar, die dit circuit juist verder opjaagt, de cocaïnegedreven verschuiving naar risico niet. Bij ratten die nooit cocaïne kregen, had het manipuleren van dezelfde baan weinig effect op de basale keuzepatronen, wat suggereert dat de interventie vooral samenhangt met door drugs gewijzigde hersenstaten. 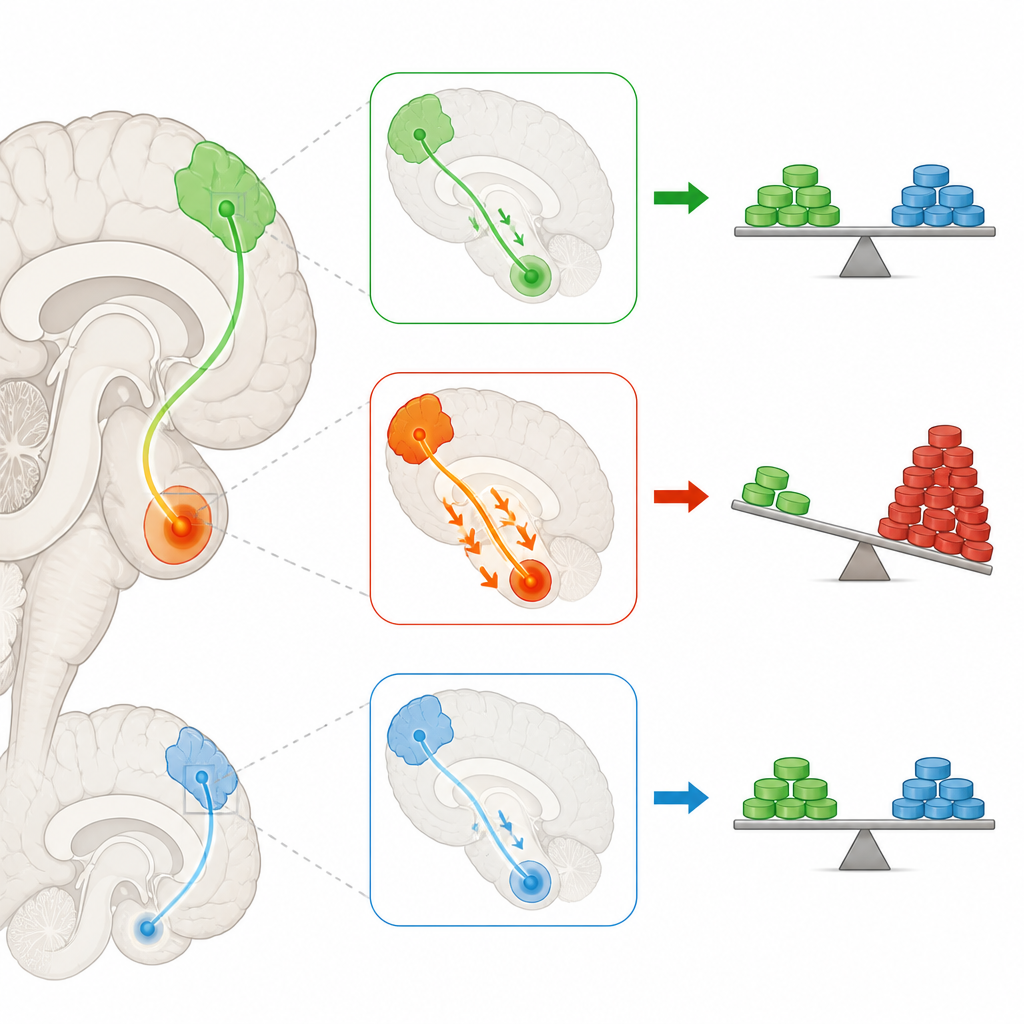
Veranderingen binnen de cellen
De onderzoekers onderzochten ook moleculaire veranderingen in prelimbische neuronen. Cocaïne verhoogde de niveaus van een specifiek calciumkanaaleiwit, CaV1.2, in risicomijdende ratten; dit eiwit beïnvloedt hoe snel hersencircuits door middelen gesensibiliseerd raken. Het veranderde ook de balans van een signaalmolecuul genaamd DARPP-32, waarbij een specifieke fosfaatkenmerkverschuiving ontstond die normaal gezien bij van nature risicogerichte ratten voorkomt. Wanneer de remmende Gi-schakelaar in de baan werd ingeschakeld, keerden zowel CaV1.2-niveaus als het veranderde DARPP-32-signaal terug richting de basislijn bij risicomijdende ratten. Bovendien hield in deze dieren de mate van DARPP-32-verschuiving verband met hoe vaak ze de veilige optie kozen, waarmee het moleculaire kenmerk aan daadwerkelijk gedrag gekoppeld werd. Deze effecten werden niet gezien bij risicogerichte ratten, wat benadrukt dat hun hersenen mogelijk al in een andere, stabiele toestand verkeren.
Wat dit voor mensen betekent
Samengevoegd suggereren de bevindingen dat een specifieke frontale-naar-beloning hersenbaan bijgestuurd kan worden om de door cocaïne veroorzaakte toename van risicovol beslissen en aandachtsproblemen tegen te gaan, maar vooral bij individuen die aanvankelijk voorzichtiger zijn. Door gedrag te koppelen aan precieze circuitactiviteit en moleculaire markers biedt het werk aanwijzingen waarom sommige mensen met middelen- of gokproblemen beter op bepaalde behandelingen reageren dan anderen. Hoewel chemogenetische schakelaars momenteel geen therapie voor mensen zijn, is het principe duidelijk: het richten op het juiste circuit, in de juiste subgroep, op het juiste moment kan helpen om meer evenwichtige keuzes te herstellen na drugsblootstelling.
Bronvermelding: Han, J., Kwak, M.J., Kim, W.Y. et al. Chemogenetic modulation of the prelimbic cortex to the nucleus accumbens core pathway reduces cocaine-induced increase of risk preference. Transl Psychiatry 16, 245 (2026). https://doi.org/10.1038/s41398-026-04015-4
Trefwoorden: risicovol beslissen, cocaïne, prefrontale cortex, nucleus accumbens, gokgedrag