Clear Sky Science · nl
Knockdown van Ddx3x in mPFC veroorzaakt autistische-achtige fenotypes bij muizen via veranderde synaptische plasticiteit
Wanneer een gen gedragsverandering veroorzaakt
Waarom leiden sommige genetische veranderingen tot verschillen in sociaal gedrag, leren en zintuiglijke reacties die we autisme noemen? Deze studie zoomt in op één zo’n gen, DDX3X, en stelt een eenvoudige maar krachtige vraag: wat gebeurt er in de hersenen wanneer dit gen niet goed werkt? Door hersencellen in kweek en zorgvuldig geconstrueerde muismodellen te bestuderen, volgen de onderzoekers het parcours van een klein moleculair defect naar veranderingen in de hersenbedrading en, uiteindelijk, naar autistische-achtige gedragingen.
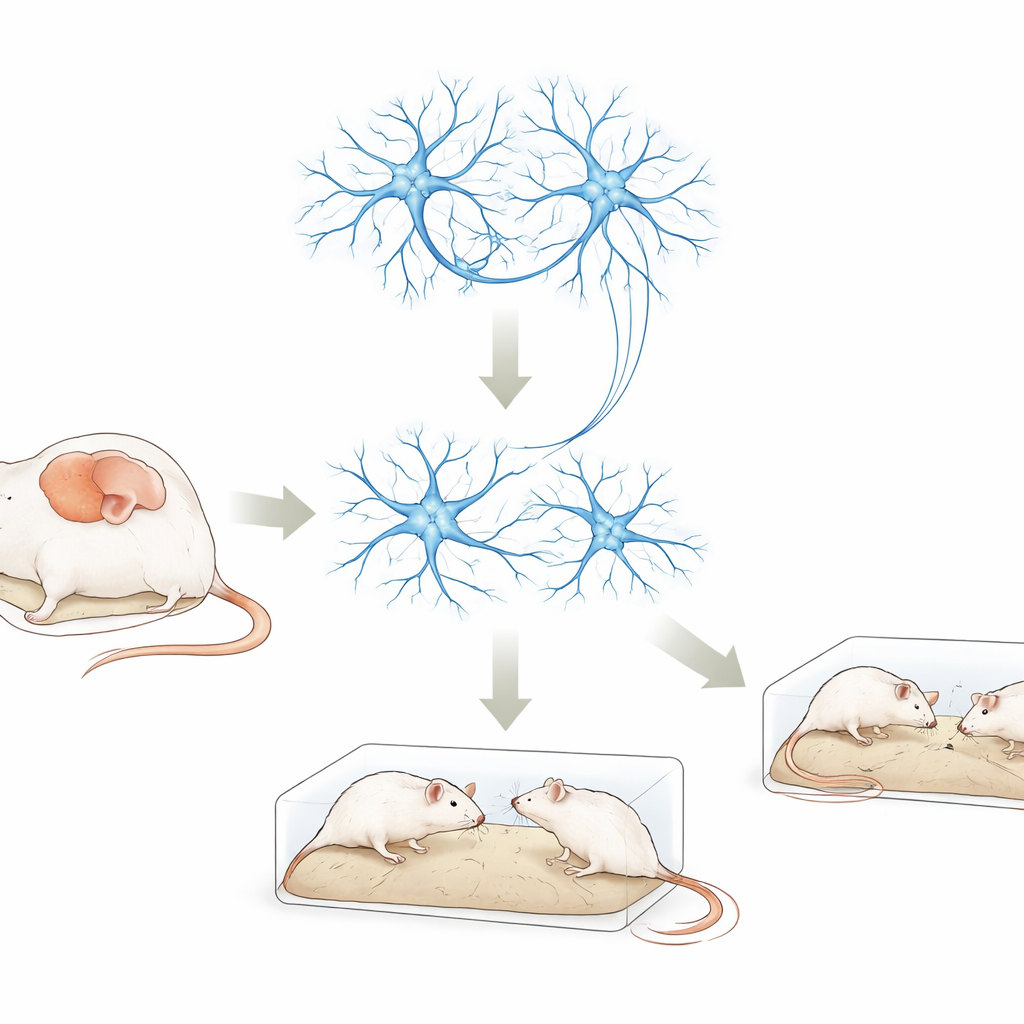
Een sleutergen van de hersenen onder de loep
DDX3X is een gen dat cellen helpt bij de verwerking van RNA, de actieve kopie van onze genetische code die gebruikt wordt om eiwitten te maken. Variaties in DDX3X worden steeds vaker gevonden bij mensen met autisme, verstandelijke beperking en ontwikkelingsachterstand. Het was echter onduidelijk hoe deze veranderingen de hersenfunctie verstoren. In dit werk verminderden wetenschappers de activiteit van de muisvariant van het gen, Ddx3x, in twee omstandigheden: in gekweekte zenuwachtige cellen en in een specifiek gebied van levende muizenhersenen, de mediale prefrontale cortex. Dit gebied speelt een belangrijke rol bij sociale interactie, besluitvorming en geheugen—vaardigheden die bij autisme vaak zijn aangetast.
Van langzamer groeiende cellen naar sociaal gedrag bij muizen
Toen het team het Ddx3x-niveau verlaagde in in het laboratorium gekweekte zenuwachtige cellen, groeiden de cellen langzamer en vormden ze minder makkelijk verbindingen dan normale cellen. Bij muizen gebruikten ze een onschadelijk virus als afleveringsmiddel om Ddx3x alleen in neuronen van de mediale prefrontale cortex te verlagen. Deze muizen werden vervolgens aan een reeks gedragsproeven onderworpen. In vergelijking met controledieren bewogen de muizen met Ddx3x-knockdown normaal en waren ze in een open veld niet opvallend angstig, maar ze toonden minder interesse in een onbekende muis, waren minder aangetrokken tot een nieuwe sociale partner en presteerden slechter in een geheugenzware doolhoftest wanneer de wachttijd langer was. Ze vertoonden ook meer repetitief graaf- en begrafingsgedrag—parallel aan twee kernkenmerken van autisme: sociale problemen en herhalende routines.
Verborgen verschuivingen in het eiwitlandschap van de hersenen
Om te zien wat er binnenin cellen veranderde, voerden de onderzoekers grootschalige eiwitanalyses uit zowel in de gekweekte cellen als in de mediale prefrontale cortex van muizen. Ze vonden honderden eiwitten waarvan de niveaus verschilden wanneer Ddx3x werd verlaagd. Veel van de meest getroffen eiwitten waren betrokken bij hoe synapsen—de aansluitpunten waar zenuwcellen communiceren—zich aanpassen en sterker worden in de loop van de tijd, een eigenschap die synaptische plasticiteit genoemd wordt. Pathways die gekoppeld zijn aan leren-gerelateerde versterking van verbindingen, chemische signalering door glutamaat en GABA (de belangrijkste exciterende en remmende signalen in de hersenen), en hormoon- en energiemetabolisme lieten allemaal tekenen van onderdrukking zien. Zowel in cellen als in hersenweefsel zagen ze ook overlappende verstoringen in systemen die nieuwe eiwitten correct vouwen en versleten eiwitten markeren voor verwijdering, wat wijst op een brede verstoring van eiwitkwaliteitscontrole.
Verzwakte verbindingen tussen zenuwcellen
Door nauwkeuriger naar de structuur van synapsen te kijken, gebruikten de onderzoekers microscopie met hoge resolutie om neuronen in het getroffen hersengebied te onderzoeken. Ze ontdekten dat muizen met verlaagd Ddx3x minder dendritische stekels hadden—de kleine uitstulpingen op vertakkingen van zenuwcellen waar exciterende synapsen zitten—met name de rijpe, paddenstoelvormige stekels die cruciaal zijn voor stabiele, sterke verbindingen. De postsynaptische dichtheid, een eiwitrijke zone die receptoren en signaalmoleculen ankert, was dunner en kleiner. Elektrische opnames van hersensneden toonden aan dat exciterende signalen minder vaak binnenkwamen, hoewel hun individuele sterkte ongewijzigd was. Samen wijzen deze bevindingen op een hersennetwerk dat is bedraad met minder en zwakkere communicatiepunten, in plaats van een netwerk dat volledig stil is.
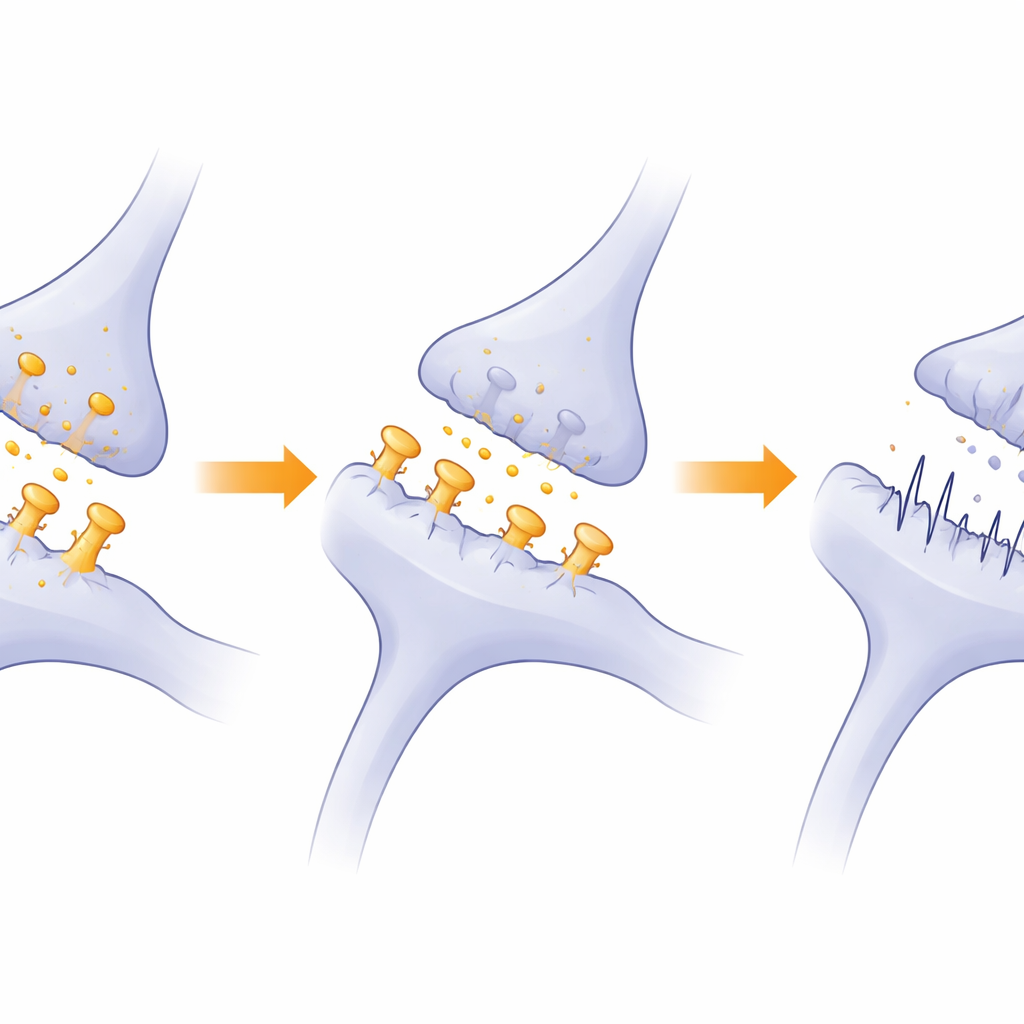
Hoe verstoorde eiwitbalans autistische kenmerken kan aanwakkeren
Voorbij individuele synapsen benadrukt de studie een dieperliggend probleem: de machinerie die synaptische eiwitten in balans houdt lijkt onderdrukt te worden wanneer Ddx3x laag is. Systemen die verse eiwitten vouwen en systemen die beschadigde eiwitten afbreken—met name het ubiquitine–proteasoompad—waren minder actief. Omdat synapsen afhankelijk zijn van voortdurende vernieuwing en fijnregeling van hun eiwitcomponenten, kan deze vertraging geleidelijk de synaptische sterkte en flexibiliteit aantasten. De auteurs stellen voor dat deze combinatie van minder rijpe stekels, verzwakte signalering en aangetaste eiwithuishouding in de mediale prefrontale cortex helpt de sociale en cognitieve veranderingen bij hun muizen te verklaren. In eenvoudige bewoordingen: wanneer DDX3X hapert, kunnen hersencircuits die sociaal gedrag en leren ondersteunen de benodigde verbindingen niet goed opbouwen of onderhouden, waardoor de ontwikkeling richting een autistische-achtige route wordt geduwd.
Bronvermelding: Zhuang, H., Cao, X., Tang, X. et al. Knockdown of Ddx3x in mPFC induces autistic-like phenotype in mice via altered synaptic plasticity. Transl Psychiatry 16, 216 (2026). https://doi.org/10.1038/s41398-026-03945-3
Trefwoorden: DDX3X, autismespectrumstoornis, synaptische plasticiteit, mediale prefrontale cortex, ubiquitine-proteasoomsysteem