Clear Sky Science · nl
Brandstof voor vernieuwing: door de ontwikkelingsnis versterkte ApoEVs ontsluiten bij volwassenen hiërarchisch weefselregeneratiepotentieel via mitochondriaal complex I-gedreven ontwikkelingsmetabool profiel
Waarom het herbouwen van volwassen weefsels zo moeilijk is
Veel organen in ons lichaam bestaan uit meerdere nauw gecoördineerde lagen, als een gelaagde taart. Zodra we volgroeid zijn, blijken deze gelaagde structuren verrassend slecht in staat zichzelf te herstellen na ernstige schade. Deze studie stelt een gedurfde vraag: in plaats van te proberen volwassen weefsels te repareren zoals ze zijn, kunnen we ze kortstondig terugschakelen naar een meer jeugdige, ontwikkelingsachtige toestand zodat ze zich goed kunnen herbouwen? Met de weefsels die tanden ondersteunen als model, presenteren de onderzoekers een nieuwe manier om volwassen cellen te "voeden" met ontwikkelingssignalen verpakt in kleine natuurlijke deeltjes.
Hoe jonge tanden een perfect ondersteuningssysteem bouwen
Tijdens de jeugd vormen de weefsels die een tand op zijn plaats houden zich op een zeer georkestreerde manier. Bot, ligament en een dun minerale laag op de wortel groeien samen en vergrendelen, waardoor de tand stabiliteit en veerkracht krijgt. Het team vergeleek deze ontwikkelende situatie met die van herstel bij volwassenen. In jong weefsel vonden ze een kalme, anti-inflammatoire omgeving gevormd door een speciaal type immuuncel, een M2-achtig macrofaag. Deze cellen helpen een ondersteunende "nis" rondom stamcellen te creëren, wat sterke energieconsumptie, gezonde mitochondriën en een voorkeur voor efficiënte zuurstofgebaseerde stofwisseling bevordert. Bij volwassenen daarentegen is de omgeving meer geïnflammeerd, zijn stamcellen schaars en trager, en groeit de fijn gelaagde structuur meestal niet terug.
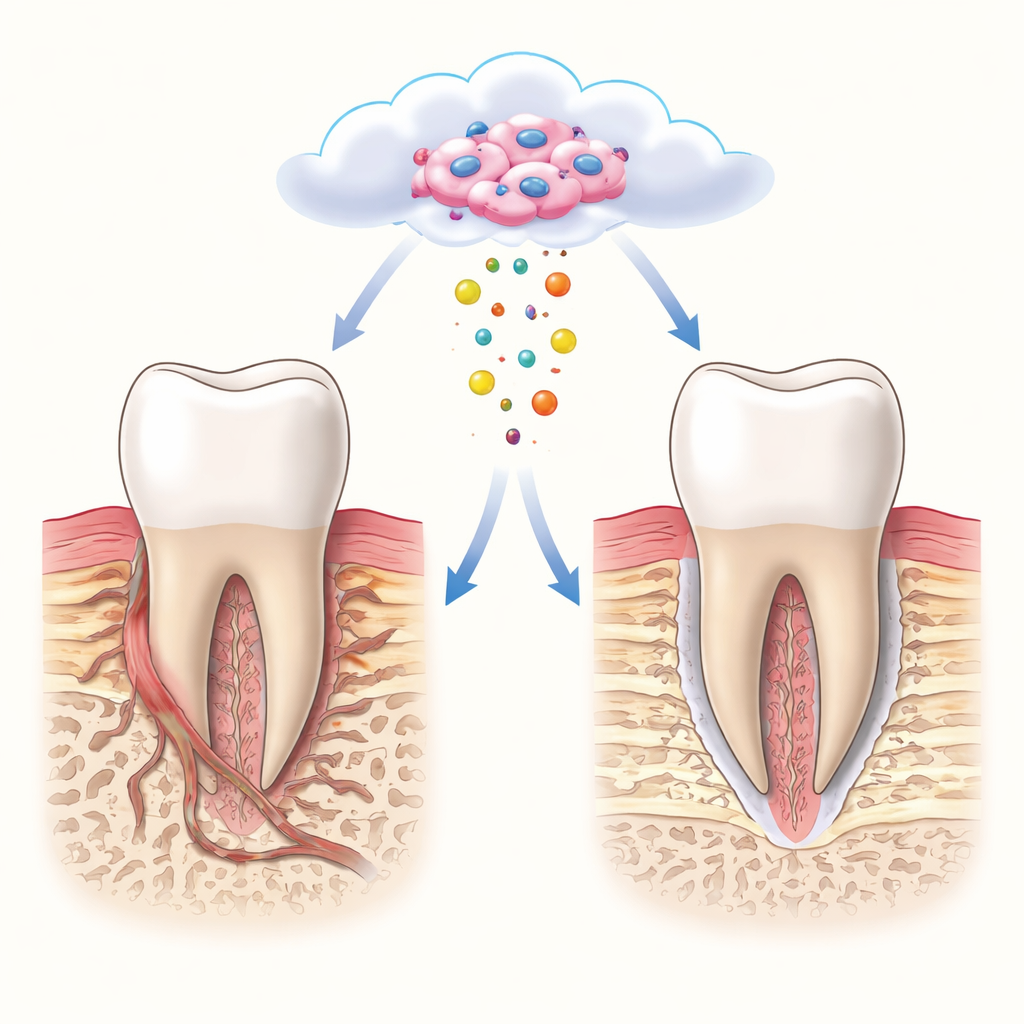
Lenen van het natuurlijke opruimsysteem
Wanneer getransplanteerde stamcellen in beschadigd weefsel worden geplaatst, sterven de meesten binnen enkele dagen. In plaats van dit als een mislukking te zien, suggereert recent werk dat de stervende cellen toch kunnen helpen door kleine membraan-omhulde deeltjes af te geven, apoptotische extracellulaire vesicles genoemd. Deze deeltjes dragen eiwitten en andere moleculen van hun oudercellen en kunnen naburige cellen beïnvloeden zonder de risico's van het transplanteren van hele cellen. De auteurs redeneerden dat als ze eerst stamcellen uit het tandligament aan een ontwikkelingsachtige nis zouden blootstellen en vervolgens hun gecontroleerde celdood zouden opwekken, de resulterende vesicles zowel de stamcelkenmerken als hun jeugdige omgeving zouden "onthouden". Ze noemden deze op maat gemaakte deeltjes DevNiche-ApoEVs.
Volwassen cellen opladen via mitochondriën
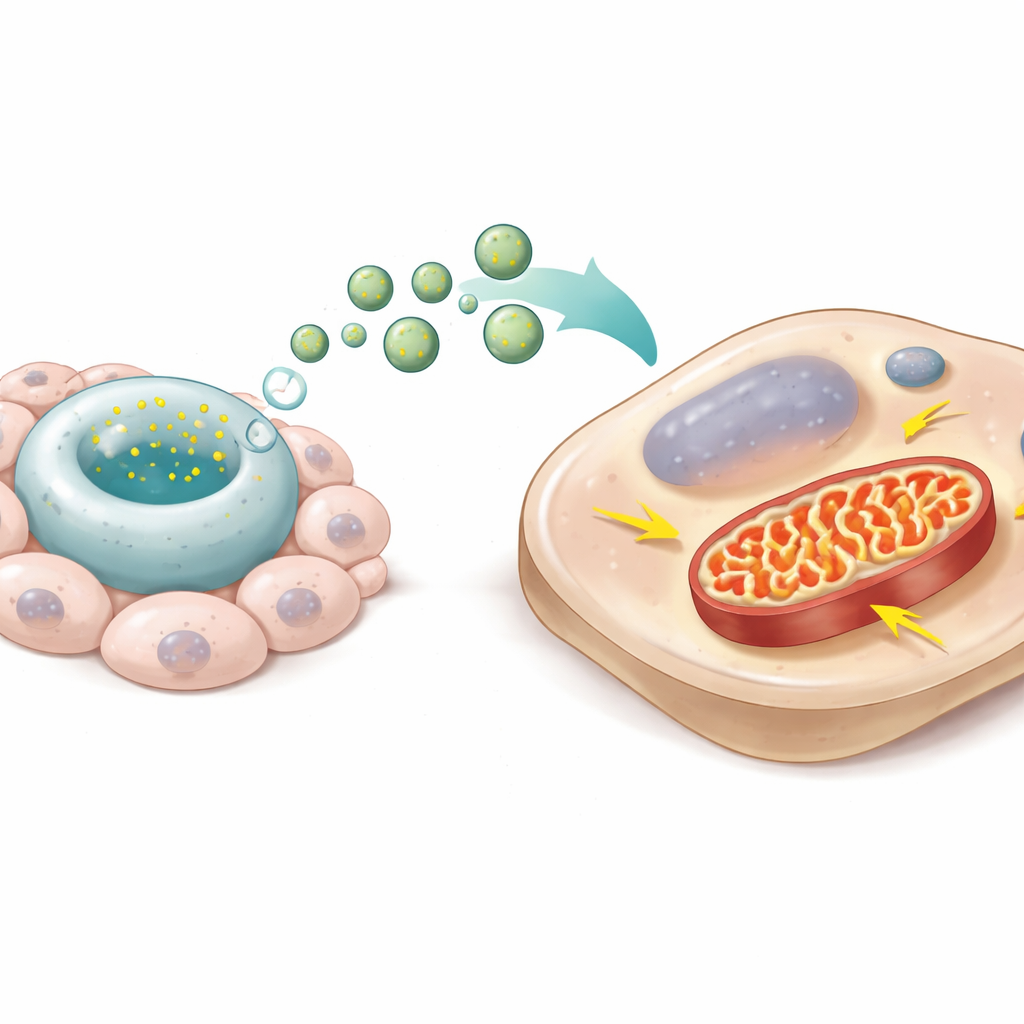
De onderzoekers analyseerden de lading van DevNiche-ApoEVs met geavanceerde eiwitprofilering. Ze ontdekten dat deze deeltjes rijk waren aan componenten van mitochondriaal complex I, een cruciaal toegangspunt voor energieproductie binnen mitochondriën. Wanneer DevNiche-ApoEVs aan volwassen ligamentcellen in het laboratorium werden toegevoegd, werden de vesicles opgenomen en verschenen hun complex I-eiwitten binnenin de ontvangende cellen. Mitochondriën werden langer met dichtere binnenplooien, produceerden meer energie via zuurstofgebruik en genereerden minder schadelijke reactieve zuurstofsoorten. Blokkeren van complex I met een geneesmiddel wist deze voordelen uit, wat aantoont dat deze mitochondriale machinerie centraal staat in het effect. In wezen schakelden de vesicles volwassen cellen om van een laag-energetische, stressgevoelige staat naar een jeugdige, hoog-efficiënte energieprofiel.
Van petrischaal naar levende kaak
Om te onderzoeken of deze metabole reboot daadwerkelijk complexe weefsels kon herbouwen, creëerde het team nauwkeurige parodontale defecten in ratten waarbij bot, ligament en wortelbekleding in één blok werden verwijderd. Ze vulden de defecten met een standaard mineraal scaffold, ofwel alleen of geladen met DevNiche-ApoEVs. In de weken daarna groeiden bij de dieren die DevNiche-ApoEVs ontvingen dichte, goed geïntegreerde botlagen, een nieuwe cementum-achtige laag op de wortel en ligamentvezels die in de juiste richting liepen en zowel in wortel als bot verankerden. Microscopen toonden tekenen van bloedvatgroei, georganiseerde celclustering, mineraalafzetting en een rustigere immuunomgeving die leek op de ontwikkelingsfase. Defecten behandeld zonder DevNiche-ApoEVs vulden grotendeels met littekenachtig weefsel en slecht georiënteerde vezels.
Wat dit kan betekenen voor toekomstige behandelingen
Deze studie suggereert dat zorgvuldig ontworpen vesicles kunnen fungeren als "ontwikkeling in een fles", door zowel stamcelkenmerken als omgevingssignalen te dragen om sluimerende herstelprogramma's in volwassen weefsels te wekken. Door mitochondriaal complex I te leveren en een jeugdig energiemodel te herstellen, hielpen DevNiche-ApoEVs volwassen cellen het tandondersteunende complex te herbouwen op een manier die sterk lijkt op natuurlijke formatie tijdens groei. Hoewel dit nog in een vroege fase is, suggereert deze benadering toekomstige therapieën waarin artsen vergelijkbare vesicles zouden kunnen gebruiken om beschadigde organen tot zelfgestuurde regeneratie aan te zetten in plaats van eenvoudige reparatie.
Bronvermelding: Zhang, Y., Xu, J., Shi, Y. et al. Fuel to fire: developmental niche-empowered ApoEVs unlock adult hierarchical tissue regenerative potential via mitochondrial complex I-driven developmental metabolic profile. Int J Oral Sci 18, 40 (2026). https://doi.org/10.1038/s41368-026-00440-9
Trefwoorden: parodontale regeneratie, stamcelnis, extracellulaire vesicles, mitochondriaal metabolisme, weefseltechniek