Clear Sky Science · ar
وقود للنار: حويصلات ApoEVs المُعزَّزة بالموئل النمائي تفتح إمكانات تجديد الأنسجة الهرمية لدى البالغين عبر ملف تماثل الأيض النمائي المعتمد على المُركب الميتوكوندري الأول
لماذا يصعب إعادة بناء الأنسجة لدى البالغين
تتكوّن العديد من أعضاء أجسامنا من طبقات متناسقة بإحكام، مثل كعكة ذات طبقات. بعد أن ننضج، تصبح هذه التركيبات الطبقية غير قادرة إلى حدٍّ مدهش على إصلاح نفسها بعد إصابة شديدة. يطرح هذا البحث سؤالًا جريئًا: بدل محاولة رقع أنسجة البالغين كما هي، هل يمكن أن نعيدها مؤقتًا إلى حالة نمائية أكثر شبابًا حتى تتمكن من إعادة البناء بشكل صحيح؟ باستخدام أنسجة دعم الأسنان كنموذج، يقدم الفريق طريقة جديدة لـ«تزويد الوقود» للخلايا البالغة بإشارات نمائية مغلفة في جسيمات طبيعية دقيقة.
كيف تبني الأسنان الشابة نظام دعم مثاليًا
خلال الطفولة، تتشكل الأنسجة التي تثبت الأسنان في موضعها بطريقة منسقة للغاية. ينمو العظم والرباط وطبقة معدنية رقيقة على الجذر معًا وتتشابك، مما يمنح السن ثباتًا ومرونة طفيفة. قارن الفريق هذا الإعداد النمائي مع حالة الإصلاح لدى البالغين. في النسيج الشاب، وجدوا بيئة هادئة مضادة للالتهاب تُشكلها خلايا مناعية نوع خاص تُشبه البلعمات M2. تساعد هذه الخلايا على خلق «موئل» داعم حول الخلايا الجذعية، مشجعة على استخدام طاقة قوي، وميتوكوندريا صحية، وتفضيل الأيض الهوائي الفعال. بالمقابل، في البالغين، تكون البيئة أكثر التهابًا، والخلايا الجذعية أقل وأكثر كسلاً، والهيكل الطبقي الدقيق عادة ما يفشل في النمو مجددًا.
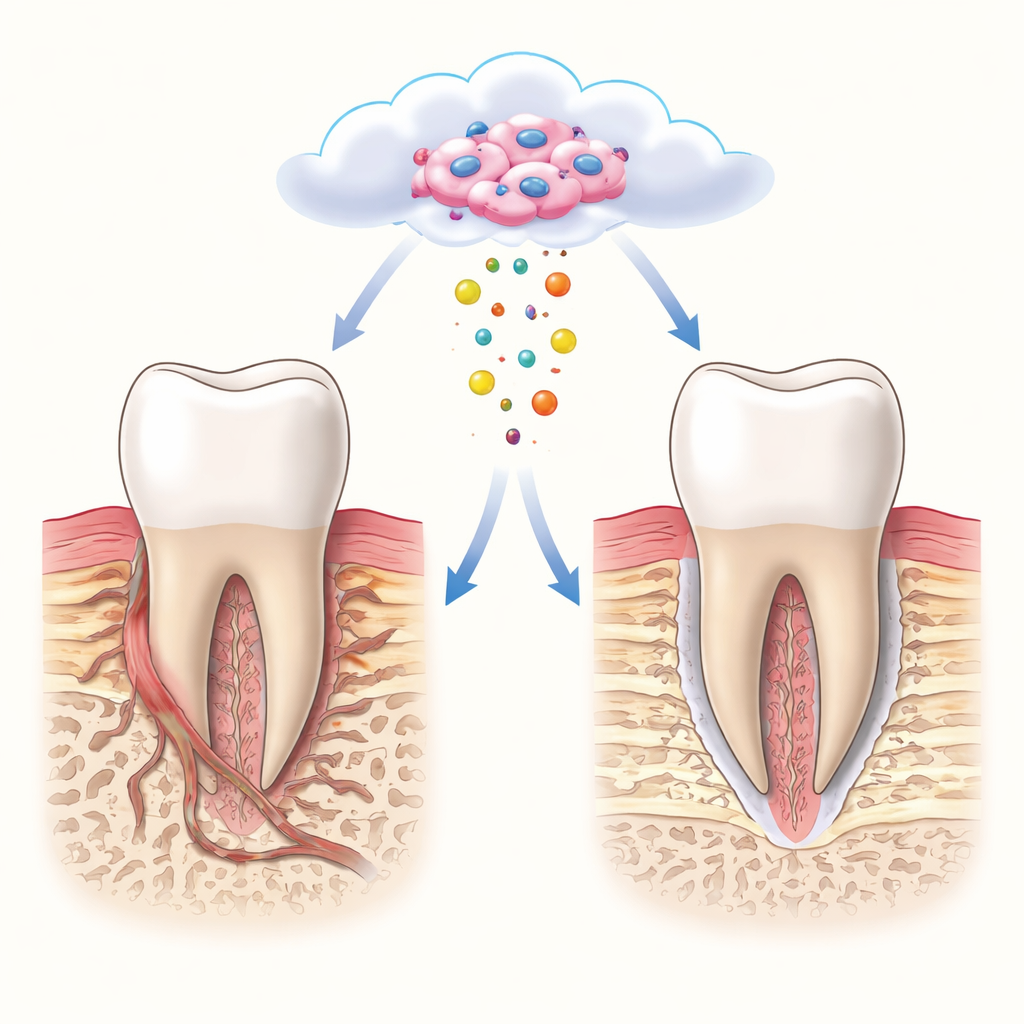
الاستفادة من آلية التنظيف الطبيعية في الجسم
عند زراعة الخلايا الجذعية في نسيج مُتضرر، تموت معظمها خلال أيام. بدل اعتبار ذلك فشلًا، اقترحت أعمال حديثة أن الخلايا الميتة قد تظل مفيدة عبر طرح جزيئات مغلفة بالغشاء تُسمى الحويصلات الخلوية المبرمجة للموت (apoptotic extracellular vesicles). تحمل هذه الجزيئات بروتينات وجزيئات أخرى من خلاياها الأم ويمكنها التأثير في الخلايا المجاورة دون مخاطر زرع خلايا كاملة. افترض المؤلفون أنه إذا عرضوا أولًا خلايا جذعية من رباط السن إلى موئل يشبه الحالة النمائية، ثم حثوا موتها المنظم، فسوف «تتذكّر» الحويصلات الناتجة كلًا من الخلايا الجذعية وبيئتها الشابة. أطلقوا على هذه الجسيمات المصممة اسم DevNiche-ApoEVs.
إعادة شحن الخلايا البالغة عبر الميتوكوندريا
فحص الباحثون حمولة DevNiche-ApoEVs باستخدام تحليل بروتيني متقدم. وجدوا أن هذه الجسيمات غنية بمكونات المركب الميتوكوندري الأول، وهو مدخل رئيسي لتوليد الطاقة داخل الميتوكوندريا. عندما أضيفت DevNiche-ApoEVs إلى خلايا الرباط البالغة في المختبر، ابتلعتها الخلايا وظهرت بروتينات المركب الأول داخلها. أصبحت الميتوكوندريا أكثر استطالة وذات طيات داخلية كثيفة، أنتجت المزيد من الطاقة عبر استخدام الأكسجين، وولدت أقل من الجذور الحرة الضارة. أدى حجب المركب الأول بدواء إلى زوال هذه الفوائد، مما يبرز أن هذه الآلية الميتوكوندرية مركزية للتأثير. باختصار، حوّلت الحويصلات الخلايا البالغة من حالة منخفضة الطاقة وعرضة للإجهاد إلى ملف طاقي شبابي عالي الكفاءة.
من طبق بتري إلى عظْم الفك الحي
لاختبار ما إذا كان هذا إعادة التشغيل الأيضي يمكن أن يعيد بالفعل أنسجة معقدة، أحدث الفريق عيوبًا دورية دقيقة في الفئران أزالت العظم والرباط وطبقة تغطية الجذر ككتلة واحدة. ملأوا العيوب بمسحوق معدني قياسي، إما وحده أو محمَّلًا بـDevNiche-ApoEVs. على مدى الأسابيع التالية، نمت لدى الحيوانات التي تلقت DevNiche-ApoEVs عظام سميكة ومندمجة جيدًا، وطبقة جديدة شبيهة بالسمنتوم على الجذر، وألياف رباط سارت في الاتجاه الصحيح وربطت بين الجذر والعظم. أظهرت المجاهر إشارات لنمو الأوعية الدموية، وتنظيم تجمعات الخلايا، وترسُب المعادن، وبيئة مناعية أكثر هدوءًا تشبه المرحلة النمائية. بالمقابل، امتلأت العيوب المعالجة دون DevNiche-ApoEVs في الغالب بنسيج شِبِه ندبي وألياف ضعيفة التوجيه.
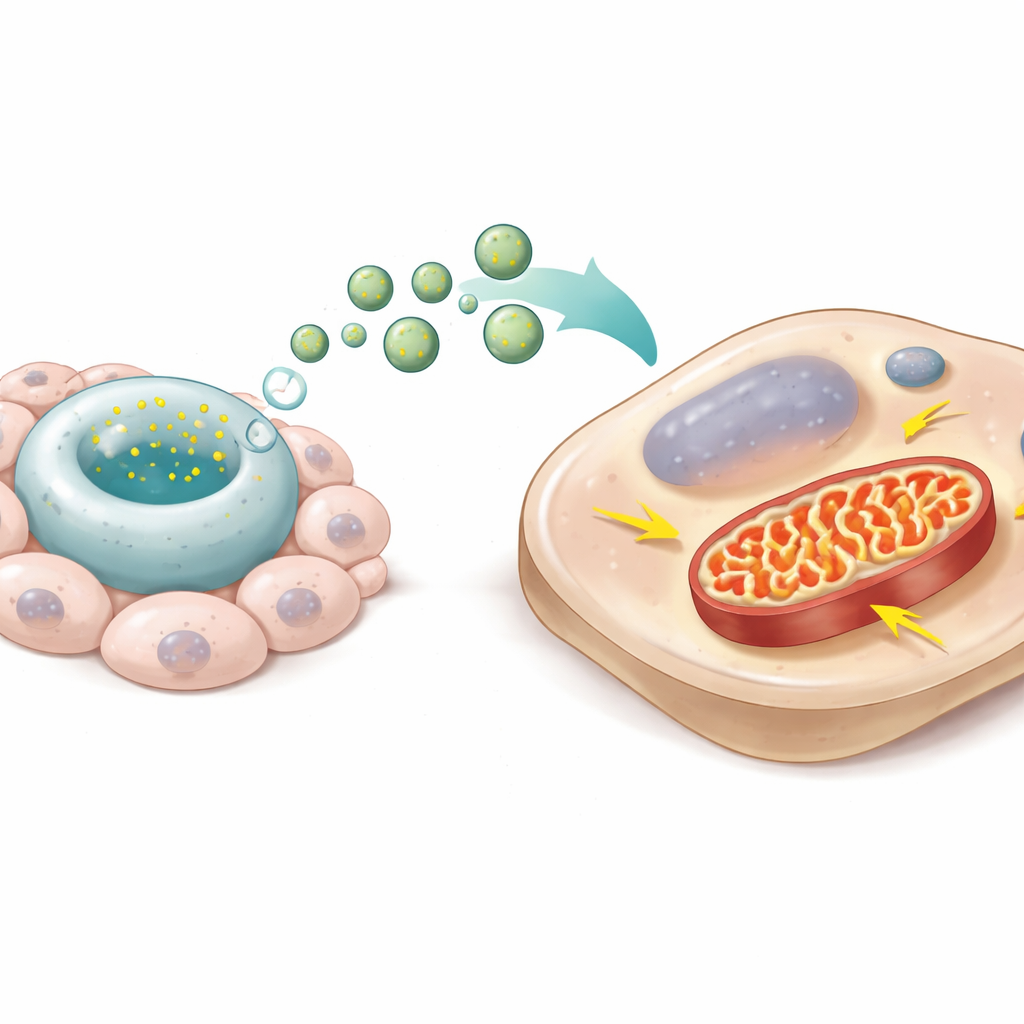
ما الذي قد يعنيه هذا للعلاجات المستقبلية
تشير هذه الدراسة إلى أن الحويصلات المصممة بعناية يمكن أن تعمل كـ«نموذج نمائي في قارورة»، حاملة صفات الخلايا الجذعية والإشارات البيئية لإيقاظ برامج الإصلاح الكامنة في الأنسجة البالغة. من خلال توصيل المركب الميتوكوندري الأول واستعادة نمط طاقة شبابي، ساعدت DevNiche-ApoEVs الخلايا البالغة على إعادة بناء مركب دعم السن بطريقة تحاكي إلى حد كبير التكوين الطبيعي خلال النمو. وبينما لا يزال النهج في مرحلة مبكرة، يلمّح إلى علاجات مستقبلية قد يستخدم فيها الأطباء حويصلات مماثلة لتحفيز الأعضاء المتضررة نحو تجدد موجه ذاتيًا بدل الإصلاح البسيط.
الاستشهاد: Zhang, Y., Xu, J., Shi, Y. et al. Fuel to fire: developmental niche-empowered ApoEVs unlock adult hierarchical tissue regenerative potential via mitochondrial complex I-driven developmental metabolic profile. Int J Oral Sci 18, 40 (2026). https://doi.org/10.1038/s41368-026-00440-9
الكلمات المفتاحية: تجديد اللثة, موئل الخلايا الجذعية, الحويصلات خارج الخلوية, أيض الميتوكوندريا, هندسة الأنسجة