Clear Sky Science · ja
ネッタイシマカ(Aedes aegypti)の小さなRNAゲノミクスが、RNA干渉応答を誘導する感染性ウイルスを発見する
なぜ蚊のウイルスが私たち全員に関係するのか
蚊はデング熱やジカ熱など人間の病気を媒介することで悪名高いが、実際にはニュースにならない多くのウイルスを体内に抱えている。この研究は時宜を得た問いを投げかける:世界的に侵入的な黄熱蚊Aedes aegyptiの内部にどのような隠れたウイルスが存在し、そのウイルスを蚊自身の防御機構がどのように抑えているのか。世界中から集めた200以上の蚊サンプルの中の最小の遺伝断片を読み取ることで、著者らは、蚊が人に危険な病原体をいつ、どのように伝えるかに影響を与え得る、豊かで主に見えないウイルス世界を明らかにした。
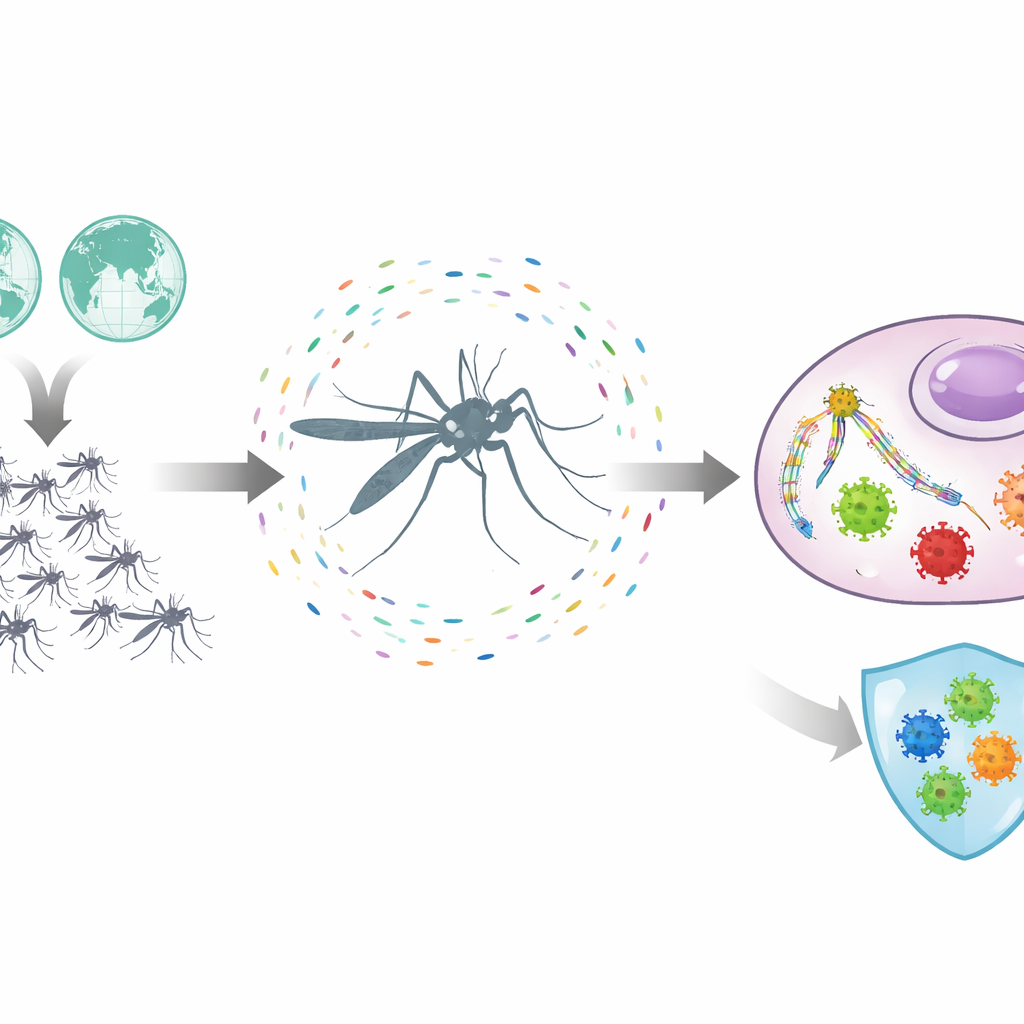
小さなRNA断片に残るウイルスの指紋を探す
研究者らは完全なウイルスゲノムを直接探すのではなく、「小さなRNA」に着目した。これらは蚊の細胞が侵入ウイルスから自然に切り出す短い遺伝断片であり、分子上の「顔写真」のように働いて免疫機構を導き、ウイルス素材を認識して切断する。チームはアメリカ、アジア、アフリカで採取された蚊と長年維持されてきた実験室系統を含む280以上のシーケンスデータセットをまとめ上げた。改良した解析パイプラインを用い、小さな断片をつなぎ合わせ、精選されたウイルスデータベースと照合し、蚊自身のDNAに埋め込まれたウイルス残存配列による誤ったシグナルを慎重に除外した。この手法により、単に存在するだけでなく実際に免疫応答を引き起こしているウイルスを見分けることが可能になった。
世界中に広がる隠れたウイルス仲間
調査の結果、Aedes aegyptiは人に感染しない多様な昆虫特異的ウイルスを意外なほど多く保持しており、それらが人に感染するウイルスの振る舞いに影響を与える可能性があることが分かった。Phasi Charoen-like virusやHumaita-Tubiacanga virusのようなウイルスはアメリカ大陸の広域からアジアにかけて見られ、一方Aedes aegypti Anphevirusはアメリカ北部でより一般的だった。注目すべき発見は、シンガポールで採取された野生蚊からデングウイルス由来の小さなRNAの形跡が見つかったことで、フィールドで捕獲されたAedes aegyptiでデングの免疫的指紋が確認されたのは初めてであり、日常的な監視ではデング感染の検出がいかに稀で短命であるかを示している。アフリカではFormosusウイルスと名付けられた別個のウイルスが現地コロニーで繰り返し検出され、親から子へ安定して伝わっていることを示唆した。
実験室蚊と植物様ウイルス
研究で多用される学術用の実験室系統は、持続感染ウイルスがほとんどみられなかった。対照的に、殺虫剤試験用に商業的に飼育されている二つのコロニーでは、植物ウイルスの親戚にあたるトンブス様ウイルスに対する非常に高い感染負荷が見られた。ウイルス由来の素材と防御的小さなRNAは成虫だけでなく卵にも検出され、母蚊から子孫への効率的な垂直伝播を示唆した。研究はまた、パルティティウイルスや追加のトンブス様ウイルスなど、植物病原体に関連するいくつかの蚊ウイルスを確認した。これらが蚊の腸内で示すパターンは、蚊が糖分を含む植物液を吸う際に植物から昆虫へ飛び移った可能性を示唆し、植物、蚊、そしてそれらのウイルスを結ぶより広い生態学的ネットワークをほのめかしている。
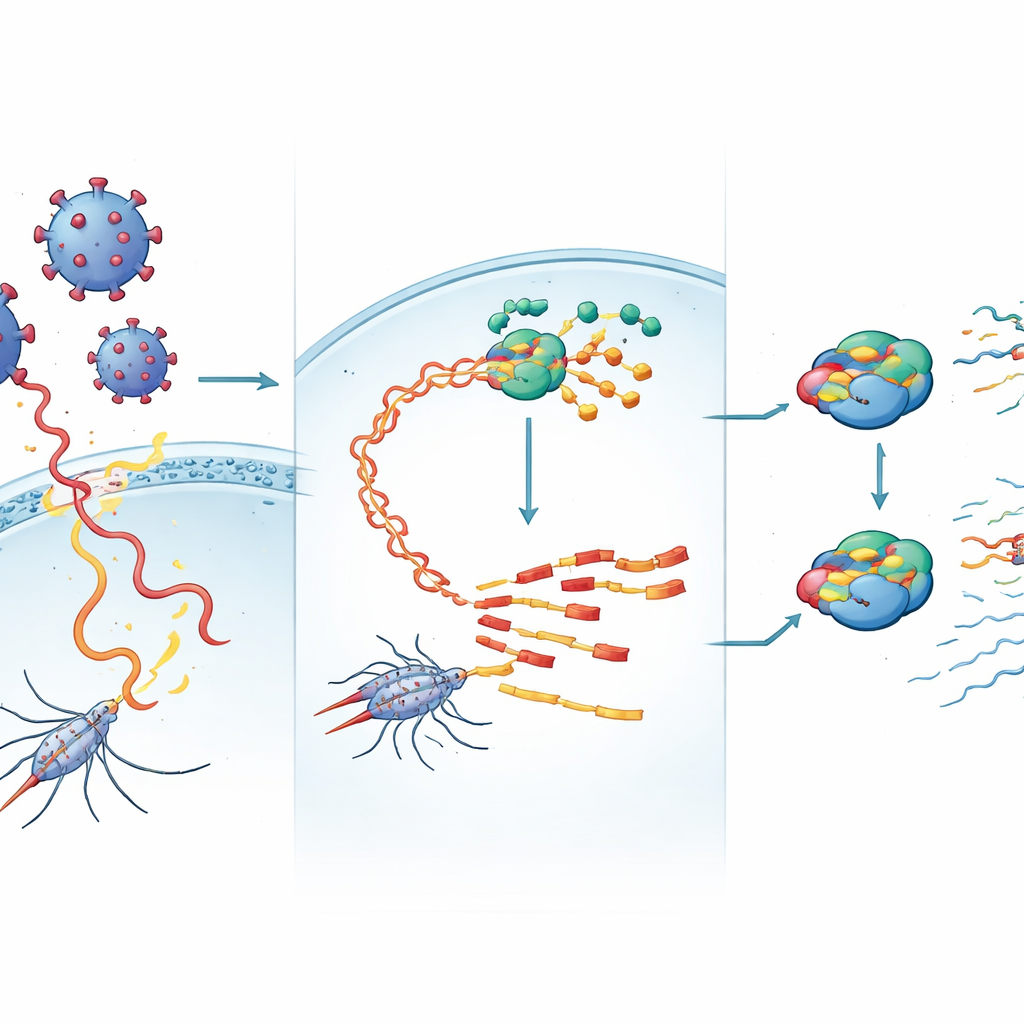
野生蚊からウイルス感染細胞へ
観察された遺伝痕跡が単なる残片ではなく、実際に感染性を持つ因子に対応していることを証明するため、著者らは均質化した蚊組織を用いて蚊の細胞株に感染させた。アフリカのFormosusウイルスや商業系統由来のトンブス様ウイルスを含むいくつかのウイルスは、これらの細胞に長期感染を確立することに成功した。定着後、ウイルスは豊富な小さなRNA産生を誘導し、しばしば全蚊で観察されたパターンを反映した。同じサンプルからより長いウイルスRNA分子の配列も解析することで、各ウイルスがどれだけ活発に複製しているかと、RNAベースの防御システムをどれほど強く刺激しているかを比較でき、ウイルスがほとんど免疫反応を引き起こさずに複製する場合や、逆に全長のウイルスRNAが薄れても小さなRNAが持続するケースが明らかになった。
遺伝子を能動的にサイレンスする小さなRNA
機能の最も直接的な検証は巧妙に設計されたレポーター実験から得られた。研究者らは発光酵素をコードする人工遺伝子を作り、その末端にウイルス配列の断片を付加した。これらのレポーターをFormosusやトンブス様ウイルスで慢性感染している蚊細胞に導入すると、細胞内のウイルス由来小さなRNAと相補的に結合し得る向きでウイルス断片を持つレポーターは強くサイレンスされたが、ウイルスRNAと同じ方向に配列が揃ったものはサイレンスされなかった。これは、感染中に生成される小さなRNAが単なる受動的なマーカーではなく、遺伝子サイレンシング機構をマッチする配列へ能動的に導くことを示し、蚊が長期的なウイルス寄生者を抑制する具体的な仕組みを提供する。
病気と蚊防除にとっての意味
これらの結果は、Aedes aegyptiが昆虫特異的ウイルスの移動する生態系であり、強力な小さなRNA防御システムによって常に監視され部分的に抑えられているという図を描く。これらの常在ウイルスはデングやジカなどの人に対する病原体の複製や伝播に影響を与え得るため、小さなRNAゲノミクスによるマッピングは、既知の脅威のみを探す従来の検査を超えて蚊の監視を大幅に強化しうる。長期的には、ウイルス由来の小さなRNAやそれらを産生するウイルスを活用することで、蚊媒介疾患を減らす新たな手段や、蚊個体群に対する標的型の遺伝子サイレンシングを実行する手法の開発につながり、将来の流行との戦いにおける予期せぬ味方を提供する可能性がある。
引用: Gupta, S., Sharma, R., Williams, A.E. et al. Small RNA genomics of Aedes aegypti mosquitoes discovers infectious viruses that trigger an RNA interference response. Nat Commun 17, 3658 (2026). https://doi.org/10.1038/s41467-026-71964-1
キーワード: Aedes aegypti, 蚊のウイルス相, 小さなRNA, RNA干渉, 媒介者監視