Clear Sky Science · de
Kleine‑RNA‑Genomik bei Aedes aegypti‑Mücken entdeckt infektiöse Viren, die eine RNA‑Interferenz‑Antwort auslösen
Warum Mückenviren uns alle betreffen
Mücken sind dafür berüchtigt, Dengue, Zika und andere Krankheiten zu übertragen, doch die Tiere tragen viele weitere Viren in sich, die kaum je Schlagzeilen machen. Diese Studie stellt eine aktuelle Frage: Welche verborgenen Viren leben im global invasiven Gelbfiebermücken‑Artenkomplex Aedes aegypti, und wie hält das Immunsystem der Mücke sie in Schach? Indem die Autorinnen und Autoren die winzigsten genetischen Fragmente in mehr als 200 Mückenproben aus aller Welt auslasen, decken sie eine reiche, weitgehend unsichtbare Virenwelt auf, die beeinflussen könnte, ob, wann und wie Mücken gefährliche Erreger auf Menschen übertragen.
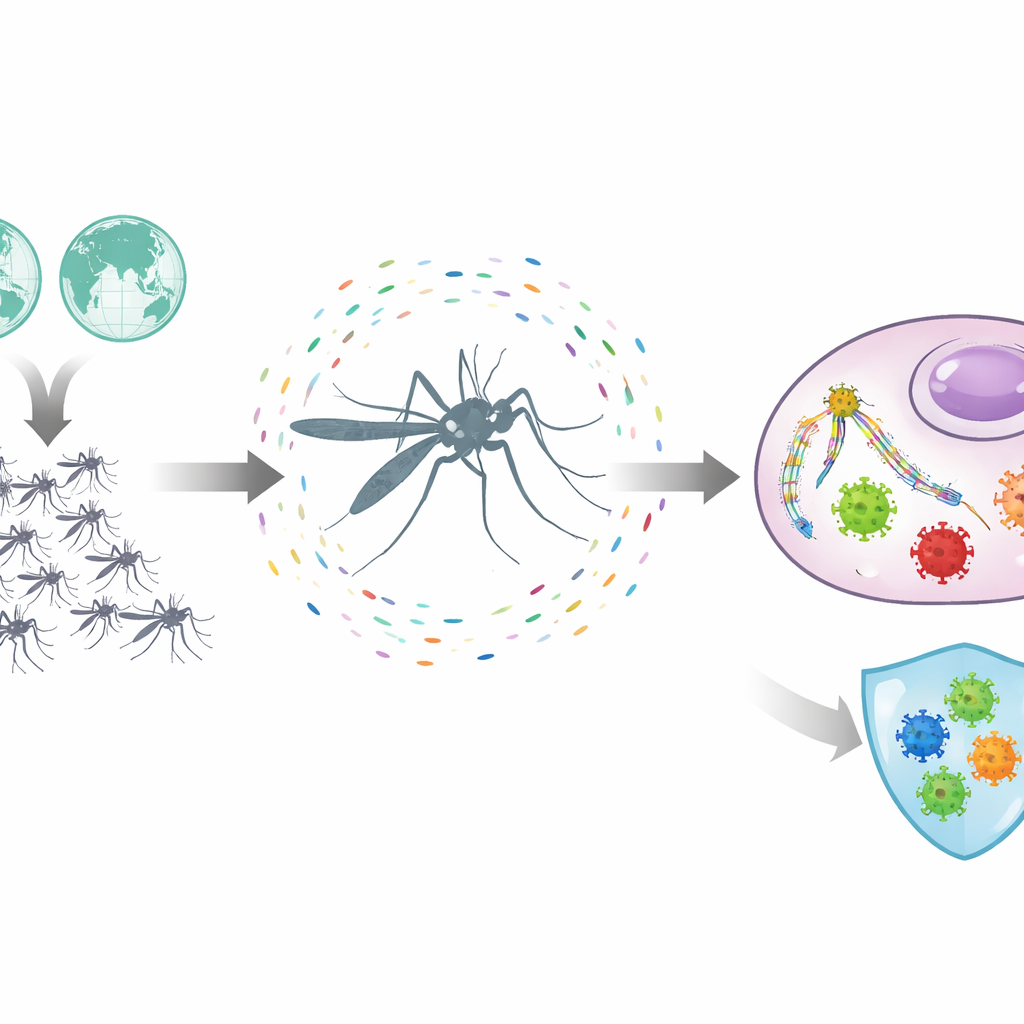
Auf der Suche nach viralen Fingerabdrücken in kleinen RNA‑Stücken
Statt direkt nach kompletten Virengenomen zu suchen, konzentrierten sich die Forschenden auf „kleine RNAs“ – kurze genetische Fragmente, die Mückenzellen natürlicherweise aus eindringenden Viren schneiden. Diese kleinen Stücke fungieren wie molekulare Täterfotos und leiten die Immunmaschinerie der Insekten an, virales Material zu erkennen und zu zerschneiden. Das Team wertete über 280 Sequenzierungsdatensätze von Mücken aus den Amerikas, Asien und Afrika sowie von langjährigen Laborstämmen aus. Mit einer verbesserten Analyse‑Pipeline setzten sie kleine Fragmente zusammen, verglichen sie mit kuratierten Virendatenbanken und filterten sorgfältig irreführende Signale heraus, die von viralen Überresten im Genom der Mücke stammen könnten. Dieser Ansatz erlaubte es ihnen, Viren zu identifizieren, die nicht nur vorhanden waren, sondern aktiv eine Immunantwort auslösten.
Verborgene virale Nachbarn rund um den Globus
Die Untersuchung zeigte, dass Aedes aegypti eine überraschende Vielfalt an insekten‑spezifischen Viren trägt, die den Menschen nicht infizieren, aber das Verhalten humanpathogener Viren beeinflussen könnten. Einige, wie Phasi Charoen‑ähnliches Virus und Humaita‑Tubiacanga‑Virus, traten großflächig in den Amerikas und bis nach Asien auf, während ein anderes, als Aedes aegypti Anphevirus bezeichnetes Virus häufiger in nördlichen Teilen der Amerikas vorkam. Auffällig war der Nachweis von Dengue‑ähnlichen kleinen RNAs in einer wilden Mücke aus Singapur – der erste Nachweis dieser immunologischen Fingerabdrücke von Dengue in einer feldgefangenen Aedes aegypti und ein Hinweis darauf, wie selten und flüchtig nachweisbare Dengue‑Infektionen in routinemäßiger Überwachung sein können. In Afrika tauchte wiederholt ein eigenständiges Virus, das Formosus‑Virus genannt wurde, in lokalen Kolonien auf, was darauf hindeutet, dass es stabil von Eltern auf Nachkommen übertragen wird.
Labormücken und pflanzenähnliche Viren
Akademische Laborstämme von Mücken, die in der Forschung häufig genutzt werden, waren größtenteils frei von persistierenden Viren. Im Gegensatz dazu trugen zwei kommerzielle Kolonien, die für Pestizidtests gehalten werden, außergewöhnlich starke Infektionen mit einem tombus‑ähnlichen Virus, einem Verwandten von Pflanzenviren. Virale RNA und defensive kleine RNAs wurden nicht nur in Adulten, sondern auch in Eiern nachgewiesen, was auf eine effiziente vertikale Übertragung von Müttern auf ihre Nachkommen hindeutet. Die Studie identifizierte zudem mehrere Mückenviren, die mit Pflanzenpathogenen verwandt sind, etwa Partitiviren und weitere tombus‑ähnliche Viren. Ihre Muster im Mückendarm deuten darauf hin, dass sie beim Saugen von zuckerhaltigen Pflanzensäften von Pflanzen auf Insekten übergesprungen sein könnten, was auf ein größeres ökologisches Netzwerk zwischen Pflanzen, Mücken und deren Viren hindeutet.
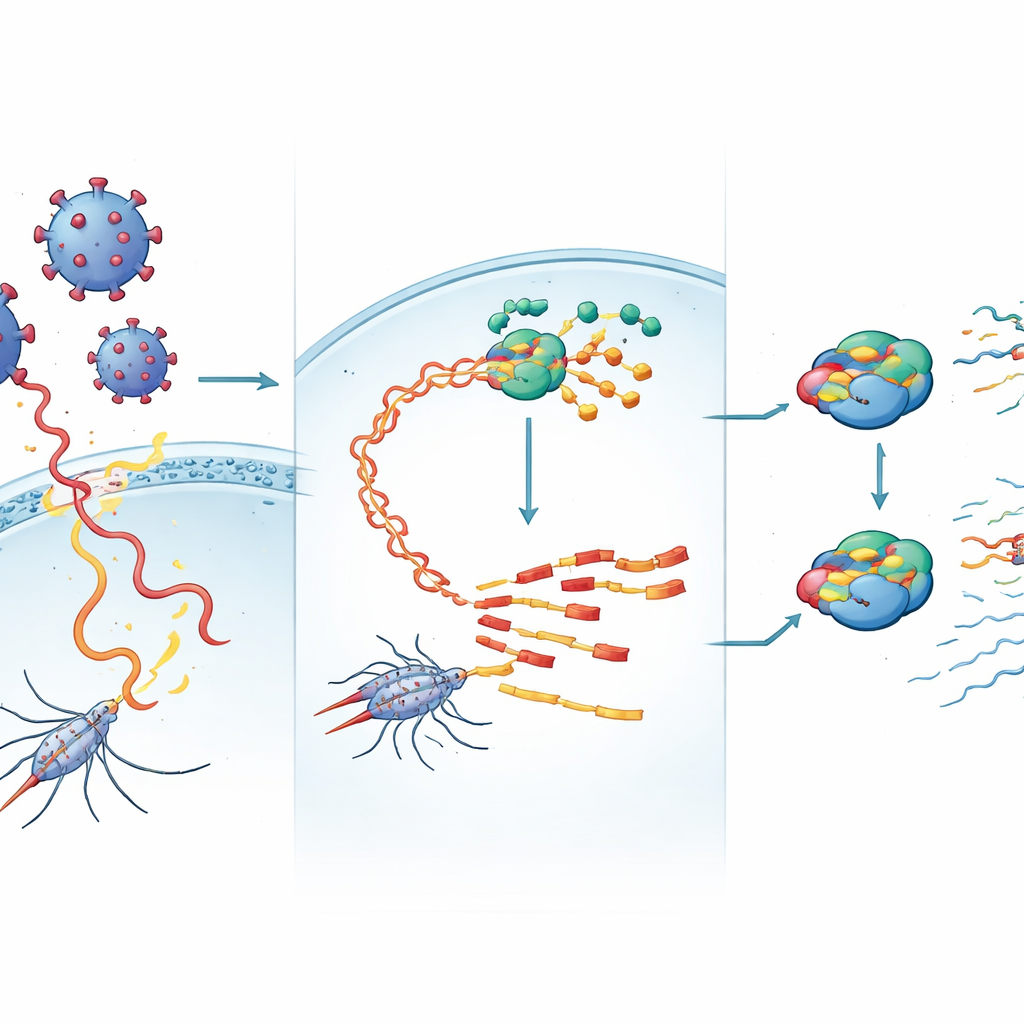
Von wilden Mücken zu virusinfizierten Zellen
Um zu beweisen, dass die genetischen Spuren echten, infektiösen Agenzien entsprachen und nicht nur Überresten, verwendeten die Autorinnen und Autoren homogenisierte Mückengewebe, um Mückenzelllinien in Kultur zu infizieren. Mehrere Viren, darunter das afrikanische Formosus‑Virus und das tombus‑ähnliche Virus aus den kommerziellen Stämmen, etablierten erfolgreich langanhaltende Infektionen in diesen Zellen. Einmal etabliert, lösten die Viren eine reichliche Produktion kleiner RNAs aus, die oft die Muster widerspiegelten, die in ganzen Mücken zu sehen waren. Durch zusätzliches Sequenzieren längerer viraler RNA‑Moleküle aus denselben Proben konnte das Team vergleichen, wie aktiv sich jedes Virus replizierte und wie stark es das RNA‑basierte Abwehrsystem erregte – und so Fälle aufzeigen, in denen Viren mit wenig Immunreaktion replizierten, sowie andere, in denen kleine RNAs fortbestanden, obwohl vollständige virale RNAs verblassten.
Kleine RNAs, die Gene aktiv stummschalten
Der direkteste Funktionstest bestand aus raffiniert gestalteten Reporter‑Experimenten. Die Forschenden konstruierten künstliche Gene, die ein lichtproduzierendes Enzym codieren, und hängten virale Sequenzabschnitte an ihre Enden. Wenn diese Reporter in Mückenzellen eingeführt wurden, die chronisch mit Formosus‑ oder tombus‑ähnlichen Viren infiziert waren, wurden Reporter, die virale Abschnitte in der Orientierung trugen, die mit den viralen kleinen RNAs der Zelle paaren konnte, stark stummgeschaltet, während solche in gleicher Richtung wie die viralen RNAs dies nicht waren. Das zeigt, dass die während der Infektion erzeugten kleinen RNAs nicht bloß passive Marker sind; sie steuern aktiv die Gen‑Silencing‑Maschinerie auf passende Sequenzen und liefern einen konkreten Mechanismus, wie Mücken langfristige virale Bewohner in Schach halten können.
Was das für Krankheit und Mückenbekämpfung bedeutet
Zusammen zeichnen diese Ergebnisse ein Bild von Aedes aegypti als beweglichem Ökosystem insekten‑spezifischer Viren, das ständig von einem starken kleinen‑RNA‑Abwehrsystem überwacht und teilweise gezähmt wird. Da diese residenten Viren beeinflussen können, wie Dengue, Zika und andere humanpathogene Viren replizieren und sich ausbreiten, könnte ihre Kartierung mittels kleiner‑RNA‑Genomik die Mückenüberwachung deutlich stärken – weit über traditionelle Tests hinaus, die nur nach bekannten Bedrohungen suchen. Langfristig könnte das Nutzen viraler kleiner RNAs oder der Viren, die sie produzieren, neue Werkzeuge bieten, um mückenübertragene Krankheiten abzuschwächen oder sogar gezielte Gen‑Stummschaltung in Mückenpopulationen einzubringen und so einen unerwarteten Verbündeten im Kampf gegen künftige Ausbrüche zu liefern.
Zitation: Gupta, S., Sharma, R., Williams, A.E. et al. Small RNA genomics of Aedes aegypti mosquitoes discovers infectious viruses that trigger an RNA interference response. Nat Commun 17, 3658 (2026). https://doi.org/10.1038/s41467-026-71964-1
Schlüsselwörter: Aedes aegypti, Mücken‑Virom, kleine RNA, RNA‑Interferenz, Vektorüberwachung