Clear Sky Science · it
Lo ione ferroabilita l’evoluzione fotocatalitica dell’idrogeno dal metanolo
Un modo semplice per produrre combustibile pulito
L’idrogeno è spesso presentato come un combustibile pulito del futuro perché, quando viene utilizzato, rilascia solo acqua e non anidride carbonica. Oggi però la maggior parte dell’idrogeno viene ancora ricavata da combustibili fossili, cosa che ne riduce i vantaggi climatici. Questo studio esplora un modo sorprendentemente semplice per ottenere idrogeno da alcoli comuni come il metanolo, impiegando sali di ferro ordinari e luce anziché metalli preziosi costosi e alte temperature. 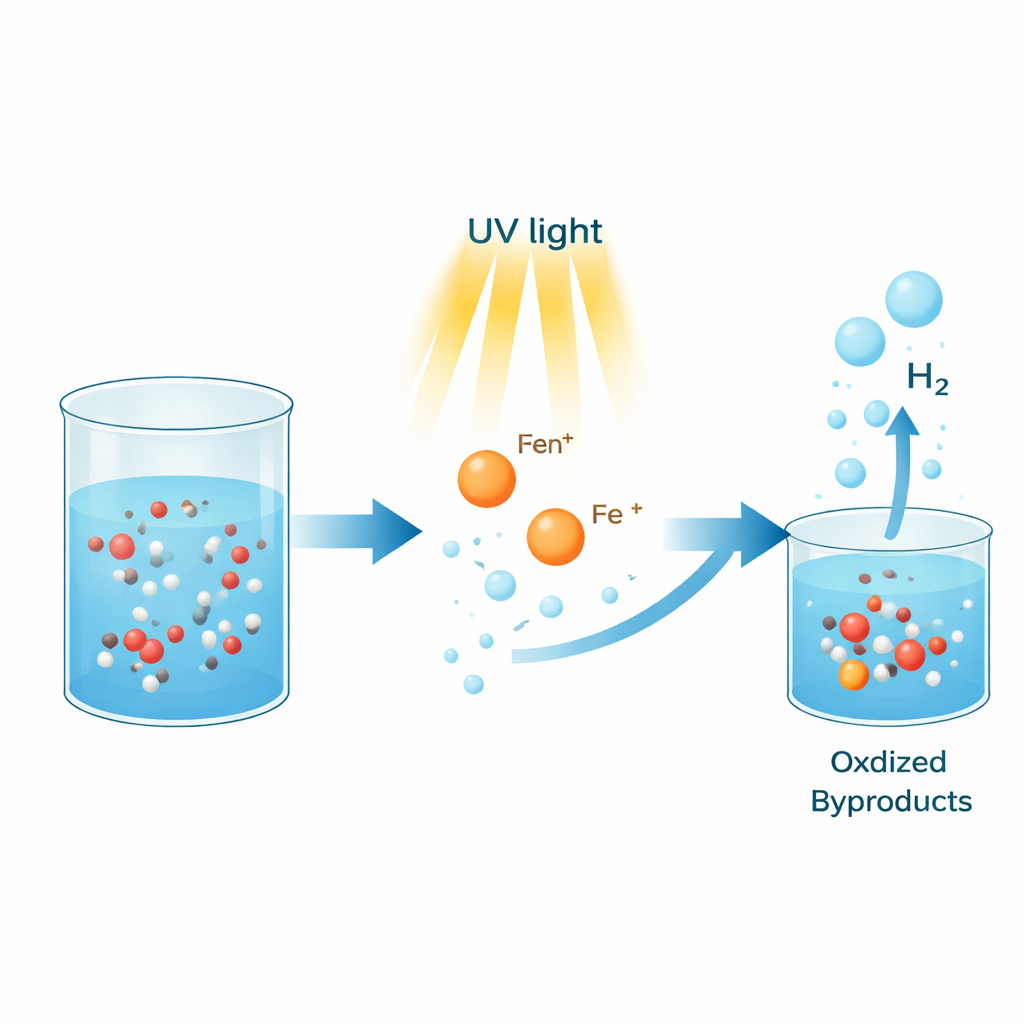
Trasformare un alcol liquido in un gas utile
I ricercatori si sono concentrati sul metanolo, un liquido comune che già immagazzina una grande quantità di idrogeno in forma compatta. Se si riesce a estrarre l’idrogeno dal metanolo in modo efficiente, il liquido può agire come un vettore di idrogeno facile da maneggiare per celle a combustibile e altri dispositivi. I metodi tradizionali si basano su composti metallici complessi o su catalizzatori solidi che contengono elementi rari come platino, rutenio o iridio e spesso richiedono alte temperature. Invece, questo lavoro dimostra che un semplice sale di ferro, disciolto nel metanolo e aiutato da una piccola quantità di base, può rilasciare idrogeno quando la miscela è illuminata con luce ultravioletta.
Come lavorano insieme luce e ferro
Nel nuovo sistema, gli ioni ferro in soluzione si legano alle molecole di metanolo vicine. La luce ultravioletta è assorbita da queste coppie ferro–alcol, provocando uno spostamento di carica interno: elettroni si muovono dal lato dell’alcol verso il centro di ferro. Questo passaggio indotto dalla luce trasforma il ferro(III) in ferro(II) e crea frammenti di alcol molto reattivi chiamati radicali. Questi frammenti a vita breve aiutano a rompere il metanolo e a far accoppiare atomi di idrogeno in molecole di idrogeno gassoso, mentre la parte carboniosa del metanolo viene lasciata in forme più ossidate come formaldeide o acido formico. Gli esperimenti del team hanno anche mostrato che la reazione richiede sia luce sia ossigeno dall’aria per procedere; sotto azoto non si forma idrogeno, il che indica che l’ossigeno partecipa discretamente a ripristinare parti del sistema. 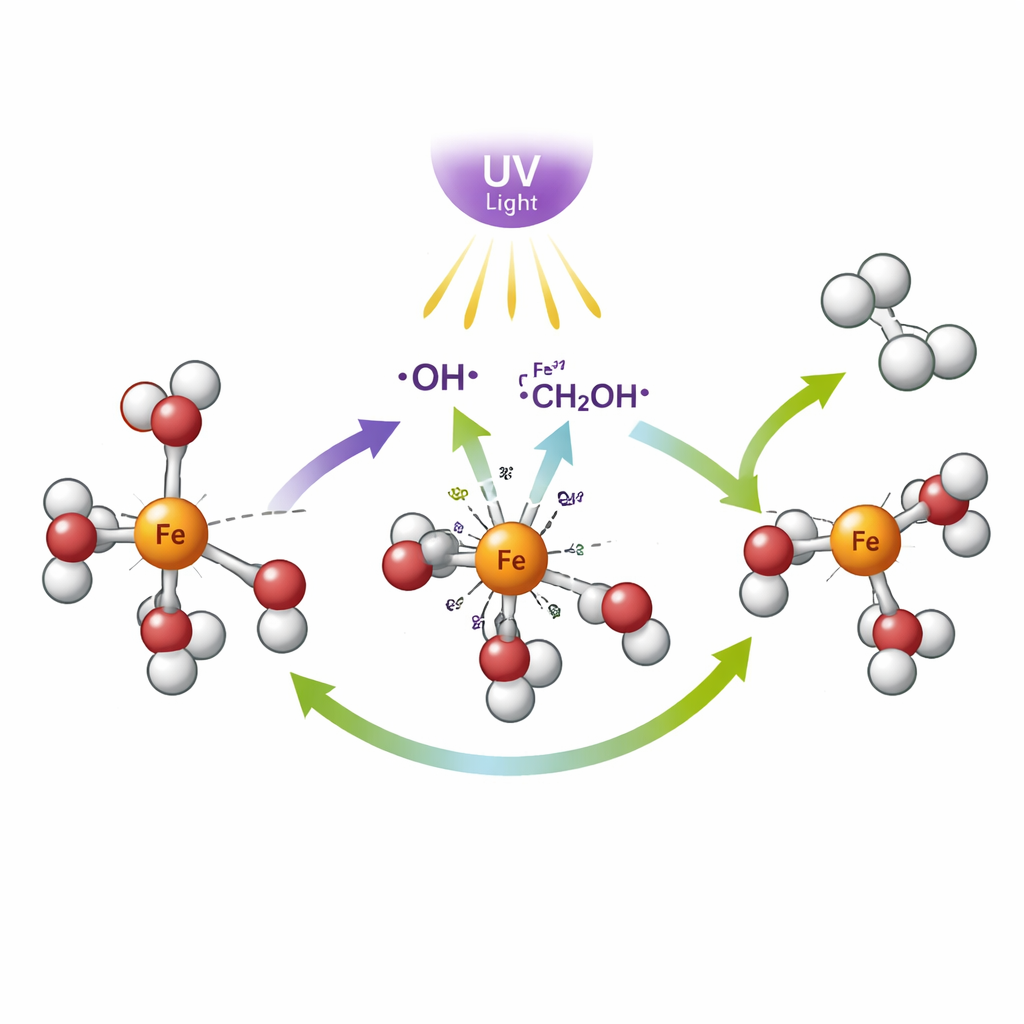
Regolare la reazione e testarne i limiti
Poiché l’allestimento è così semplice, gli autori hanno potuto indagare facilmente cosa lo rende più efficiente. L’aggiunta di idrossido di sodio, una base comune, aumenta notevolmente la reazione aiutando a convertire il metanolo in una forma più reattiva che si lega al ferro in modo più efficace. La misura di come la velocità di reazione varia con la concentrazione di base ha rivelato un comportamento di saturazione simile a quello osservato per gli enzimi, suggerendo un rapido passo di adattamento iniziale seguito da un passaggio più lento guidato dalla luce. La quantità di idrogeno prodotta dipende anche dalla quantità di ferro presente e dall’intensità della luce: concentrazioni di ferro più basse e un’illuminazione ultravioletta più intensa danno maggiore efficienza per ogni ione ferro. La reazione procede in modo costante per giorni, può essere moderatamente scalata e la stessa soluzione di ferro può essere riutilizzata più volte senza una perdita significativa di attività.
Oltre il metanolo: altri alcoli e biomassa
Il gruppo ha esplorato se questo approccio luce–ferro potesse trattare anche altri reagenti. Hanno scoperto che alcoli semplici come etanolo, 1-propanolo e 2-propanolo producono anch’essi idrogeno, sebbene con efficienza inferiore rispetto al metanolo, probabilmente perché molecole più ingombranti sono più difficili da deidrogenare. Quando è stata aggiunta acqua, la reazione è rallentata ma ha continuato a produrre idrogeno a ritmi comparabili ad alcuni fotocatalizzatori solidi riportati in letteratura. Più sorprendentemente, il sistema è stato in grado di generare idrogeno anche da fonti rinnovabili più complesse come glucosio, cellobiosio, amido, cellulosa e polvere di legno, sebbene in questi casi le velocità fossero molto più basse e i materiali solidi subissero solo alterazioni leggere.
Cosa significa per l’energia del futuro
Nel complesso, lo studio mostra che qualcosa di basilare come un sale di ferro disciolto può competere con catalizzatori molto più elaborati nel trasformare il metanolo in idrogeno sotto luce. Il processo si basa ancora sulla luce ultravioletta e funziona meglio con poca acqua, quindi non è ancora pronto a sostituire i metodi industriali esistenti. Tuttavia, il suo basso costo, la semplicità e la capacità di trattare una gamma di alcoli e biomassa suggeriscono una nuova direzione per la ricerca sui combustibili puliti. Dimostrando che ioni di ferro nudi in soluzione possono agire come catalizzatori efficaci guidati dalla luce, il lavoro apre la porta a nuovi progetti essenziali per la produzione di idrogeno da fonti rinnovabili.
Citazione: Sakurai, M., Kawasaki, Y., Itabashi, Y. et al. Iron ion enables photocatalytic hydrogen evolution from methanol. Commun Chem 9, 151 (2026). https://doi.org/10.1038/s42004-026-02009-3
Parole chiave: produzione fotocatalitica di idrogeno, deidrogenazione del metanolo, catalizzatori a base di ferro, carburanti solari, portatori liquidi di idrogeno