Clear Sky Science · fr
Les ions fer permettent l’évolution photocatalytique de l’hydrogène à partir du méthanol
Une manière simple de produire un carburant propre
L’hydrogène est souvent présenté comme un carburant propre du futur parce qu’il ne libère que de l’eau lorsqu’il est utilisé, et non du dioxyde de carbone. Mais aujourd’hui, la majeure partie de l’hydrogène est encore produite à partir de combustibles fossiles, ce qui réduit ses bénéfices climatiques. Cette étude explore une voie étonnamment simple pour produire de l’hydrogène à partir d’alcools courants comme le méthanol, en utilisant des sels de fer ordinaires et la lumière plutôt que des métaux précieux coûteux et des températures élevées. 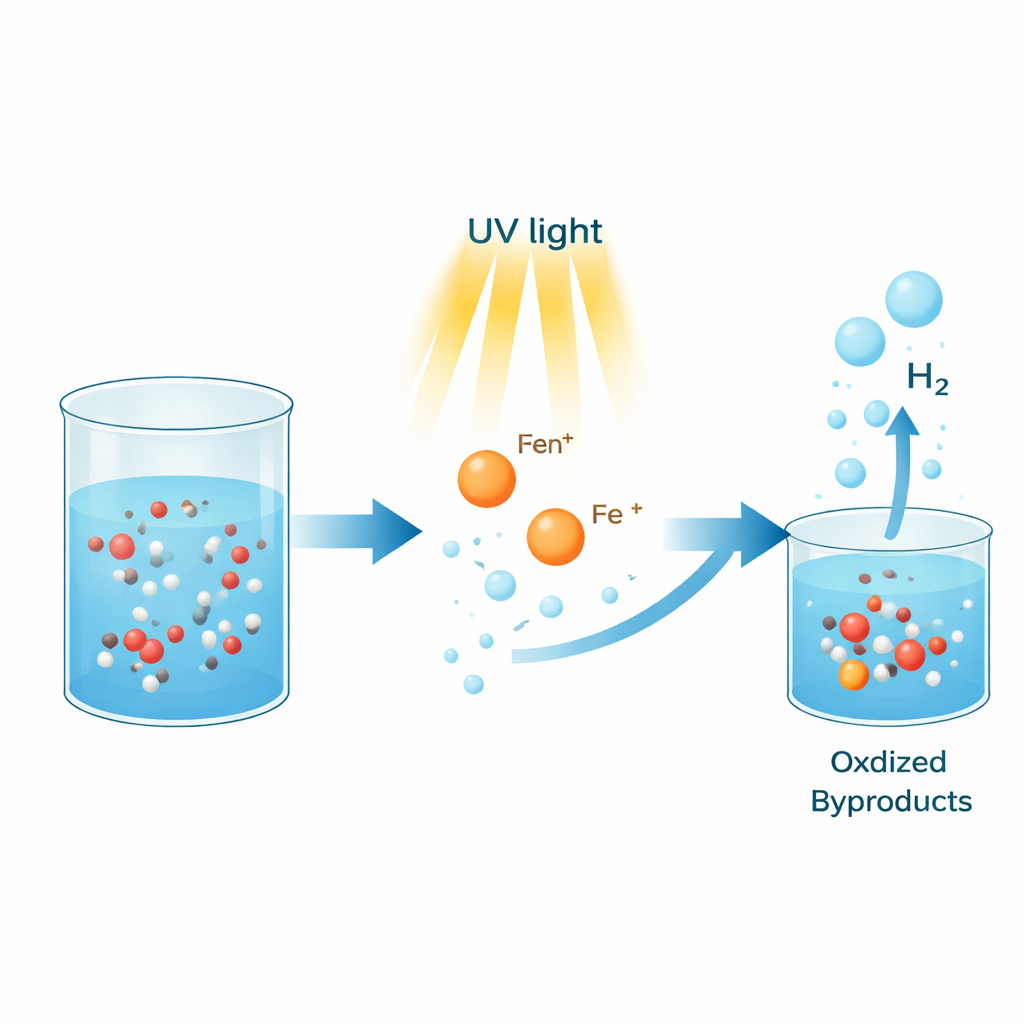
Transformer un alcool liquide en un gaz utile
Les chercheurs se sont concentrés sur le méthanol, un liquide courant qui contient déjà beaucoup d’hydrogène de façon compacte. Si l’on peut extraire l’hydrogène du méthanol de manière efficace, ce liquide peut servir de vecteur d’hydrogène facile à manipuler pour des piles à combustible et d’autres appareils. Les méthodes traditionnelles reposent sur des composés métalliques complexes ou des catalyseurs solides contenant des éléments rares comme le platine, le ruthénium ou l’iridium, et exigent souvent des températures élevées. En revanche, ce travail montre qu’un simple sel de fer, dissous dans le méthanol et aidé par une petite quantité de base, peut libérer de l’hydrogène lorsque le mélange est éclairé par des rayons ultraviolets.
Comment la lumière et le fer agissent ensemble
Dans le nouveau système, des ions fer en solution s’attachent à des molécules de méthanol proches. La lumière ultraviolette est absorbée par ces paires fer–alcool, provoquant un déplacement de charge interne : des électrons se déplacent depuis la partie alcool vers le centre ferrique. Cette étape induite par la lumière transforme le fer(III) en fer(II) et crée des fragments d’alcool très réactifs appelés radicaux. Ces fragments de courte durée de vie aident à scinder le méthanol et à associer des atomes d’hydrogène pour former du dihydrogène, tandis que la partie carbonée du méthanol est laissée sous une forme plus oxydée comme le formaldéhyde ou l’acide formique. Les expériences de l’équipe ont également montré que la réaction nécessite à la fois la lumière et l’oxygène de l’air pour se poursuivre ; sous azote, aucun hydrogène n’est formé, ce qui indique que l’oxygène participe discrètement à la réinitialisation de certaines parties du système. 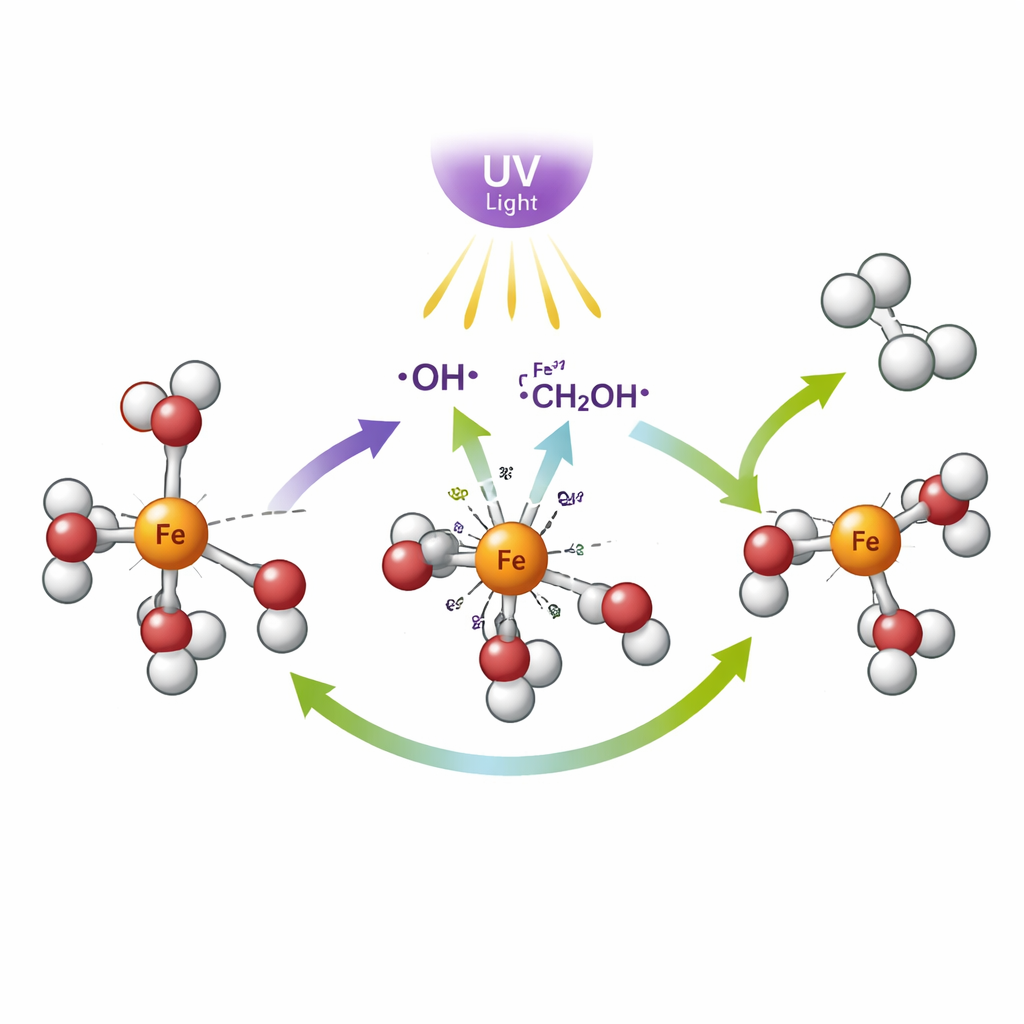
Régler la réaction et tester ses limites
Parce que le dispositif est si simple, les auteurs ont pu étudier facilement ce qui le rend optimal. L’ajout d’hydroxyde de sodium, une base courante, augmente fortement la réaction en aidant à convertir le méthanol en une forme plus réactive qui se lie plus fortement au fer. La mesure de la vitesse de réaction en fonction de la concentration en base a révélé un comportement de saturation similaire à celui observé pour les enzymes, suggérant une étape d’ajustement initiale rapide suivie d’une étape plus lente contrôlée par la lumière. La quantité d’hydrogène produite dépend aussi de la concentration en fer et de l’intensité lumineuse : des concentrations en fer plus faibles et une illumination UV plus intense donnent une plus grande efficacité par ion fer. La réaction se poursuit de façon stable pendant plusieurs jours, peut être modestement montée en échelle, et la même solution de fer peut être réutilisée plusieurs fois sans perte d’activité majeure.
Au-delà du méthanol : autres alcools et biomasse
L’équipe a exploré si cette approche lumière–fer pouvait traiter d’autres substrats. Ils ont constaté que des alcools simples comme l’éthanol, le 1-propanol et le 2-propanol produisaient également de l’hydrogène, bien que moins efficacement que le méthanol, probablement parce que des molécules plus encombrantes sont plus difficiles à déshydrogéner. Lorsque de l’eau a été ajoutée, la réaction a ralenti mais a continué à produire de l’hydrogène à des débits comparables à ceux de certains photocatalyseurs solides rapportés dans la littérature. Fait particulièrement remarquable, le système a même pu générer de l’hydrogène à partir de sources renouvelables plus complexes comme le glucose, la cellobiose, l’amidon, la cellulose et la poudre de bois, bien que les vitesses aient été bien plus faibles et que les matériaux solides n’aient été que légèrement modifiés.
Ce que cela signifie pour l’énergie de demain
Dans l’ensemble, l’étude montre que quelque chose d’aussi basique qu’un sel de fer dissous peut rivaliser avec des catalyseurs bien plus élaborés pour convertir le méthanol en hydrogène sous lumière. Le procédé dépend encore de la lumière ultraviolette et fonctionne mieux avec peu d’eau, il n’est donc pas encore prêt à remplacer les méthodes industrielles existantes. Toutefois, son faible coût, sa simplicité et sa capacité à traiter une gamme d’alcools et de biomasses suggèrent une piste nouvelle pour la recherche sur les carburants propres. En démontrant que de simples ions fer en solution peuvent agir comme catalyseurs efficaces activés par la lumière, ce travail ouvre la voie à des conceptions plus épurées pour la production d’hydrogène à partir de matières premières renouvelables.
Citation: Sakurai, M., Kawasaki, Y., Itabashi, Y. et al. Iron ion enables photocatalytic hydrogen evolution from methanol. Commun Chem 9, 151 (2026). https://doi.org/10.1038/s42004-026-02009-3
Mots-clés: production d’hydrogène photocatalytique, déshydrogénation du méthanol, catalyseurs à base de fer, carburants solaires, vecteurs d’hydrogène liquides