Clear Sky Science · it
Il ginsenoside Rg1 attenua i comportamenti depressivi indotti da lipopolisaccaride nei topi riducendo la neuroinfiammazione e i danni neuronali
Perché questo conta per l’umore e la salute cerebrale
La depressione colpisce centinaia di milioni di persone nel mondo, eppure molti antidepressivi attuali agiscono lentamente e possono provocare effetti collaterali rilevanti. Questo studio esplora se un ingrediente naturale del ginseng, chiamato ginsenoside Rg1, possa alleviare i sintomi depressivi nei topi calmando l’infiammazione cerebrale e proteggendo i neuroni vulnerabili. Il lavoro offre una finestra su come l’infiammazione, i circuiti cerebrali coinvolti nell’umore e nuove idee terapeutiche possano essere collegati.
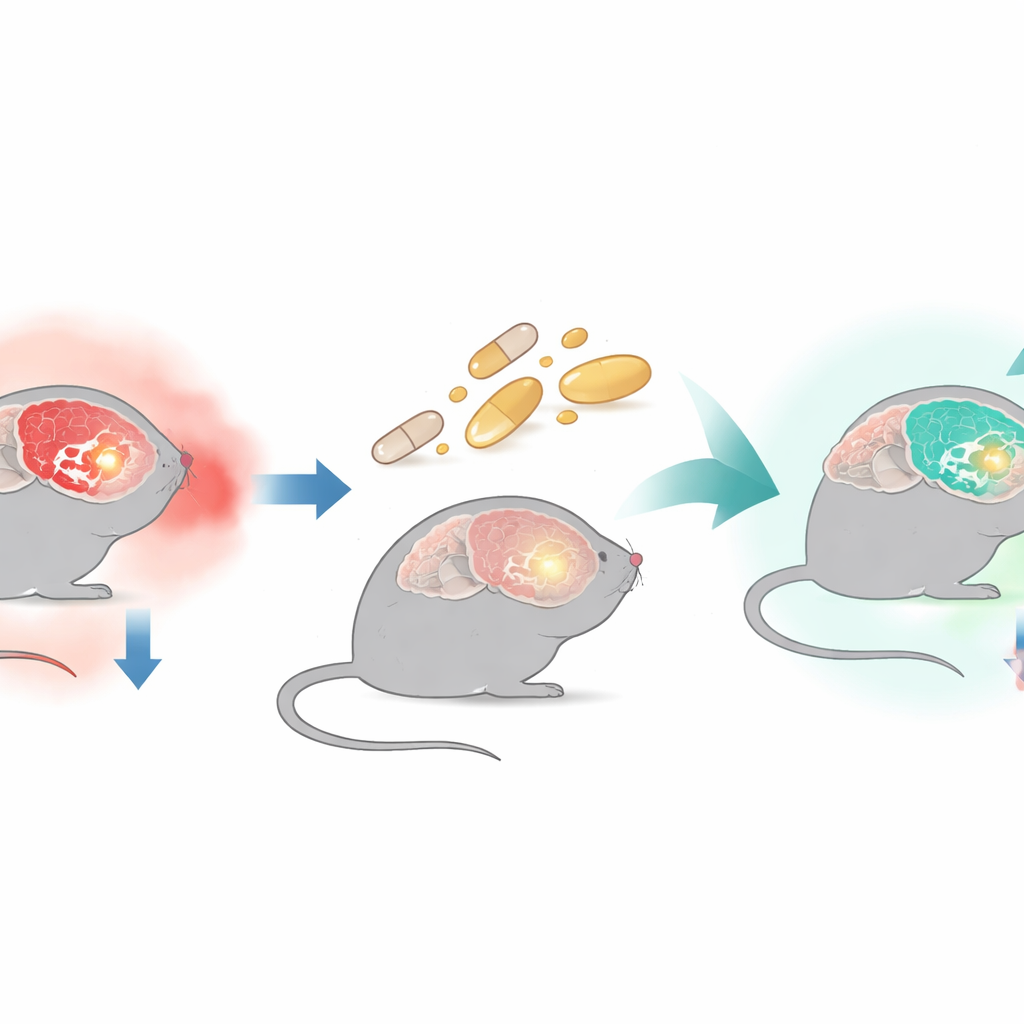
Ginseng, infiammazione e umore basso
Gli scienziati sospettano da tempo che l’infiammazione cerebrale possa contribuire a scatenare o peggiorare la depressione. In questo studio i ricercatori si sono concentrati sull’ippocampo, una regione cerebrale profondamente coinvolta nella memoria e nelle emozioni e nota per atrofizzarsi o perdere cellule in molte persone con depressione. Hanno usato una sostanza batterica chiamata lipopolisaccaride (LPS) per scatenare una forte infiammazione direttamente nel cervello dei topi. Questa singola iniezione ha prodotto in modo affidabile cambiamenti duraturi che assomigliano alla depressione umana, inclusa la riduzione del piacere, un aumento dei comportamenti di tipo disperazione e una maggiore evitazione di spazi aperti con ansia correlata.
Testare un protettore cerebrale naturale
Dopo l’innesco dell’infiammazione, i topi hanno ricevuto dosi giornaliere di ginsenoside Rg1 per quattro settimane, a dose bassa o alta. Per confronto, un altro gruppo ha ricevuto fluoxetina, un antidepressivo ampiamente usato. Gli animali sono poi stati sottoposti a test comportamentali standard: il test dello swim forzato per valutare l’immobilità di tipo disperazione, il test della preferenza per il saccarosio per misurare la perdita di piacere e l’elevated plus maze per valutare ansia e propensione all’esplorazione. I topi trattati solo con LPS hanno trascorso più tempo immobili, hanno evitato l’acqua zuccherata e hanno evitato i bracci aperti del labirinto. Al contrario, i topi trattati con Rg1 o fluoxetina hanno mostrato tempi di immobilità significativamente più brevi, maggiore interesse per il saccarosio e maggiore esplorazione, suggerendo che Rg1 ha attenuato i comportamenti depressivi e ansiosi.
Proteggere le cellule cerebrali dai danni
Per capire cosa accadeva all’interno del cervello, i ricercatori hanno esaminato l’ippocampo al microscopio. Nei topi infiammati, i neuroni ippocampali risultavano disorganizzati, meno numerosi e presentavano segni di atrofia e vacuoli — piccole cavità indicative di danno cellulare. Colorazioni specifiche che evidenziano i neuroni sani hanno rilevato una diminuzione delle cellule nervose mature, e la microscopia elettronica ha mostrato mitocondri ingrossati e danneggiati, le centrali energetiche delle cellule. Il trattamento con Rg1 ha migliorato in modo evidente questi aspetti: i neuroni erano più ordinati, le strutture più intatte e il danno mitocondriale ridotto, soprattutto alla dose più alta. Anche i livelli di molecole infiammatorie chiave nel cervello, in particolare TNF-α e IL‑1β, sono stati riportati verso valori normali, suggerendo che Rg1 attenua l’infiammazione e protegge i neuroni dai suoi effetti dannosi.
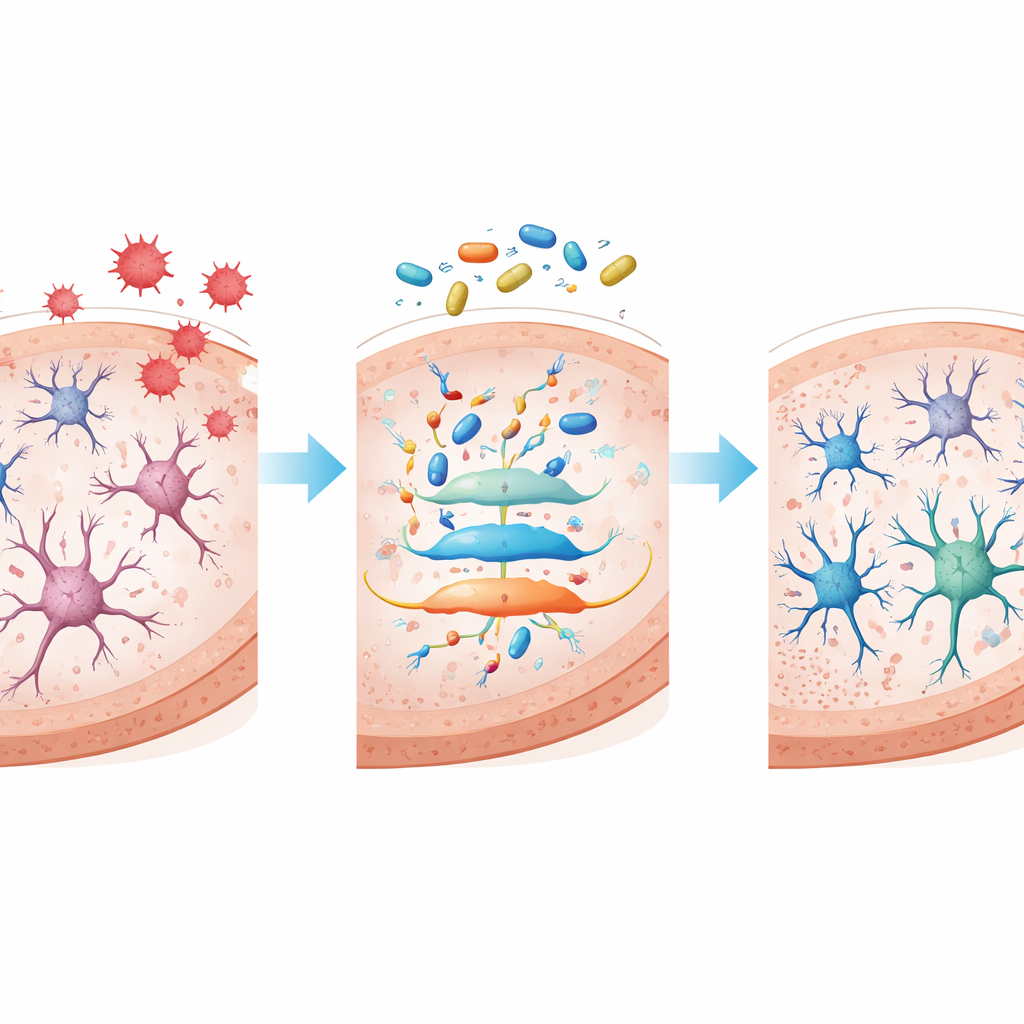
Indagare un interruttore di controllo nascosto nelle cellule cerebrali
Oltre ai danni visibili, il team voleva sapere quali sistemi di controllo interni alle cellule cerebrali stessero cambiando. Hanno utilizzato l’analisi proteomica — un approccio che esamina migliaia di proteine contemporaneamente — per confrontare tessuto ippocampale di topi sani, topi infiammati e topi infiammati trattati con alta dose di Rg1. Tra migliaia di proteine, è emersa una rete predominante: la via di segnalazione Hippo–YAP, un centro di controllo molecolare che regola se le cellule crescono, sopravvivono o muoiono. Nei topi infiammati, proteine chiave della via Hippo–YAP risultavano eccessivamente attivate tramite fosforilazione, una modifica chimica che può alterare la segnalazione normale. Il trattamento con Rg1 ha invertito questo pattern, riducendo la fosforilazione e ripristinando un equilibrio più sano in questa via.
Cosa potrebbe significare per trattamenti futuri
Nel complesso, i risultati suggeriscono che il ginsenoside Rg1 può ridurre i comportamenti di tipo depressivo nei topi calmando l’infiammazione cerebrale, preservando i neuroni ippocampali e normalizzando una via di controllo della crescita e sopravvivenza all’interno delle cellule cerebrali. Sebbene resti molto lavoro prima di poter considerare un simile composto per l’uso umano, lo studio rafforza l’idea che mirare all’infiammazione e alle vie di protezione cellulare nel cervello possa offrire nuove strade per trattare la depressione oltre i farmaci antidepressivi tradizionali.
Citazione: Zhang, L., Tang, J., Fang, Z. et al. Ginsenoside Rg1 ameliorates lipopolysaccharide-induced depressive-like behaviors in mice by attenuating neuroinflammation and neuronal damage. Sci Rep 16, 11948 (2026). https://doi.org/10.1038/s41598-026-41622-z
Parole chiave: depressione, neuroinfiammazione, ginsenoside Rg1, ippocampo, via Hippo YAP