Clear Sky Science · it
Progettazione, caratterizzazione, studi DFT e docking molecolare di nuovi ibridi benzofurano–pirazol-acrilamide come agenti insetticidi contro Spodoptera littoralis e Tribolium castaneum
Nuove armi per proteggere le colture alimentari
Gli agricoltori di tutto il mondo combattono una battaglia continua contro gli insetti che divorano le foglie nei campi e i cereali nelle riserve. Due colpevoli particolarmente dannosi sono la tignola del cotone egiziana e il tribolio della farina, che insieme possono distruggere porzioni consistenti dei raccolti e contaminare la farina immagazzinata. Questo articolo descrive la progettazione e la prova di una nuova famiglia di molecole sintetiche che mirano a uccidere questi parassiti in modo più mirato, prendendo di mira il loro sistema nervoso, offrendo al contempo il potenziale per rischi inferiori per le persone e per l’ambiente.
Perché questi parassiti sono un problema così grave
La tignola del cotone egiziana si nutre di dozzine di colture, dal cotone ai pomodori, dal grano alle fragole, e può ridurre le rese fino alla metà. Il tribolio della farina, intanto, prospera in magazzini di cereali e mulini caldi, trasformando cibo prezioso in polvere contaminata che oltre a emanare odori sgradevoli può comportare rischi per la salute. Gli insetticidi esistenti sono spesso ad ampio spettro, possono danneggiare organismi non bersaglio e stanno perdendo efficacia man mano che gli insetti sviluppano resistenza. Esiste una forte spinta a trovare nuove sostanze che agiscano in modi più specifici, così da poter usare dosi più basse e ridurre effetti collaterali indesiderati.
Costruire un nuovo tipo di molecola insetticida
Il gruppo di ricerca ha creato otto composti correlati che combinano tre matrici consolidate spesso presenti nei farmaci: un anello benzofurano, un anello pirazolo e un gruppo acrilamide. Unendo questi frammenti in un unico scheletro e variando in modi diversi un anello sostituente, hanno generato una piccola “famiglia” di candidati. Hanno quindi usato strumenti standard della chimica—spettroscopia infrarossa e risonanza magnetica nucleare e spettrometria di massa—per confermare che ogni prodotto avesse la struttura prevista. Parallelamente al lavoro di laboratorio, hanno impiegato calcoli avanzati per esplorare come la forma tridimensionale e la distribuzione elettronica di ciascun composto cambino quando una parte chiave della molecola ruota tra due disposizioni speculari, note come forme E e Z.
Mettere alla prova i nuovi composti
Successivamente, gli scienziati hanno misurato la tossicità dei composti sulle larve allo stadio quattro della tignola del cotone e sugli adulti del tribolio della farina. Gli insetti sono stati esposti a diverse dosi su superfici trattate e i decessi sono stati registrati nell’arco di tre giorni. Tre molecole—etichettate 3a, 3b e 3c—si sono distinte, causando elevata mortalità in entrambe le specie, mentre le altre si sono rivelate deboli o inattive. Tra queste, 3a è risultata la più potente contro la tignola, e 3b la più efficace contro il tribolio, ottenendo la completa eliminazione alla dose massima testata entro 72 ore. Confrontando le piccole modifiche chimiche tra i membri attivi e quelli inattivi della serie, il team ha scoperto che l’aggiunta di gruppi elettron-donatori, come metile o metossile, in una posizione specifica aumentava l’attività insetticida, mentre gruppi fortemente elettron-attrattori, come nitro o carbossile, la sopprimevano in larga misura.
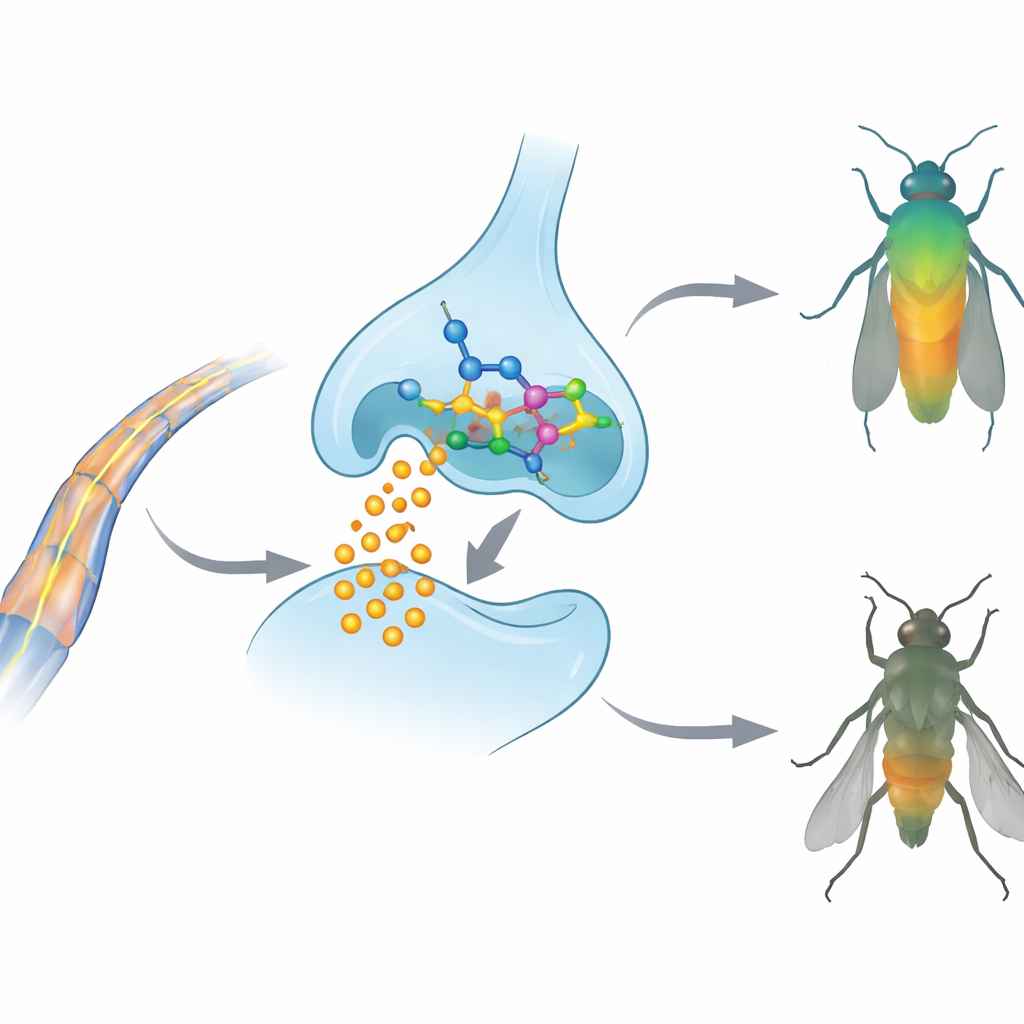
Uno sguardo all’interno del sistema nervoso degli insetti
Per capire il meccanismo d’azione, gli autori hanno utilizzato modelli al computer dell’acetilcolinesterasi, un enzima chiave che interrompe i segnali nervosi degradando un neurotrasmettitore chiamato acetilcolina. Molti insetticidi classici disattivano questo enzima. Attraverso il docking molecolare, il team ha simulato come i composti 3a, 3b e 3c si inseriscano nell’acetilcolinesterasi di entrambe le specie bersaglio. Tutti e tre erano predetti legarsi saldamente nella tasca attiva tramite una rete di contatti idrofobici e legami idrogeno, con affinità di legame simili o superiori rispetto a un insetticida di riferimento largamente usato. Ulteriori simulazioni di dinamica molecolare, che seguono il moto degli atomi nel tempo, hanno mostrato che il complesso tra il composto 3b e l’enzima rimane stabile e compatto, suggerendo un effetto di bloccaggio persistente. Allo stesso tempo, lo screening ADMET basato su computer (assorbimento, distribuzione, metabolismo, escrezione e tossicità) ha indicato che queste molecole rispettano comuni regole di “drug‑likeness” e sono improbabili siano fortemente mutagene o cancerogene, sebbene la loro natura lipofila possa limitare formulazioni semplici a base d’acqua.
Cosa rivelano i calcoli elettronici
La teoria del funzionale della densità, un approccio di modellizzazione a livello quantistico, è stata impiegata per sondare perché piccole modifiche strutturali causino grandi differenze. I calcoli hanno mostrato che per alcuni membri della serie, in particolare il composto 3c, la forma E presenta un gap energetico molto piccolo tra orbitali chiave che trattengono elettroni, rendendola altamente reattiva e un forte accettore elettronico. Altri membri, come 3b, risultavano preferire la forma Z, che offriva un migliore allineamento degli elettroni e momenti di dipolo maggiori. Queste sottili caratteristiche elettroniche influenzano quanto bene una molecola possa interagire con il bersaglio enzimatico o con le superfici, e aiutano a spiegare perché certe varianti si leghino più saldamente anche se non sono le più reattive sulla carta. In questo modo lo studio collega la forma e la distribuzione di carica di una molecola al suo impatto biologico.
Dove potrebbe portare questo lavoro
Complessivamente, lo studio individua un piccolo gruppo di ibridi benzofurano–pirazolo–acrilamide, in particolare i composti 3a, 3b e 3c, come promettenti lead per nuovi insetticidi contro due parassiti di rilevanza economica. I saggi di laboratorio mostrano che possono uccidere bruchi e coleotteri a concentrazioni relativamente basse, e i modelli al computer suggeriscono che agiscono bloccando saldamente un enzima nervoso vitale pur presentando caratteristiche di sicurezza accettabili. Sebbene siano necessari molti altri test in condizioni reali e su organismi non bersaglio, questi risultati delineano un percorso razionale per progettare agenti di controllo dei parassiti di nuova generazione che siano potenti e più finemente mirati ai propri bersagli.
Citazione: El-Bana, G.G., Fouad, M.R., Deeb, A.D.H. et al. Design, characterization, DFT studies, and molecular docking of new benzofuran–pyrazol-acrylamide hybrids as insecticidal agents against Spodoptera littoralis and Tribolium castaneum. Sci Rep 16, 10344 (2026). https://doi.org/10.1038/s41598-026-39839-z
Parole chiave: progettazione di insetticidi, inibitori dell’acetilcolinesterasi, controllo dei parassiti delle colture, ibridi benzofurano pirazolo, tossicologia computazionale