Clear Sky Science · it
Deconvoluzione doppia nella microscopia a illuminazione strutturata multiphoton per immagini super-risolute in tessuti profondi
Vedere più in profondità nei tessuti vivi
La biologia moderna dipende spesso dalla possibilità di osservare i dettagli più minuti all’interno di campioni spessi, come sezioni cerebrali o embrioni in sviluppo. Sfortunatamente, mentre la luce attraversa questi ambienti affollati viene rifratta e disturbata, rendendo le immagini sfocate proprio quando gli scienziati hanno più bisogno di visioni nitide. Questo articolo presenta un modo per "disfare" digitalmente tale sfocatura, permettendo a un microscopio avanzato standard di rivelare strutture estremamente fini in profondità nei tessuti senza aggiungere hardware costosi o complessi.
Perché l’imaging in profondità è così difficile
I microscopi a fluorescenza consentono ai ricercatori di marcare molecole specifiche e osservare come cellule e tessuti si costruiscono e si comportano. Negli ultimi decenni, diversi metodi di “super-risoluzione” hanno superato i limiti tradizionali di nitidezza, rivelando dettagli ben al di sotto dei 200 nanometri. Tuttavia, la maggior parte di questi metodi funziona bene solo vicino alla superficie del campione. In tessuti spessi, come il cervello di topo, sia la luce usata per eccitare i marcatori fluorescenti sia la luce emessa verso il rivelatore vengono distorte da piccole variazioni nella struttura del tessuto. Queste deformazioni, chiamate aberrazioni, sfocano il fuoco del microscopio ed eliminano le informazioni ad alta risoluzione, soprattutto a profondità superiori a qualche decina di micrometri.
Dalle soluzioni hardware a un approccio software
Un modo comune per combattere le aberrazioni è l’ottica adattiva hardware, che usa specchi mobili o altri dispositivi per rimodellare il fronte d’onda della luce e ripristinare un fuoco nitido. Pur essendo potenti, questi sistemi sono costosi, tecnicamente impegnativi e spesso correggono solo una lunghezza d’onda o una direzione di viaggio della luce alla volta. Gli autori propongono invece un approccio computazionale che funziona con un tipo di microscopio già diffuso in molti laboratori: il microscopio multiphoton a scansione laser. Sostituendo il consueto singolo rivelatore di luce con una camera, registrano una ricca pila di immagini scansionate che codifica come sia la luce di eccitazione in ingresso sia la fluorescenza in uscita sono state distorte dal tessuto.
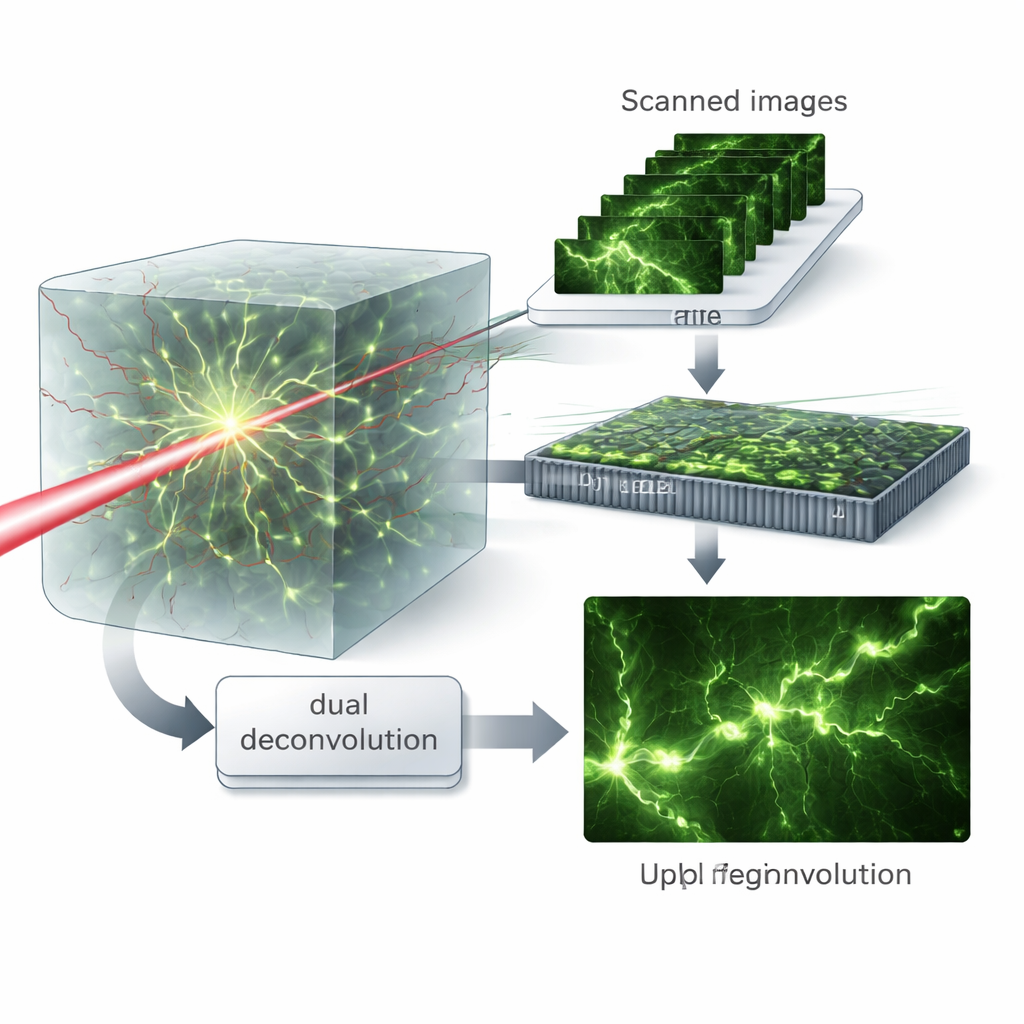
Pattern virtuali e pulizia doppia
L’intuizione chiave è trattare le immagini scansionate come se il campione fosse stato illuminato con molti diversi pattern luminosi fini, un concetto che gli autori chiamano illuminazione strutturata virtuale. Ricombinando matematicamente questi dati nel dominio delle frequenze si riesce a separare i ruoli dei processi di eccitazione e di emissione. Introducono quindi un algoritmo di “deconvoluzione doppia” che stima e corregge alternativamente la sfocatura da ciascun lato — la luce in ingresso e la luce in uscita — invece di sommarle in un’unica blur effettiva. Questo trattamento matriciale preserva più dettagli ad alta frequenza e permette all’algoritmo di recuperare strutture fini anche quando le aberrazioni sono intense.
Visioni più nitide in simulazioni e campioni reali
Per testare il loro metodo, il team ha prima utilizzato simulazioni al computer della microscopia a due fotoni, una tecnica di imaging profondo che usa coppie di fotoni a energia più bassa per eccitare la fluorescenza solo nel punto di fuoco. Sotto severe distorsioni simulate, le ricostruzioni convenzionali a due fotoni e le ricostruzioni con illuminazione strutturata standard hanno prodotto immagini visibilmente sfocate. Al contrario, la deconvoluzione doppia ha ripristinato pattern nitidi la cui risoluzione si avvicinava a un quarto della lunghezza d’onda della fluorescenza — circa 130 nanometri — in accordo con le aspettative teoriche. Gli autori hanno poi costruito un apparato a due fotoni personalizzato con una camera scientifica e hanno applicato il loro algoritmo a campioni reali, inclusi microsfere fluorescenti, pattern di prova nascosti dietro strati diffusivi, cellule in coltura, tessuto cerebrale di topo e zebrafish interi montati. Ripetutamente, strutture che apparivano sfumate o raddoppiate nelle immagini convenzionali sono emerse come caratteristiche chiaramente separate dopo l’elaborazione, e elementi neuronali fini come le spine dendritiche sono rimasti risolvibili a profondità fino a 180 micrometri nel cervello di topo.
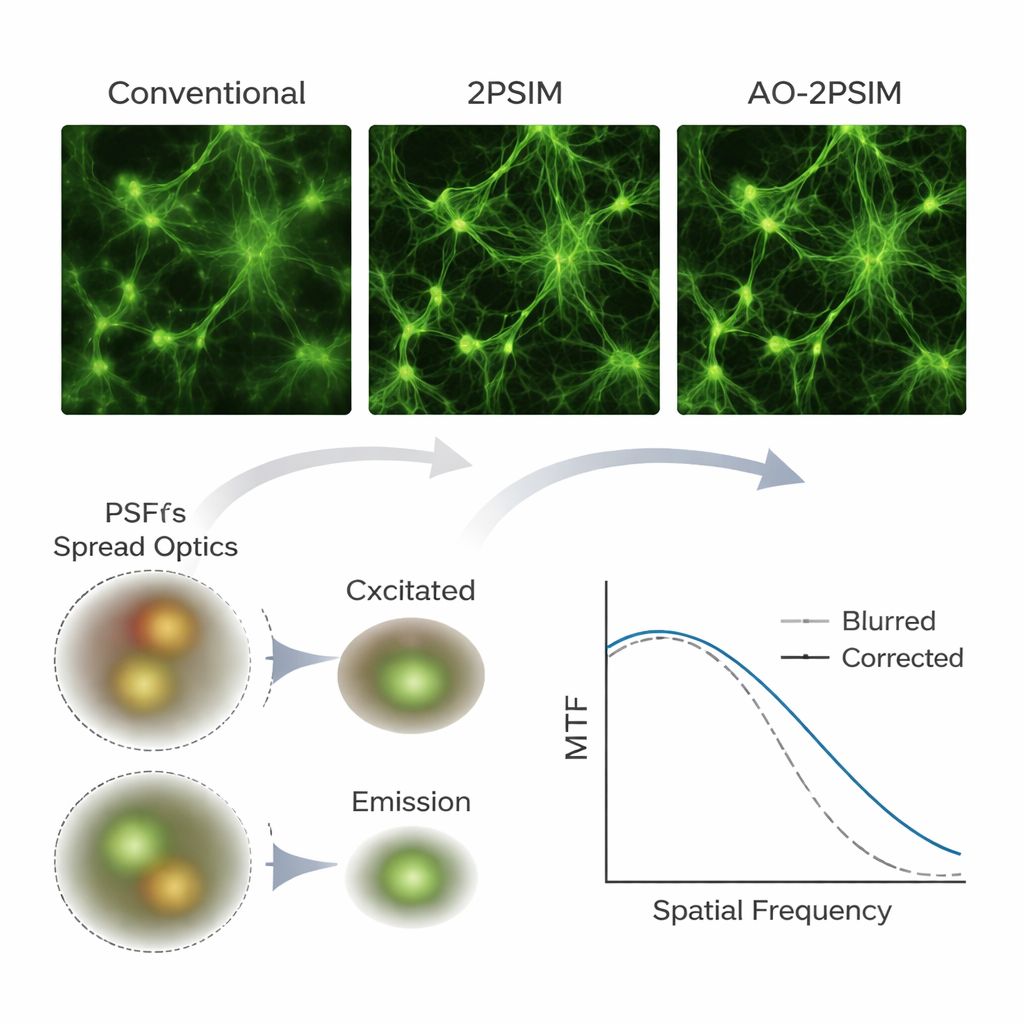
Cosa significa per l’imaging biologico
Per i non specialisti, il messaggio principale è che gli autori hanno mostrato come trasformare i microscopi multiphoton esistenti in strumenti di imaging in tessuti profondi molto più potenti utilizzando principalmente software e un aggiornamento alla camera. Modellando e correggendo con cura come i tessuti deviano la luce sia in ingresso sia in uscita, l’approccio di deconvoluzione doppia raddoppia il limite di risoluzione abituale in campioni spessi e difficili senza fare affidamento su specchi adattivi complessi. Pur dipendendo ancora dalla raccolta di segnale sufficiente e richiedendo attualmente scansioni relativamente lente, offre una via pratica e conveniente verso viste tridimensionali ultra-nitide del cervello e di altri organi, aprendo la strada a studi più dettagliati su come le strutture biologiche sono organizzate e cambiano nel tempo.
Citazione: Lim, S., Kang, S., Hong, J.H. et al. Dual deconvolution in multiphoton structured illumination microscopy for deep-tissue super-resolution imaging. Nat Commun 17, 2123 (2026). https://doi.org/10.1038/s41467-026-69798-y
Parole chiave: microscopia super-risoluta, imaging a due fotoni, ottica adattiva, imaging in tessuti profondi, imaging computazionale