Clear Sky Science · it
La disinibizione dell’area tegmentale ventrale durante l’apprendimento iniziale della punizione causa un’insensibilità alla punizione duratura
Perché a volte ignoriamo le conseguenze negative
La maggior parte di noi impara rapidamente a smettere di fare cose che arrecano dolore o problemi. Eppure alcune persone, e molti animali, continuano a inseguire ricompense anche quando il costo è elevato, come nella dipendenza o nelle decisioni rischiose. Questo studio indaga cosa accade all’interno di un centro chiave della ricompensa nel cervello nei primi istanti in cui apprendiamo che un’azione ha conseguenze dolorose, e come interrompere quel processo possa lasciarci ostinatamente insensibili alla punizione molto tempo dopo che il pericolo è stato chiarito.
Un nodo cerebrale per valutare ricompensa e danno
Nel profondo del mesencefalo si trova l’area tegmentale ventrale, una piccola regione le cui cellule che rilasciano dopamina diffondono potenti “segnali di insegnamento” sulle ricompense. Questi neuroni esplodono di attività quando gli eventi risultano migliori del previsto e si silenziano quando gli esiti sono peggiori. Sono circondati da cellule inibitorie che usano il neurotrasmettitore GABA per spegnere brevemente l’output dopaminergico. Le teorie classiche sostengono che questa inibizione aiuti gli animali a imparare ad evitare azioni dannose. Tuttavia, i ricercatori non sapevano esattamente come si comportino i segnali di GABA e dopamina in questa regione durante la punizione, né se il breve spegnimento delle cellule dopaminergiche sia realmente necessario per apprendere a tenersi lontani dal pericolo.
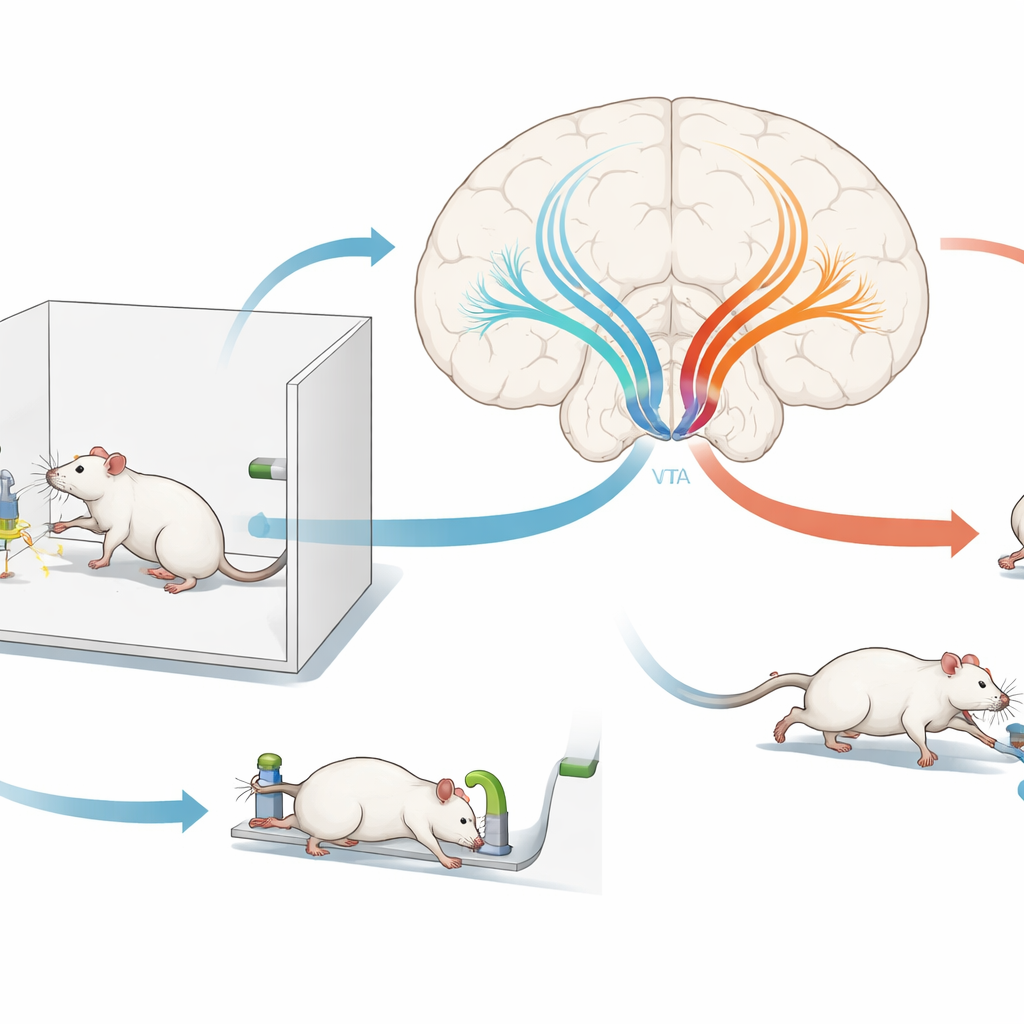
Osservare i segnali di punizione in tempo reale
Gli autori hanno addestrato ratti a premere due leve per ottenere cibo. Successivamente, le pressioni su una leva causarono anche una lieve scossa elettrica, trasformando quell’azione in una scelta punita, mentre l’altra leva rimase sicura. Usando strumenti di registrazione fibra-ottica, il team ha misurato l’attività delle cellule dopaminergiche e l’input di GABA che esse ricevevano mentre gli animali sperimentavano scosse e ricompense e decidevano quale leva premere. Sia l’attività dopaminergica sia l’input di GABA mostrarono picchi brevi quando si verificavano cibo o scosse. Le cellule dopaminergiche rispondevano più intensamente al cibo, mentre l’input di GABA era particolarmente forte per le scosse durante la primissima sessione di punizione e poi diminuiva con l’esperienza. Attorno alle azioni stesse, i modelli di attività cambiarono in modo che le pressioni sulla leva punita cominciassero a evocare un’esplosione distinta di attività dopaminergica, mentre la leva sicura no. Questi schemi suggerivano che un’ondata di inibizione guidata dal GABA proprio quando la punizione è incontrata per la prima volta potrebbe essere un segnale di insegnamento cruciale.
Bloccare l’inibizione in una finestra critica
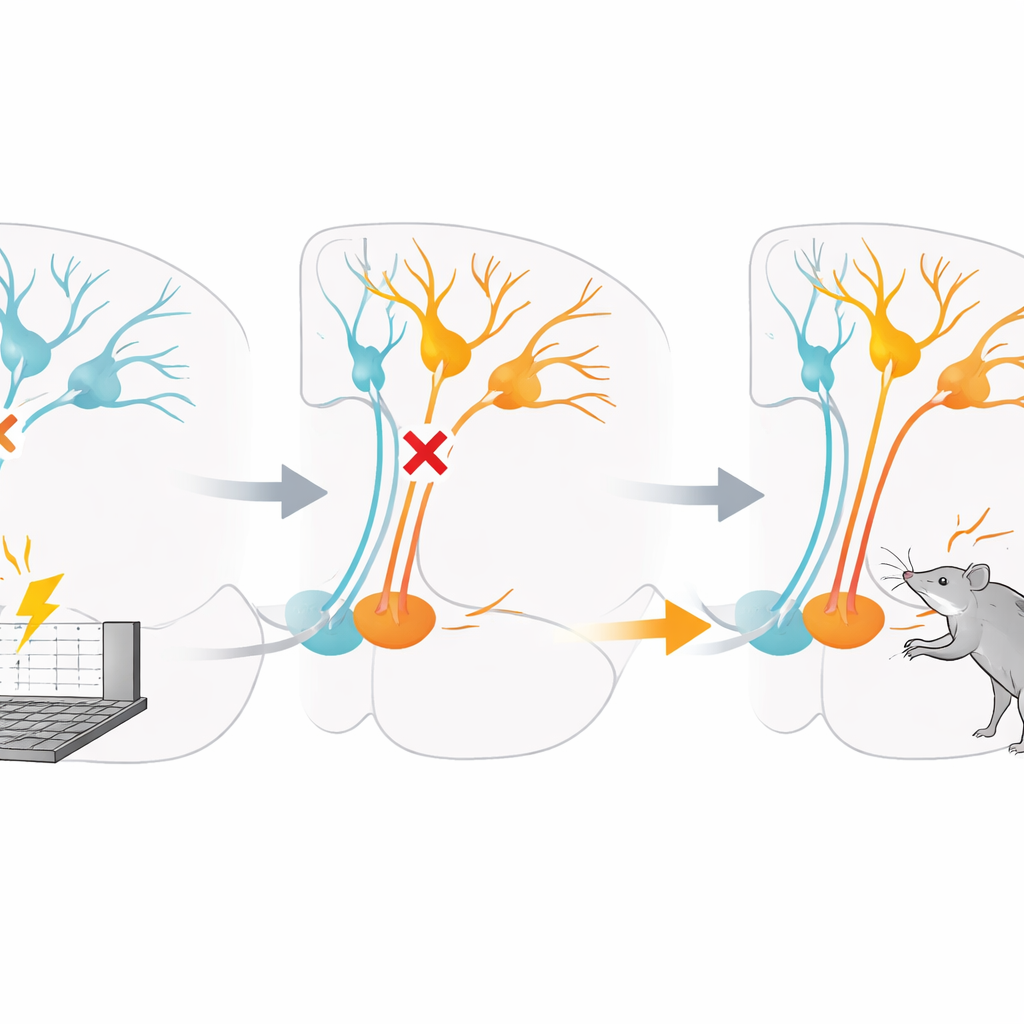
Per mettere alla prova questa idea, i ricercatori interferirono con la capacità del GABA di inibire le cellule nell’area tegmentale ventrale. In un gruppo di ratti infusero direttamente in questa regione un farmaco che bloccava i recettori GABA di tipo A durante le prime due sessioni di punizione. In un altro gruppo usarono una tecnica di recettori designer per eccitare artificialmente i neuroni dopaminergici durante le stesse sessioni iniziali. In entrambi i casi, l’effetto immediato fu che i ratti riducevano meno la pressione sulla leva punita rispetto agli animali di controllo e finirono per ricevere più scosse. Colpisce che, una volta trascorsa questa finestra iniziale, ripristinare la chimica cerebrale normale non risolvette il problema: anche nei giorni successivi senza farmaco, questi ratti continuavano a premere più facilmente la leva punita e esitavano meno prima di farlo.
Cambiamenti duraturi nel modo in cui il pericolo è valutato
Quando l’apprendimento della punizione era già ben consolidato, bloccare temporaneamente l’inibizione o eccitare i neuroni dopaminergici non produsse lo stesso danno duraturo. Le manipolazioni in quella fase successiva potevano spostare i livelli di attività complessivi, per esempio rendendo gli animali più o meno attivi, ma non cancellavano la tendenza appresa ad evitare la leva punita. Test aggiuntivi mostrarono che il trattamento non rendeva semplicemente le ricompense più attraenti in generale: la ricerca di cibo non punito non aumentò in modo coerente. Invece, la perturbazione sembrava interferire specificamente con il modo in cui il cervello collegava una particolare azione al suo esito doloroso durante quel primo incontro, lasciando gli animali con una cecità a lungo termine verso quel pericolo.
Cosa significa per le scelte rischiose nel mondo reale
Per un lettore non specialistico, la conclusione è che sembra esistere una finestra di apprendimento breve ma potente, proprio quando sperimentiamo per la prima volta che una scelta ha conseguenze dannose, durante la quale un’inibizione precisa in un hub di ricompensa del cervello ci insegna a fare un passo indietro. Se quel segnale inibitorio viene attenuato e l’attività dopaminergica rimane elevata, il cervello può non registrare correttamente il pericolo, producendo una tendenza duratura a continuare a fare la scelta rischiosa anche quando fa male. Poiché molte droghe che creano dipendenza aumentano la dopamina o riducono la sua inibizione, questi risultati suggeriscono un modo in cui tali sostanze potrebbero rimodellare il cervello verso abitudini persistenti e insensibili alla punizione — e lasciano intendere che proteggere o ripristinare questo segnale di insegnamento precoce potrebbe essere fondamentale per aiutare le persone a reimparare a evitare comportamenti dannosi.
Citazione: Tan, S.Y.S., Shen, M.H., Keevers, L.J. et al. Disinhibition of ventral tegmental area during initial punishment learning causes enduring punishment insensitivity. Neuropsychopharmacol. 51, 1045–1055 (2026). https://doi.org/10.1038/s41386-026-02368-4
Parole chiave: dopamina, apprendimento della punizione, area tegmentale ventrale, dipendenza, assunzione di rischi