Clear Sky Science · de
Dysinhibition des ventralen tegmentalen Areals während der anfänglichen Bestrafungslernung führt zu anhaltender Bestrafungsresistenz
Warum wir manchmal schlechte Folgen ignorieren
Die meisten von uns lernen schnell, mit schmerzhaften oder problematischen Handlungen aufzuhören. Dennoch verfolgen manche Menschen — und viele Tiere — weiter Belohnungen, selbst wenn die Kosten hoch sind, etwa bei Sucht oder riskanten Entscheidungen. Diese Studie fragt, was in einem wichtigen Belohnungszentrum des Gehirns in den ersten Momenten passiert, in denen wir lernen, dass eine Handlung schmerzhafte Konsequenzen hat, und wie eine Störung dieses Prozesses uns lange Zeit unempfänglich gegenüber Bestrafung machen kann, selbst wenn die Gefahr längst klar ist.
Ein Hirnzentrum zum Abwägen von Belohnung und Schaden
Tief im Mittelhirn liegt das ventrale tegmentale Areal, eine kleine Region, deren dopaminfreisetzende Zellen starke „Lehrsignale“ über Belohnungen aussenden. Diese Neuronen feuern auf, wenn Ereignisse besser als erwartet sind, und drosseln ihre Aktivität, wenn Outcomes schlechter ausfallen. Sie sind von inhibitorischen Zellen umgeben, die das Molekül GABA nutzen, um die Dopaminausschüttung kurzzeitig zu unterdrücken. Klassische Theorien besagen, dass diese Inhibition Tieren hilft, schädliche Handlungen zu vermeiden. Bislang war jedoch unklar, wie GABA- und Dopaminsignale in dieser Region während Bestrafung genau reagieren und ob die kurze Stummschaltung der Dopaminzellen wirklich notwendig ist, damit sich das Vermeidungsverhalten einstellt.
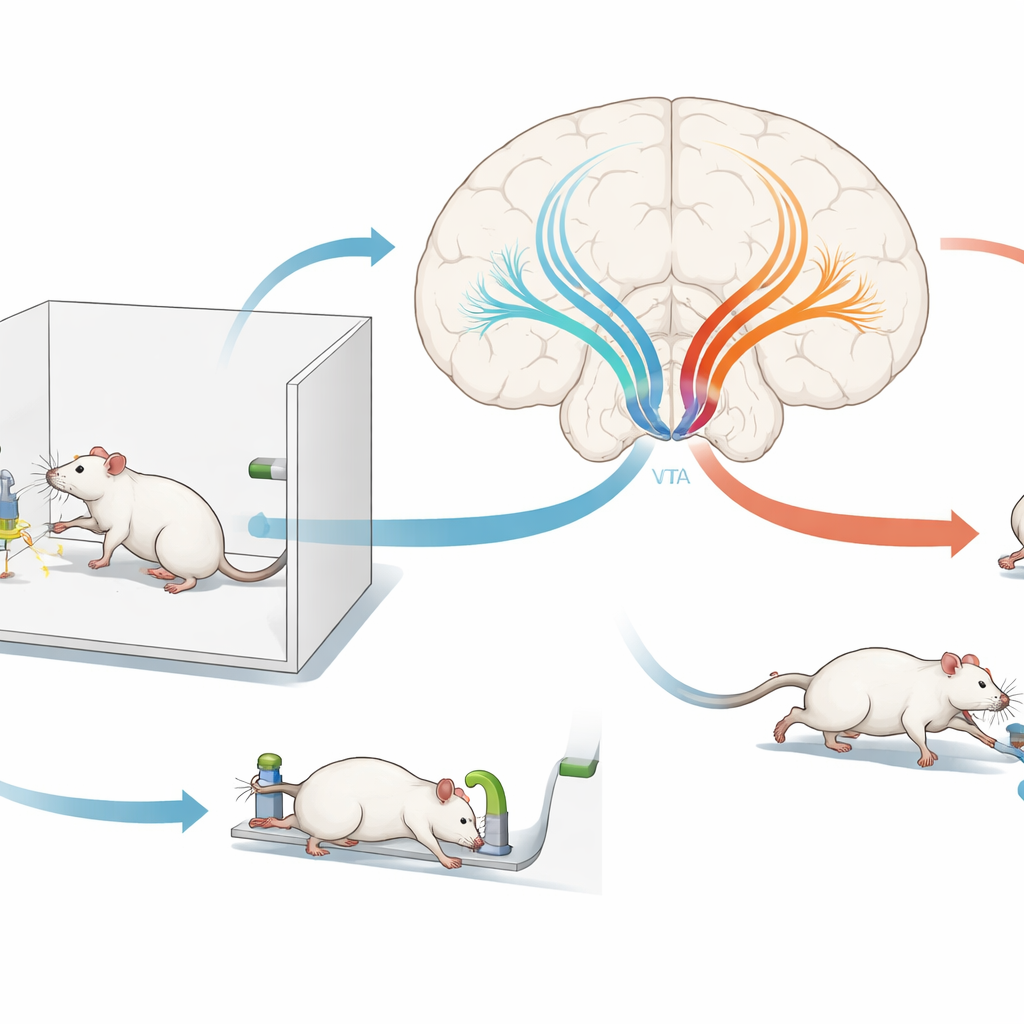
Bestrafungssignale in Echtzeit beobachten
Die Autorinnen und Autoren brachten Ratten bei, zwei Hebel für Futter zu drücken. Später lösten Drücke an einem Hebel zusätzlich einen leichten Elektroschock aus, wodurch diese Handlung bestraft wurde, während der andere Hebel sicher blieb. Mit faseroptischen Aufzeichnungsmethoden maßen die Forschenden die Aktivität der Dopaminzellen und den GABA-Eingang, den sie erhielten, während die Tiere Schocks und Belohnungen erlebten und sich für einen Hebel entschieden. Sowohl Dopaminaktivität als auch GABA-Eingang zeigten kurzzeitige Spitzen, wenn Futter oder Schock auftraten. Dopaminzellen reagierten stärker auf Futter, während der GABA-Eingang besonders stark auf Schocks während der allerersten Bestrafungssitzung war und mit der Erfahrung abschwächte. Rund um die Handlungen verschoben sich die Aktivitätsmuster so, dass Drücke am bestraften Hebel eine charakteristische Dopaminbombe hervorriefen, während der sichere Hebel dies nicht tat. Diese Muster deuteten darauf hin, dass ein GABA-getriebener Inhibitionsschub genau dann, wenn Bestrafung erstmals auftritt, ein wesentliches Lehrsignal sein könnte.
Inhibition während eines kritischen Zeitfensters blockieren
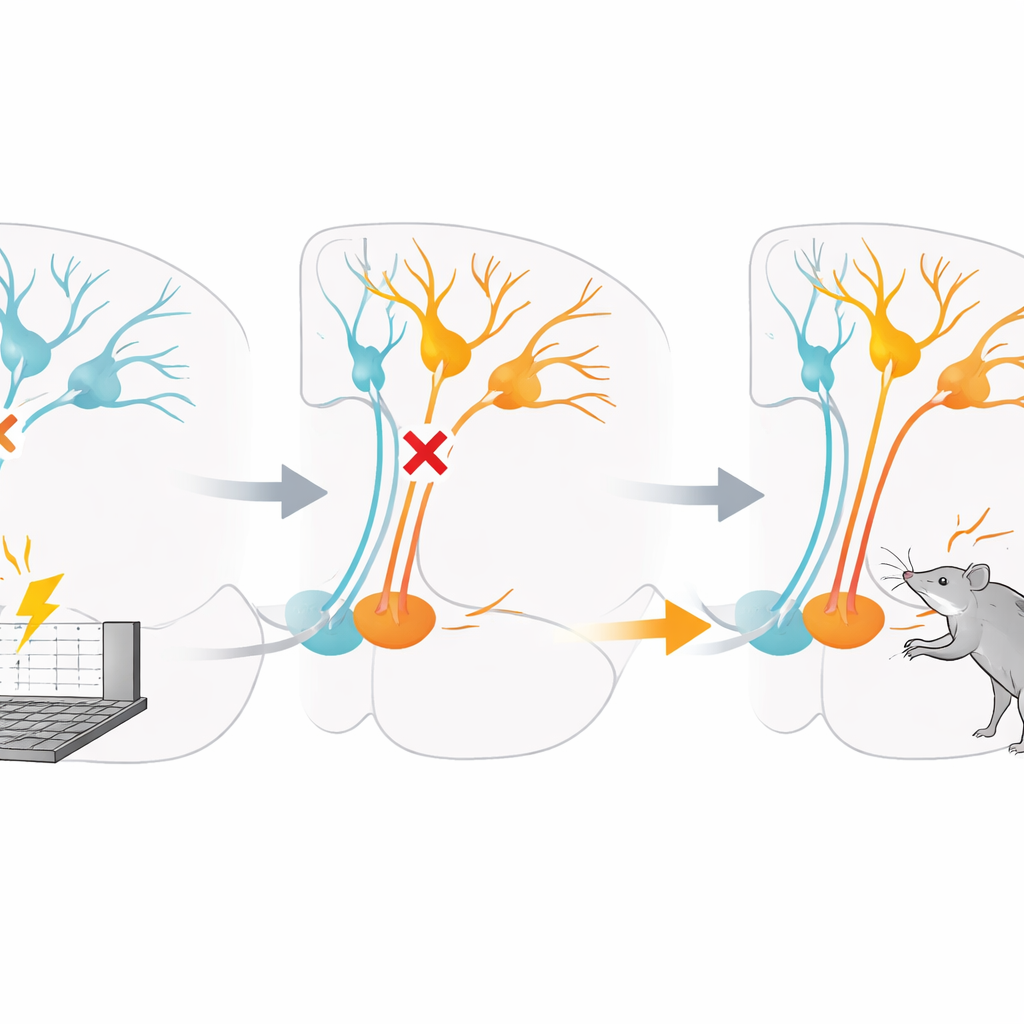
Um diese Idee zu prüfen, störten die Forschenden anschließend GABAs Fähigkeit, Zellen im ventralen tegmentalen Areal zu hemmen. In einer Gruppe Ratten injizierten sie ein Medikament direkt in diese Region, das GABA-A-Rezeptoren während der ersten beiden Bestrafungssitzungen blockierte. In einer anderen Gruppe nutzten sie eine Designer-Rezeptor-Technik, um Dopaminneurone in denselben frühen Sitzungen künstlich zu erregen. In beiden Fällen war die unmittelbare Folge, dass die Ratten das Drücken des bestraften Hebels weniger reduzierten als Kontrolltiere und dadurch mehr Schocks erhielten. Auffällig war, dass nach Ablauf dieses frühen Fensters die Wiederherstellung der normalen Neurochemie das Problem nicht behob: Auch an späteren Tagen ohne Medikament drückten diese Ratten weiterhin häufiger den bestraften Hebel und zögerten weniger, bevor sie es taten.
Anhaltende Veränderungen in der Bewertung von Gefahr
Wenn das Bestrafungslernen bereits gut etabliert war, führte eine vorübergehende Blockade der Inhibition oder die Erregung von Dopaminzellen nicht mehr zu derselben bleibenden Schädigung. Manipulationen in diesem späteren Stadium konnten das allgemeine Aktivitätsniveau verändern, etwa indem Tiere insgesamt aktiver oder weniger aktiv wurden, aber sie löschten nicht die gelernte Tendenz, den bestraften Hebel zu meiden. Weitere Tests zeigten, dass die Behandlung nicht einfach Belohnungen allgemein attraktiver machte; das unbestrafte Nahrungssuchen nahm nicht konsistent zu. Stattdessen schien die Störung spezifisch die Verknüpfung einer bestimmten Handlung mit ihrer schmerzhaften Konsequenz beim ersten Zusammentreffen zu beeinträchtigen und hinterließ so eine langfristige Blindstelle gegenüber dieser Gefahr.
Was das für reale riskante Entscheidungen bedeutet
Für eine allgemeine Leserschaft lautet die Quintessenz: Es gibt offenbar ein kurzes, aber starkes Lernfenster — genau dann, wenn wir zum ersten Mal erleben, dass eine Wahl schädliche Folgen hat — in dem präzise Inhibition in einem Belohnungszentrum des Gehirns uns lehrt, Abstand zu halten. Wenn dieses inhibitorische Signal abgeschwächt ist und die Dopaminaktivität hoch bleibt, kann das Gehirn die Gefahr möglicherweise nicht richtig registrieren, was zu einer anhaltenden Neigung führt, die riskante Wahl weiterhin zu treffen, selbst wenn sie schadet. Da viele suchterzeugende Substanzen Dopamin steigern oder dessen Inhibition verringern, legen diese Befunde nahe, wie solche Substanzen das Gehirn auf persistente, bestrafungsresistente Gewohnheiten verdrahten könnten — und deuten darauf hin, dass das Schützen oder Wiederherstellen dieses frühen Lehrsignals entscheidend sein könnte, damit Menschen wieder lernen, schädliches Verhalten zu vermeiden.
Zitation: Tan, S.Y.S., Shen, M.H., Keevers, L.J. et al. Disinhibition of ventral tegmental area during initial punishment learning causes enduring punishment insensitivity. Neuropsychopharmacol. 51, 1045–1055 (2026). https://doi.org/10.1038/s41386-026-02368-4
Schlüsselwörter: Dopamin, Bestrafungslernen, ventrales tegmentales Areal, Sucht, Risikoverhalten