Clear Sky Science · he
חומצות שומן אומגה‑3 משפרות את חילוף החומרים של שומנים באמצעות ויסות miR-34a
מדוע המחקר הזה חשוב לבריאות יומיומית
מחלת כבד שומני ורמות שומנים גבוהות בדם הופכות נפוצות יותר ככל שהתזונה העשירה בקלוריות ושומן מתפשטת. רבים נוטלים שמן דגים או תוספי אומגה‑3 בתקווה להגן על הלב והכבד, אך האופן שבו שומנים אלה פועלים בתוך הגוף עדיין מתגלה. המחקר בוחן כיצד חומצות השומן מסוג אומגה‑3 משפרות את אופן הטיפול של הכבד בשומן, ומתרכז במתג גנטי זעיר בשם miR‑34a שעשוי להסביר מדוע אומגה‑3 מועילות במצבים מטבוליים מסוימים.
מתזונות עשירים לכבדים שומניים
החוקרים יצרו תחילה מודל של הפרעה מטבולית מונעת תזונה על ידי האכלת עכברים בדיאטה עתירת שומן במשך 12 שבועות. בהשוואה לבעלי החיים בקבוצת הביקורת שקיבלו מזון רגיל, עכברים אלה עלו במשקל יותר, הראו רמות טריגליצרידים וכולסטרול גבוהות יותר בדם והציגו סימנים לעמידות לאינסולין: רמות הסוכר בדם נשארו גבוהות למשך זמן ארוך יותר לאחר אתגר סוכר, וגופם נזקק לכמות רבה יותר של אינסולין על מנת להתמודד. כאשר המדענים בדקו את כבדם של בעלי החיים הללו, הם מצאו הצטברויות גדולות של שומן, ואישרו התפתחות מצב של כבד שומני הדומה לשלב מוקדם של מחלת כבד שומנית שאינה אלכוהולית בבני אדם.
בדיקת אומגה‑3 כטיפול מציל לכבד
כדי לבדוק האם חומצות שומן אומגה‑3 יכולות להפוך את הנזק הזה, עכברים שהוזנו בדיאטה עתירת שומן קיבלו מינונים שונים של תכשיר מרוכז של אומגה‑3 העשיר ב‑EPA ו‑DHA. על פני שמונה שבועות, הטיפול באומגה‑3 הוריד את רמות הטריגליצרידים בדם, את הכולסטרול הכללי ואת כולסטרול ה‑LDL «הרע», בעוד שכולסטרול ה‑HDL «הטוב» נותר במידה רבה ללא שינוי. בתוך הכבד ירדו רמות הטריגליצרידים והכולסטרול, ותמונות מיקרוסקופיות הראו טיפות שומן פחותות וקטנות יותר אצל בעלי החיים שטופלו באומגה‑3 לעומת קבוצות הביקורת על דיאטה עתירת שומן. באופן מעניין, אומגה‑3 שיפרו את האופן שבו בעלי החיים מטפלים בסוכר ובאינסולין אך לא שינו משמעותית את משקל הגוף הכולל, מה שמרמז על אפקט ישיר על המטבוליזם ולא על ירידה במשקל בלבד.
התמקדות במתגים מיקרוסקופיים
הצוות בדק אז שחקנים מולקולריים המווסתים האם הכבד מאחסן שומן או שורף אותו. בעכברים שניזונו בדיאטה עתירת שומן, רמות miR‑34a — מולקולת RNA קצרה שמדייקת פעילות גנים — היו גבוהות, בעוד חלבונים מגן שמקדמים שריפת שומנים, כגון SIRT1, PGC‑1α ו‑CPT‑1A, היו ירודים. במקביל, חלבון המעודד ייצור שומן, SREBP‑1c, עלה. הטיפול באומגה‑3 הפך את הדפוס הזה: miR‑34a ו‑SREBP‑1c ירדו, וחלבוני שריפת השומן עלו, באופן תלוי מינון ובאופן ברור. השינויים נצפו הן ברמת הגן והן ברמת החלבון, מה שמרמז על שכתוב מוצק של המנגנון שמטפל בשומן בכבד.
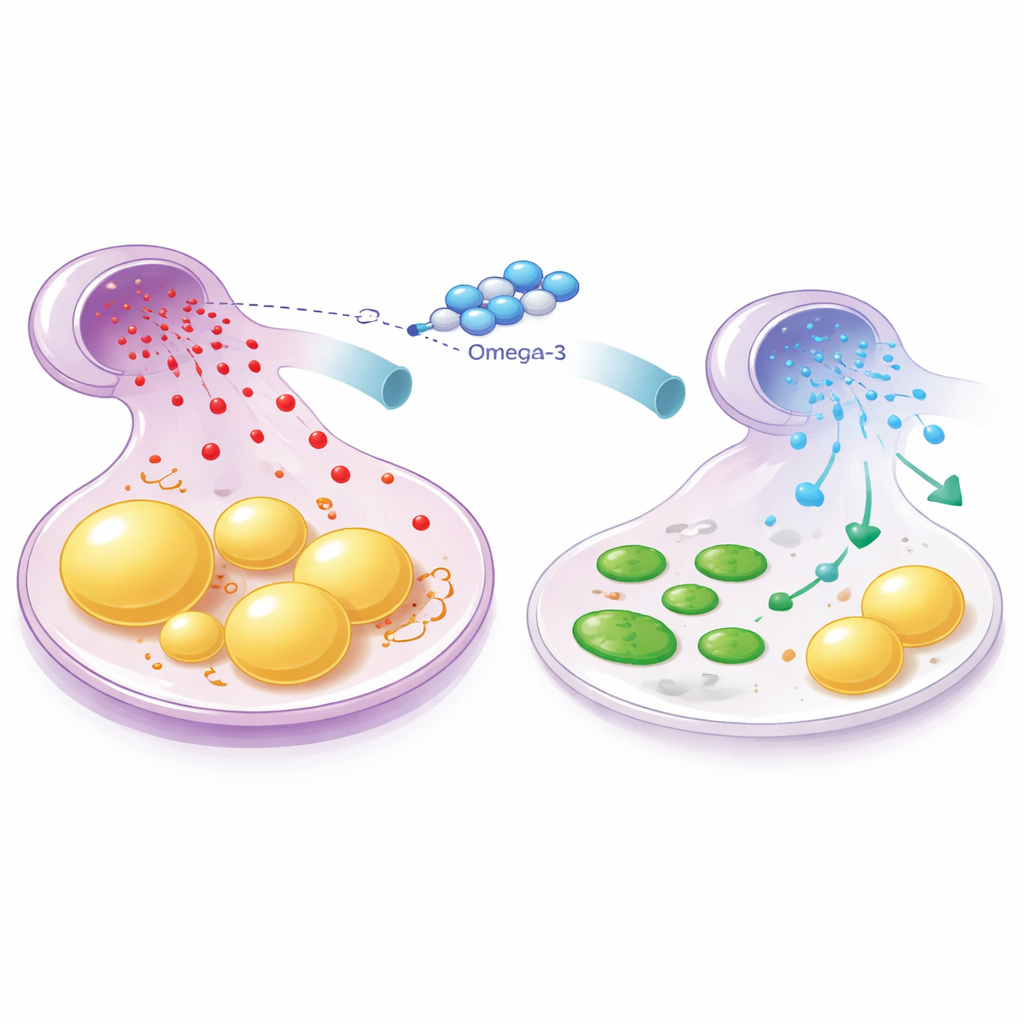
אימות המנגנון בתאי כבד אנושיים
כדי לבדוק האם הסיפור דומה גם בתאים אנושיים, החוקרים השתמשו בתאי כבד HepG2 בפטריה וגרמו להם למתח בעזרת חומצת הפלמיטית, שומן רווי שמניע הצטברות שומן. כפי שקרה בעכברים, טיפול זה הגביר את אחסון השומן בתאים והזיז את פעילות הגנים לכיוון ייצור שומן מוגבר ופירוק שומן מופחת. הוספת EPA, אחד מאומגה‑3 העיקריים, צמצמה את הצטברות השומן והשיבה איזון בריא יותר של חלבונים מרכזיים אלה. בעיקרו של דבר, כאשר המדענים הגבירו באופן מלאכותי את רמות miR‑34a, EPA כבר לא יכלה לספק את יתרונותיה: חלבוני שריפת השומן ירדו שוב, החלבון המעודד בניית שומן עלה, והתאים המשיכו להצטבר שומן. זה הראה ש‑miR‑34a פועל כמתג מרכזי שאומגה‑3 חייבות להשתיק על מנת להגן על תאי הכבד.
מה משמעות הממצאים לאנשים ולכבדיהם
לסיכום, המחקר מציע שחומצות השומן אומגה‑3 מסייעות לפינוי שומן מהכבד לא רק על ידי דילול שומנים תזונתיים, אלא על ידי שכתוב פעיל של האופן שבו תאי הכבד מטפלים בליפידים. על ידי הפחתת הפעילות של הבקר הקטן miR‑34a, אומגה‑3 משחררות את SIRT1 ודרכים קשורות שמגבירות את שריפת השומן ומורידות את ייצורו. בעוד שיש צורך במחקר נוסף כדי להבין כיצד מנגנון זה פועל באנשים עם מחלת כבד מתקדמת, הממצאים מחזקים את הבסיס הביולוגי לשימוש באומגה‑3 לתמיכה בבריאות מטבולית ועשויים להנחות טיפולים עתידיים שמכוונים ישירות יותר ל‑miR‑34a.
ציטוט: Li, L., Tang, Y., Wang, X. et al. Omega-3 fatty acids improve lipid metabolism by regulating miR-34a. Sci Rep 16, 12390 (2026). https://doi.org/10.1038/s41598-026-43353-7
מילות מפתח: חומצות שומן אומגה‑3, מחלת כבד שומני, חילוף חומרים של ליפידים, מיקרו‑RNA miR-34a, עמידות לאינסולין