Clear Sky Science · fr
Les acides gras oméga-3 améliorent le métabolisme lipidique en régulant miR-34a
Pourquoi cette recherche compte pour la santé quotidienne
La stéatose hépatique et l’élévation des graisses sanguines deviennent de plus en plus fréquentes à mesure que les régimes alimentaires s’enrichissent en calories et en lipides. Beaucoup de personnes prennent de l’huile de poisson ou d’autres compléments en oméga-3 en espérant protéger leur cœur et leur foie, mais le mode d’action de ces lipides dans l’organisme reste partiellement élucidé. Cette étude examine comment les acides gras oméga-3 améliorent la gestion des graisses par le foie, en se focalisant sur un petit interrupteur génétique appelé miR-34a qui pourrait expliquer pourquoi les oméga-3 sont utiles dans certaines maladies métaboliques.
Des régimes riches aux foies gras
Les chercheurs ont d’abord établi un modèle de perturbation métabolique induite par l’alimentation en donnant aux souris un régime riche en graisses pendant 12 semaines. Par rapport aux animaux témoins nourris avec une alimentation standard, ces souris ont pris davantage de poids, présenté des taux de triglycérides et de cholestérol sanguins plus élevés, et montré des signes de résistance à l’insuline : leur glycémie restait élevée plus longtemps après un test de charge en sucre et leur organisme nécessitait plus d’insuline pour y répondre. À l’examen des foies, les scientifiques ont constaté d’importants dépôts lipidiques, confirmant l’apparition d’un état de stéatose hépatique proche des premiers stades de la maladie du foie gras non alcoolique chez l’humain.
Tester les oméga-3 comme remède pour le foie
Pour évaluer si les acides gras oméga-3 pouvaient inverser ces dommages, les souris nourries au régime riche en graisses ont reçu différentes doses d’une préparation concentrée d’oméga-3 riche en EPA et DHA. Sur huit semaines, le traitement par oméga-3 a réduit les triglycérides sanguins, le cholestérol total et le « mauvais » cholestérol LDL, tout en laissant le « bon » cholestérol HDL globalement inchangé. Dans le foie, les niveaux de triglycérides et de cholestérol ont diminué, et les images au microscope ont montré beaucoup moins de gouttelettes lipidiques, et de plus petite taille, chez les animaux traités par oméga-3 que chez les contrôles nourris en excès. Fait intéressant, les oméga-3 ont amélioré la gestion du glucose et de l’insuline sans modifier significativement le poids corporel global, ce qui suggère un effet direct sur le métabolisme plutôt qu’une simple perte de poids.
Approfondir les interrupteurs microscopiques
L’équipe s’est ensuite intéressée aux acteurs moléculaires qui déterminent si le foie stocke ou brûle les graisses. Chez les souris alimentées riche en graisses, les niveaux de miR-34a — un petit ARN qui ajuste finement l’activité des gènes — étaient augmentés, tandis que des protéines protectrices favorisant la combustion des lipides, comme SIRT1, PGC-1α et CPT-1A, étaient réduites. Parallèlement, une protéine qui stimule la synthèse des graisses, SREBP-1c, était augmentée. Le traitement par oméga-3 a inversé ce schéma : miR-34a et SREBP-1c ont diminué, et les protéines de combustion lipidique ont augmenté, de manière dépendante de la dose. Ces modifications ont été observées tant au niveau des gènes que des protéines, ce qui suggère une réorganisation robuste des mécanismes hépatiques de gestion des lipides.
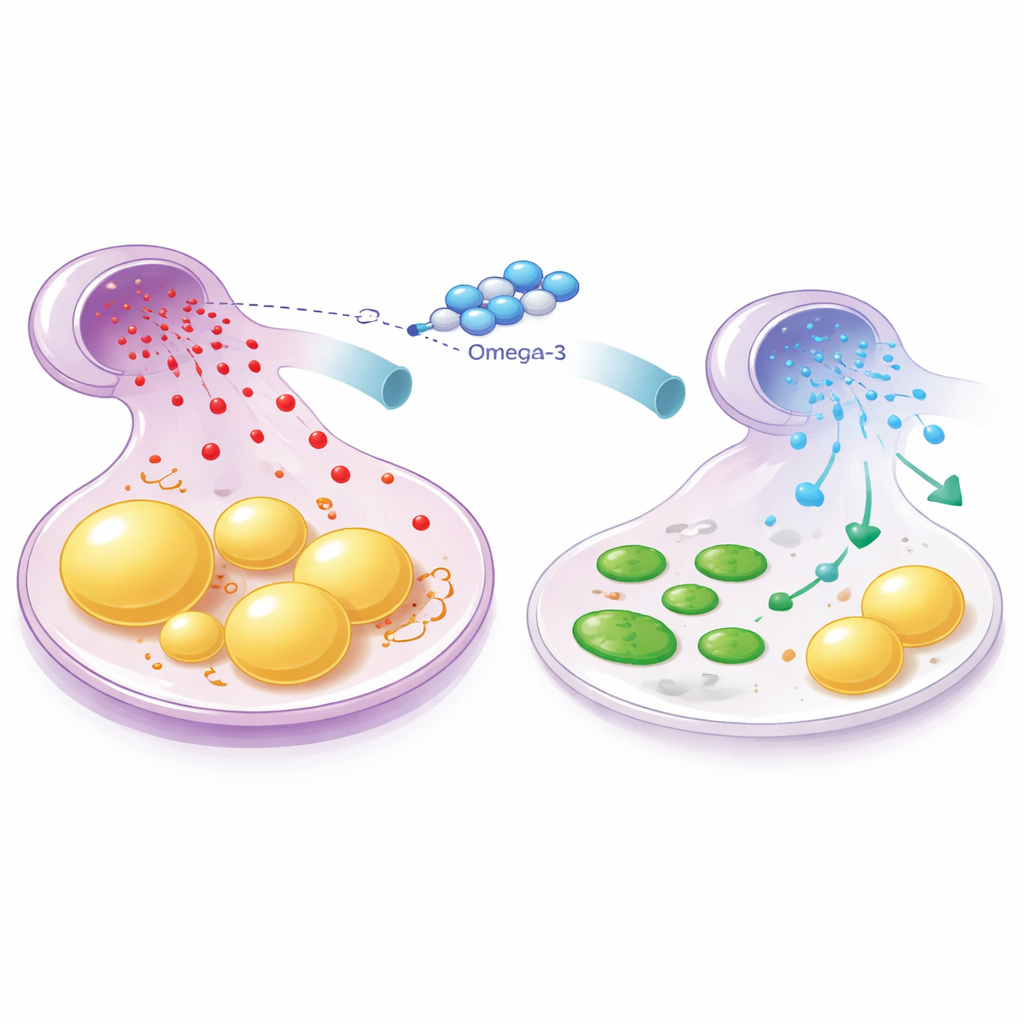
Confirmation du mécanisme dans des cellules hépatiques humaines
Pour vérifier si le même mécanisme s’applique aux cellules humaines, les chercheurs ont utilisé des cellules HepG2 en culture et les ont stressées avec de l’acide palmitique, un acide gras saturé qui favorise l’accumulation lipidique. Comme chez la souris, ce traitement a augmenté le stockage des lipides dans les cellules et a orienté l’expression génique vers davantage de production de graisses et moins de dégradation. L’ajout d’EPA, un acide gras oméga-3 majeur, a réduit l’accumulation lipidique et rétabli un équilibre plus sain de ces protéines clés. De manière cruciale, lorsque les scientifiques ont artificiellement augmenté les niveaux de miR-34a, l’EPA n’a plus pu exercer ses effets bénéfiques : les protéines de combustion lipidique ont de nouveau chuté, la protéine promotrice de synthèse des graisses a augmenté et les cellules ont continué d’accumuler des lipides. Cela montre que miR-34a agit comme un interrupteur central que les oméga-3 doivent inhiber pour protéger les cellules hépatiques.
Ce que cela signifie pour les personnes et leur foie
Dans l’ensemble, l’étude suggère que les acides gras oméga-3 aident à dégager les lipides du foie non seulement en diluant les apports lipidiques, mais en reconfigurant activement la manière dont les cellules hépatiques gèrent les lipides. En abaissant le petit régulateur miR-34a, les oméga-3 libèrent SIRT1 et des voies associées qui stimulent la combustion des graisses et réduisent leur production. Bien que des travaux supplémentaires soient nécessaires pour déterminer comment ce mécanisme fonctionne chez des personnes atteintes de maladies hépatiques avancées, ces résultats renforcent la base biologique de l’utilisation des oméga-3 pour soutenir la santé métabolique et pourraient orienter le développement futur de thérapies ciblant plus directement miR-34a.
Citation: Li, L., Tang, Y., Wang, X. et al. Omega-3 fatty acids improve lipid metabolism by regulating miR-34a. Sci Rep 16, 12390 (2026). https://doi.org/10.1038/s41598-026-43353-7
Mots-clés: acides gras oméga-3, stéatose hépatique, métabolisme des lipides, microARN miR-34a, résistance à l’insuline