Clear Sky Science · he
סריקה של מעכבי קינאז בקו תאי סרטן השד MDA-MB-231 המשויך למוטציית KRAS G13D ושלילי לכך טריפל
מדוע המחקר הזה חשוב
סרטן השד הטריפל‑שלילי הוא אחד הצורות הקשות ביותר לטיפול. הוא נוטה להתפשט מוקדם, לחזור לעתים קרובות ולחסור את הסמנים ההורמונליים ואת HER2 שעליהם סומכות תרופות רבות מוצלחות. מחקר זה בוחן האם דור חדש של תרופות החוסמות מתגי גדילה מרכזיים בתוך תאי הגידול יכול לשולב כדי להאט או לעצור טוב יותר את המחלה האגרסיבית הזו, תוך שימוש בקו תאי שנחקר נרחב כשטח ניסוי.
סרטן שד שקשה לטפל בו
גידולי שד טריפל‑שליליים אינם מגיבים לטיפולים הורמונליים או לתרופות קלאסיות המכוונות ל‑HER2, ולכן רוב החולות מקבלות כימותרפיה. בעוד שחלק מהגידולים מצטמצמים לחלוטין, רבים משאירים תאים עמידים המובילים מאוחר יותר לשחזור ולהתפשטות. חלק מהסרטן הזה נושא פירצות בגֵן הגדילה KRAS ומציג פעילות נמוכה אך משמעותית של מולקולה משטח קשורה שנקראת HER2. יחד, שינויים אלה יכולים לקדם גדילה וחודרנות גידולית, מה שמרמז כי חסימת מספר מתגי גדילה מקושרים בו‑זמנית עשויה להיות יעילה יותר מאשר פגיעה בכל אחד בנפרד.
חיפוש בספריית תרופות רחבה
החוקרים עבדו עם תאי MDA‑MB‑231, קו סרטן שד טריפל‑שלילי הנושא מוטציית KRAS ספציפית (G13D) ופעילות נמוכה של HER2. הם חשפו תאים אלה ל‑157 תרופות שונות המכוונות לאנזימים הנקראים קינאזות — מתגי הדלק/כיבוי מרכזיים בסיגנלינג הסרטני. כמה תרכובות שפגעו במסלולי סטרס או הישרדות כלליים היו רעילות מאוד אך לא מאוד סלקטיביות, ולכן הושמו בצד. בין התרופות היותר ספציפיות, שתי תרופות שפותחו במקור לחלק מסוגי הלוקמיה, בוסוטיניב ודסאטיניב, בלטו ביכולתם העזה לעכב גדילת תאים. שתיהן חוסמות קינאז הנקרא c‑Abl (וכמו כן קינאזות SRC קרובות). תרופה שלישית, סארקאטיניב, שפונה בעיקר ל‑SRC אך לא ל‑c‑Abl, הייתה חלשה במידה ניכרת במודל סרטן השד הזה.
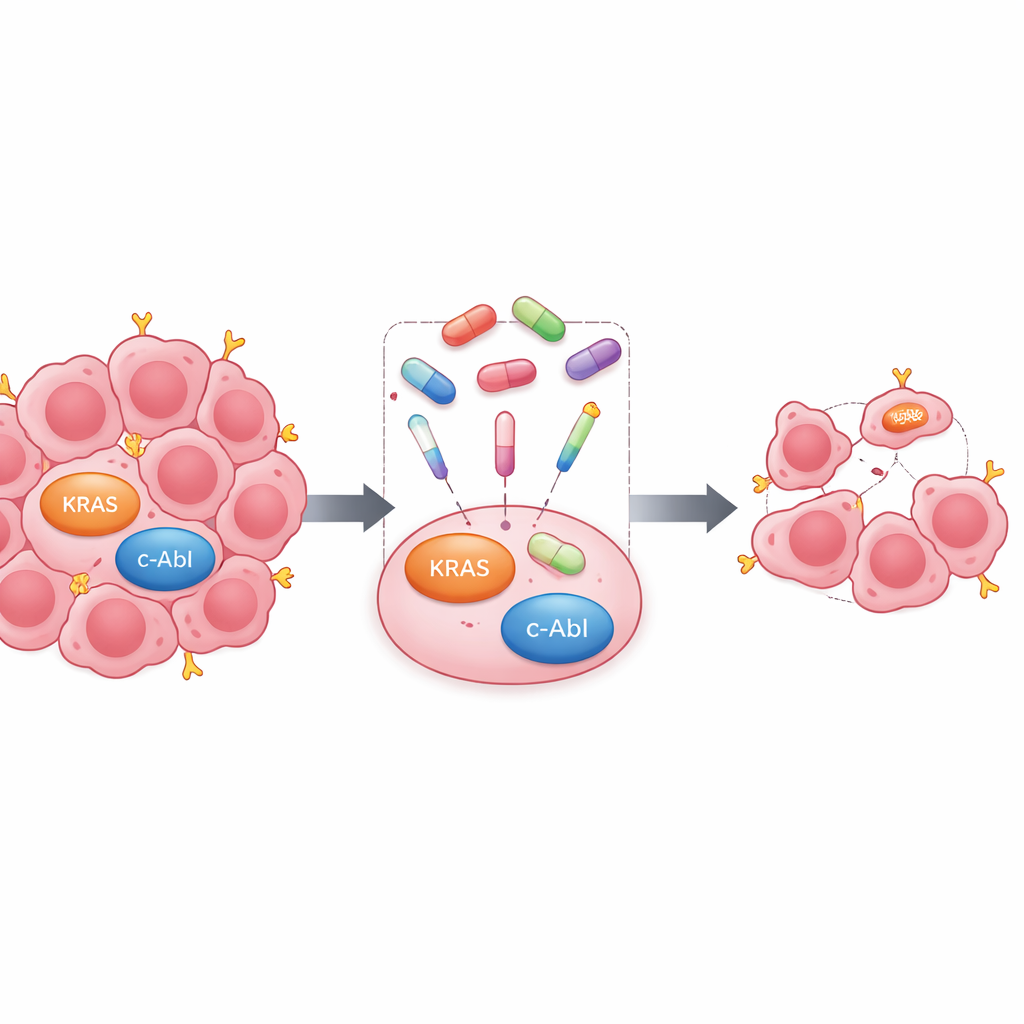
קישור בין מטרות בלוקמיה לתאי סרטן שד
כדי להבין מדוע תרופות הלוקמיה היו יעילות, השווה הצוות את תאי סרטן השד לבין קו תאי לוקמיה שנושא את הפיוז'ן המפורסם BCR‑ABL. באמצעות בדיקות חלבון הם אישרו שתאי MDA‑MB‑231 אינם נושאים את הפיוז'ן הזה אך כן מייצרים c‑Abl נורמלי. ממצא זה הצביע על c‑Abl עצמו — ולא על BCR‑ABL — כמניע רלוונטי בתאי סרטן השד הללו. הקבוצה פנתה אז לשתי תרופות מודרניות המכוונות ל‑KRAS: MRTX1133, המתוכננת למוטציה קרובה ב‑KRAS, ו‑RMC‑7977, תרופה חדשה שמייצרת קומפלקס תלת‑חלקי עם חלבון מסייע ו‑RAS פעיל כדי לכבות מספר וריאנטים של KRAS. כשנבדקו לבד, שתי התרופות הורידו את השרידות של התאים, אך RMC‑7977 היה עוצמתי יותר ושמר על השפעתו על מסלולי סיגנלינג מרכזיים זמן ארוך יותר מ‑MRTX1133.
שילוב חוסמי מתגי גדילה
גרעין המחקר בחן שילובים של חוסמי KRAS אלה עם תרופות קינאז נבחרות, כולל מעכבי c‑Abl/SRC ותרופות הקשורות ל‑HER2. באמצעות שיטות סטנדרטיות למדידת האם זוג תרופות פועל טוב יותר יחד מהמצופה, מצאו המחברים סינרגיה רחבה. MRTX1133 עבד במיוחד טוב עם דסאטיניב ובוסוטיניב, והראה גם השפעות שיתופיות עם חוסם SOS1 (המושפע מהפעלת KRAS) ועם סוכנים המכוונים ל‑HER2 כגון מובוסרטיניב ו‑נראטיניב. RMC‑7977 הופיעה מרשימה אף יותר: כל השילובים שנבדקו עמה היו סינרגיסטיים על פני טווחי מינון. במבחני הגירה מסוג "שריטה" (scratch) העוקבים כמה מהר תאים נעים לסגור רווח, בוסוטיניב ודסאטיניב האטו במובהק את תנועת התאים, בעוד ש‑RMC‑7977 עיכב קצרות את התנועה אך לא שמר על האפקט הזה, מה שמשקף את השפעתו החלקית על גדילה כללית של התאים.

מה זה יכול להעיד עבור מטופלים
אף על פי שהעבודה נעשתה במנות מעבדה ולא בחולים, היא מדגישה אסטרטגיה מבטיחה לסוג סרטן מאתגר במיוחד: כוונון משותף של KRAS, c‑Abl וסיגנלינג מקושר ל‑HER2. הממצאים מציעים כי c‑Abl הוא מניע חשוב של גדילה והגירה במודל הטריפל‑שלילי עם מוטציית KRAS זה, וכי תרופות לוקמיה שכבר נמצאות בשימוש קליני יכולות להגביר את עוצמת הטיפולים המכוונים ל‑KRAS ול‑HER2. על ידי תקיפת מספר מתגי גדילה מחוברים בו‑זמנית, שילובים אלה עשויים לסייע להתגבר על עמידות שהגבילה טיפולים ממוקדים קודמים ובמרץ הזמן לתרום לאפשרויות יעילות יותר לאנשים עם סרטן שד טריפל‑שלילי חיובי ל‑KRAS.
ציטוט: Stickler, S., Eggerstorfer, MT., Rieche, M. et al. Screening of kinase inhibitors in the triple negative KRAS G13D-mutated MDA-MB-231 breast cancer cell line. Sci Rep 16, 13170 (2026). https://doi.org/10.1038/s41598-026-43207-2
מילות מפתח: סרטן השד טריפל-שלילי, מעכבי KRAS, קינאז c-Abl, שילובי תרופות, טיפול ממוקד