Clear Sky Science · he
שימוש בריצוף RNA בקנה מידה גדול וברמת תא יחיד כדי לזהות סמנים פוטנציאליים הקשורים לאנגיוגנזה ולמנגנון התגובת הלחץ המשולב בכונדרוסרקומה
מדוע מחקר סרטן העצם הזה חשוב
כונדרוסרקומה היא סרטן עצם נדיר אך עקשן שפוגע בעיקר במבוגרים ולעתים קרובות עמיד לטיפולים סטנדרטיים כמו כימותרפיה וקרינה. במקרים מסוימים ניתן להסיר את הגידול בניתוח, אך כאשר המחלה מתפשטת או חוזרת, האפשרויות מוגבלות. במחקר זה בחנו את המנגנונים המולקולריים בתאי הכונדרוסרקומה כדי לזהות "דגלים" מולקולריים שמסייעים לגידול ליצור כלי דם חדשים ולהישרדות תחת מצבי לחץ. דגלים אלה עשויים בעתיד להנחות אבחון מוקדם וטיפולים מדויקים ומותאמים יותר.
חיפוש סימנים גנטיים אופייניים בגידול
החוקרים התחילו מנתונים גנטיים זמינים לציבור של גידולים כונדרוסרקומה ורקמת סחוס בריאה. באמצעות פרופיל RNA בקנה מידה גדול, שמודד אילו גנים פעילים או מושתקים, חיפשו גנים המקושרים לשתי תהליכים שחשובים במיוחד בסרטן תוקפני: היווצרות כלי דם חדשים (אנגיוגנזה) ומערכת החירום התאית הידועה כמנגנון התגובת הלחץ המשולב. על ידי השוואת דגימות גידול לרקמה נורמלית וקיבוץ גנים שנוטים לעלות ולרדת יחד, הצמצמו אלפי מועמדים לקבוצת גנים קטנה שהייתה גם בלתי-מסודרת בסרטן וגם קשורה לצמיחת כלי דם ולאותות לחץ.
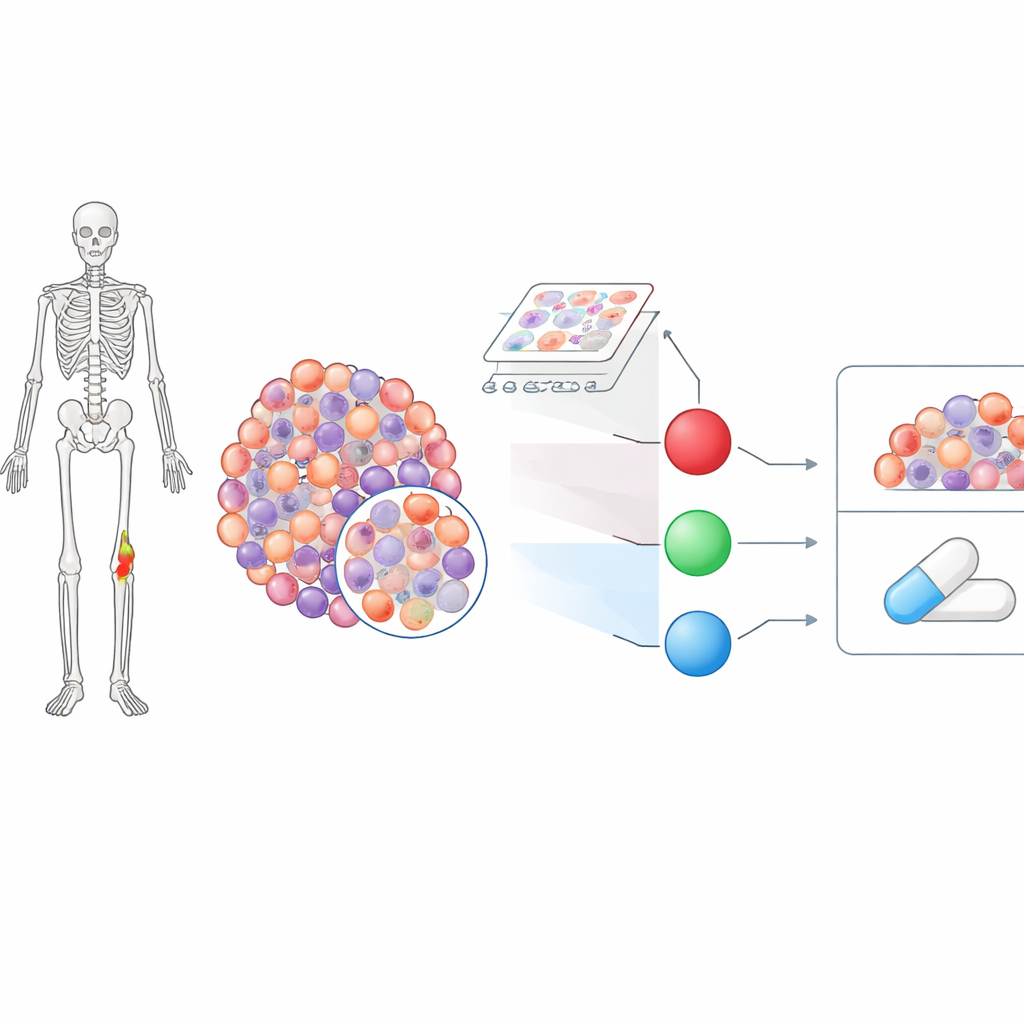
שלוש מולקולות מרכזיות בולטות
מרשימת הגנים הארוכה צמחו שלושה גנים שהיראו כבסיסיים כסמנים מבטיחים: HSPA8, LMNA ו-SERPINH1. שלושתם הפגינו פעילות מוגברת בעקביות בדגימות גידול בשני מאגרי מטופלים עצמאיים. כל אחד ממלא תפקיד שונה אך משלים בתא. HSPA8 מסייע לקיפול נכון של חלבונים ומגן על תאים מפגיעה כשהם סובלים ממחסור בחמצן או מצטברים חלבונים מקופלים בצורה שגויה — מצבים שכיחים בתוך גידולים הגדלים במהירות. LMNA מקודד חלבונים מבניים שמחזיקים על צורת ויציבות גרעין התא, שבו מאוחסן ונקרא ה-DNA. SERPINH1 מסייע בבניית קולגן, מרכיב מרכזי של המטריקס הדמוי סחוס שמקיף תאי כונדרוסרקומה ויכול להגן עליהם מפני טיפול.
חיבור בין לחץ, תאי תמיכה וכלי דם
כדי להתגבר על ממוצעים בקנה מידה גדול, הצוות בחן נתוני ריצוף RNA בתא יחיד ממאות עד אלפי תאים שנלקחו מגידולי כונדרוסרקומה. מבט מדויק זה אפשר לזהות אילו סוגי תאים נושאים רמות גבוהות של שלושת המ biomarkers. האותות החזקים ביותר הופיעו בתאים סטרומאליים — תאי תמיכה בסביבת הגידול שיכולים להשפיע על גדילה, פלישה והיווצרות כלי דם. באמצעות שחזור של שינויי תאים על פני מסלול "זמן-מדומה" (pseudo-time), הראו החוקרים ש-HSPA8 ו-LMNA נוטים לעלות ככל שהתאים מתמחים יותר, בעוד ש-SERPINH1 יורד בהדרגה. מיפוי תקשורת בין סוגי התאים הציע איתות חזק במיוחד בין התאים הסטרומאליים לצבירי תאים דמויי-סחוס סמוכים, מה שמרמז כי הסמנים עשויים לתאם תקשורת שמסייעת להתקדמות הגידול.
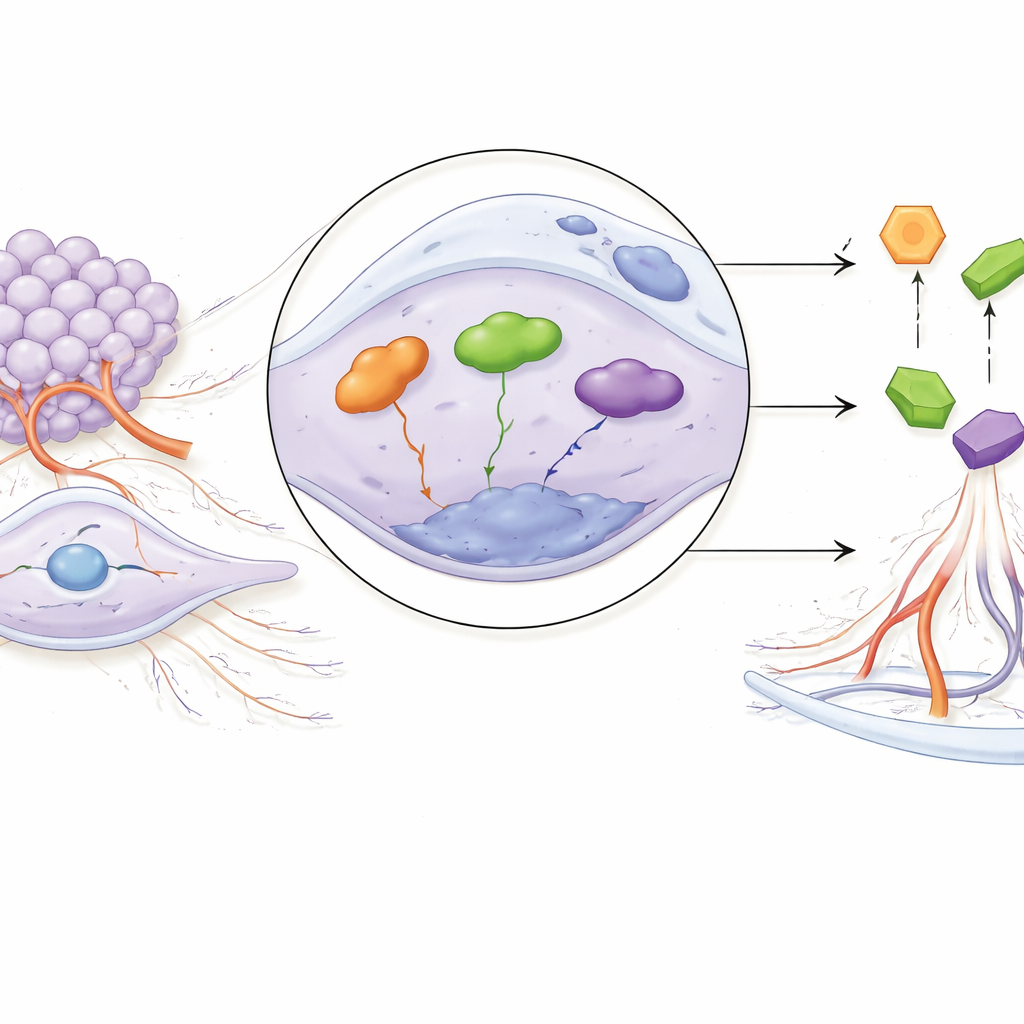
מרשתות למול תרופות אפשריות
החוקרים שיבצו את שלושת הסמנים לרשתות רגולטוריות ותקשורת עם תרופות. הם מצאו רשת של גורמי שעתוק, microRNA ורנ״א ארוך שאינו מקודד לחלבון שנראים כבעלי תפקיד בשליטה על גנים אלו, כאשר גורם אחד, STAT1, בולט כצומת מרכזי המקשר בין השלושה. באמצעות כלים חישוביים, הם גם חזו כמה תרכובות קיימות שעשויות להיקשר לחלבונים המוצגים על־ידי HSPA8, LMNA ו-SERPINH1. סיומי דוקינג מדומים הציעו קשירה חזקה בין HSPA8 ל-ADP, בין LMNA ולונאפארניב (lonafarnib) — תרופה ניסיונית לסרטן — וקשירה מתונה למולקולה קטנה שלישית ל-SERPINH1. לבסוף, ניסויים במעבדה בעזרת דגימות רקמה של מטופלים אישרו שהשלושה אכן פעילים יותר בכונדרוסרקומה מאשר בבקרים בריאים, מה שמגבירה את טענתם כסמנים במציאות קלינית.
מה זה יכול להיות משמעותי עבור מטופלים
במילים פשוטות, המחקר מצביע על כך ששלוש המולקולות — HSPA8, LMNA ו-SERPINH1 — פועלות כעוזרות חשובות לכונדרוסרקומה, מאפשרות לתאי תמיכה לעמוד בפני לחץ, לשנות את סביבתם ולעודד כלי דם חדשים. מאחר שהן מוערכות בעקביות בדגימות מטופלים ונמצאות בצומת של מסלולי הישרדות מרכזיים, הן יכולות לשמש כאיתותים לאבחון או כיעדים לתרופות עתידיות. למרות שדרוש עוד עבודה — במיוחד בבחינת תרופות מועמדות ואימות המסלולים בעוד מטופלים — הממצאים מספקים מפת דרכים ברורה יותר של האופן שבו סרטן עצם זה מתמשך ומצביעים על אסטרטגיות חדשות להאטתו או לעצירתו.
ציטוט: Li, S., Zhao, J., Qin, Q. et al. Utilizing bulk and single-cell RNA sequencing to identify potential biomarkers linked to angiogenesis and integrated stress response in chondrosarcoma. Sci Rep 16, 10133 (2026). https://doi.org/10.1038/s41598-026-40800-3
מילות מפתח: כונדרוסרקומה, אנגיוגנזה, מנגנון התגובת הלחץ המשולב, ריצוף RNA בתא יחיד, סמנים ביולוגיים