Clear Sky Science · de
Verwendung von Bulk- und Einzelzell-RNA-Sequenzierung zur Identifizierung potenzieller Biomarker, die mit Angiogenese und integriertem Stressantwort in Chondrosarkom verknüpft sind
Warum diese Studie zu Knochentumoren wichtig ist
Chondrosarkom ist ein seltener, aber hartnäckiger Knochentumor, der vorwiegend Erwachsene betrifft und häufig gegenüber Standardtherapien wie Chemotherapie und Bestrahlung resistent ist. Operative Eingriffe können den Tumor manchmal entfernen, doch wenn die Erkrankung metastasiert oder wiederkehrt, sind die Optionen begrenzt. Diese Studie schaut in die molekulare Mechanik von Chondrosarkomzellen, um „Markierungen“ zu finden, die dem Tumor helfen, neue Blutgefäße zu bilden und unter Stress zu überleben. Solche Marker könnten eines Tages eine frühere Diagnose und gezieltere Therapien ermöglichen.
Auf der Suche nach charakteristischen Genmustern im Tumor
Die Forschenden begannen mit öffentlich zugänglichen Genomdaten von Chondrosarkom‑Tumoren und gesundem Knorpelgewebe. Mit großflächiger RNA‑Profilierung, die misst, welche Gene ein- oder ausgeschaltet sind, suchten sie nach Genen, die mit zwei Prozessen verknüpft sind, die in aggressiven Tumoren besonders wichtig sind: dem Wachstum neuer Blutgefäße (Angiogenese) und der zellulären Notfallreaktion, der sogenannten integrierten Stressantwort. Durch den Vergleich von Tumorproben mit normalem Gewebe und die Gruppierung von Genen, die gemeinsam an‑ oder abgeschaltet wurden, reduzierten sie Tausende von Kandidaten auf eine kleine Anzahl von Genen, die sowohl im Krebs fehlreguliert als auch mit Gefäßbildung und Stresssignalen verbunden waren.
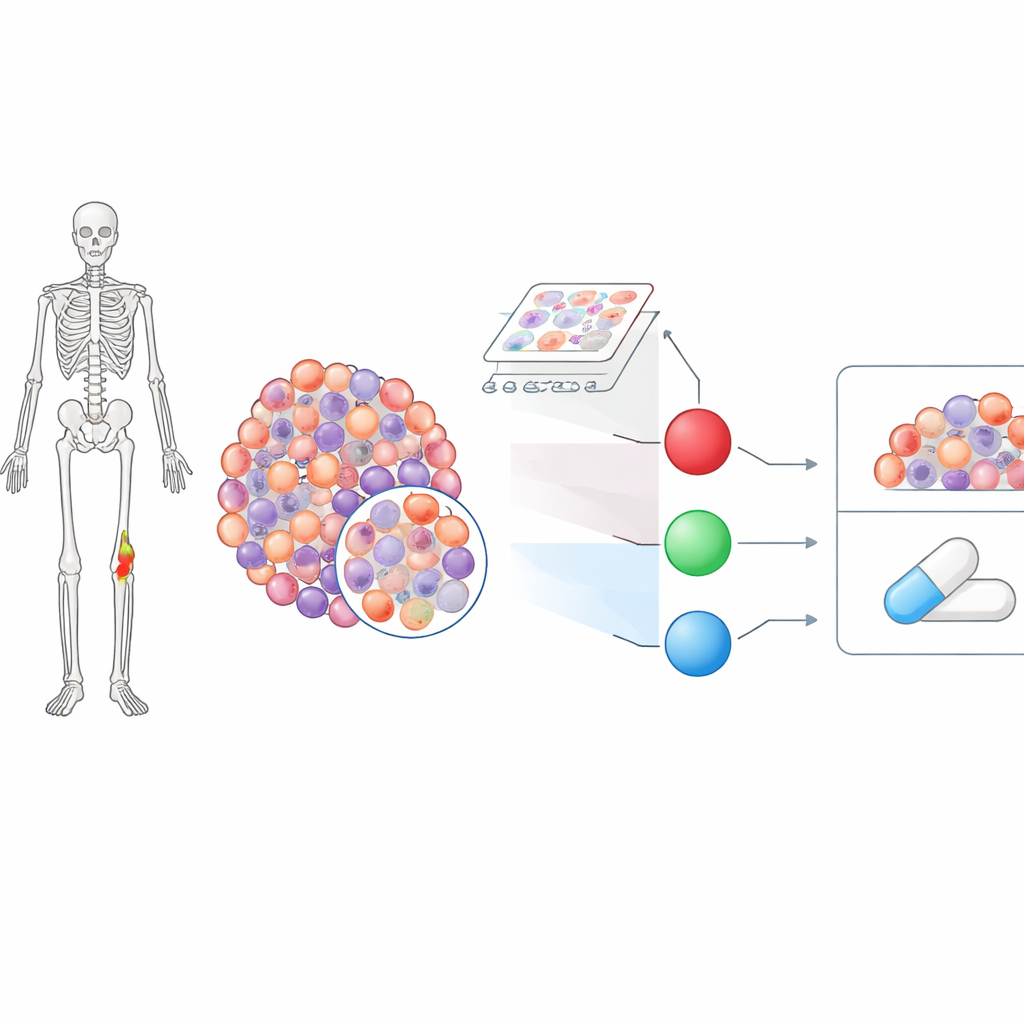
Drei Schlüsselmoleküle stechen hervor
Aus dieser Auswahl traten drei Gene als besonders vielversprechende Biomarker hervor: HSPA8, LMNA und SERPINH1. Alle drei zeigten in Tumorproben aus zwei unabhängigen Patientendatensätzen konstant erhöhte Aktivität. Jedes spielt eine unterschiedliche, aber ergänzende Rolle in der Zelle. HSPA8 unterstützt das korrekte Falten anderer Proteine und schützt Zellen vor Schäden, wenn Sauerstoff knapp ist oder fehlgefaltete Proteine anfallen — Zustände, die in schnell wachsenden Tumoren häufig sind. LMNA kodiert für strukturelle Proteine, die Form und Stabilität des Zellkerns erhalten, in dem die DNA gespeichert und abgelesen wird. SERPINH1 unterstützt den Aufbau von Kollagen, einem Hauptbestandteil der knorpelähnlichen Matrix, die Chondrosarkomzellen umgibt und sie vor Therapien abschirmen kann.
Verknüpfung von Stress, Stützzellen und Blutgefäßen
Um über mittlere Werte aus Bulk‑Daten hinauszugehen, untersuchte das Team Einzelzell‑RNA‑Sequenzierungsdaten von Tausenden einzelner Zellen aus Chondrosarkomtumoren. Diese feinere Perspektive erlaubte es, genau zu bestimmen, welche Zelltypen hohe Werte der drei Biomarker tragen. Die stärksten Signale fanden sich in stromalen Zellen — Stütz‑ und Interaktionszellen im Tumormikromilieu, die Wachstum, Invasion und Gefäßbildung beeinflussen können. Durch die Rekonstruktion eines „Pseudo‑Zeit“-Trajektors zeigten die Forschenden, dass HSPA8 und LMNA tendenziell ansteigen, während die Zellen sich weiter differenzieren, während SERPINH1 allmählich abnimmt. Kommunikationsanalysen zwischen Zelltypen deuteten auf besonders starke Signalwege zwischen diesen stromalen Zellen und benachbarten knorpelähnlichen Tumorclustern hin, was nahelegt, dass die Biomarker an der Koordination von Interaktionen beteiligt sein könnten, die das Tumorwachstum begünstigen.
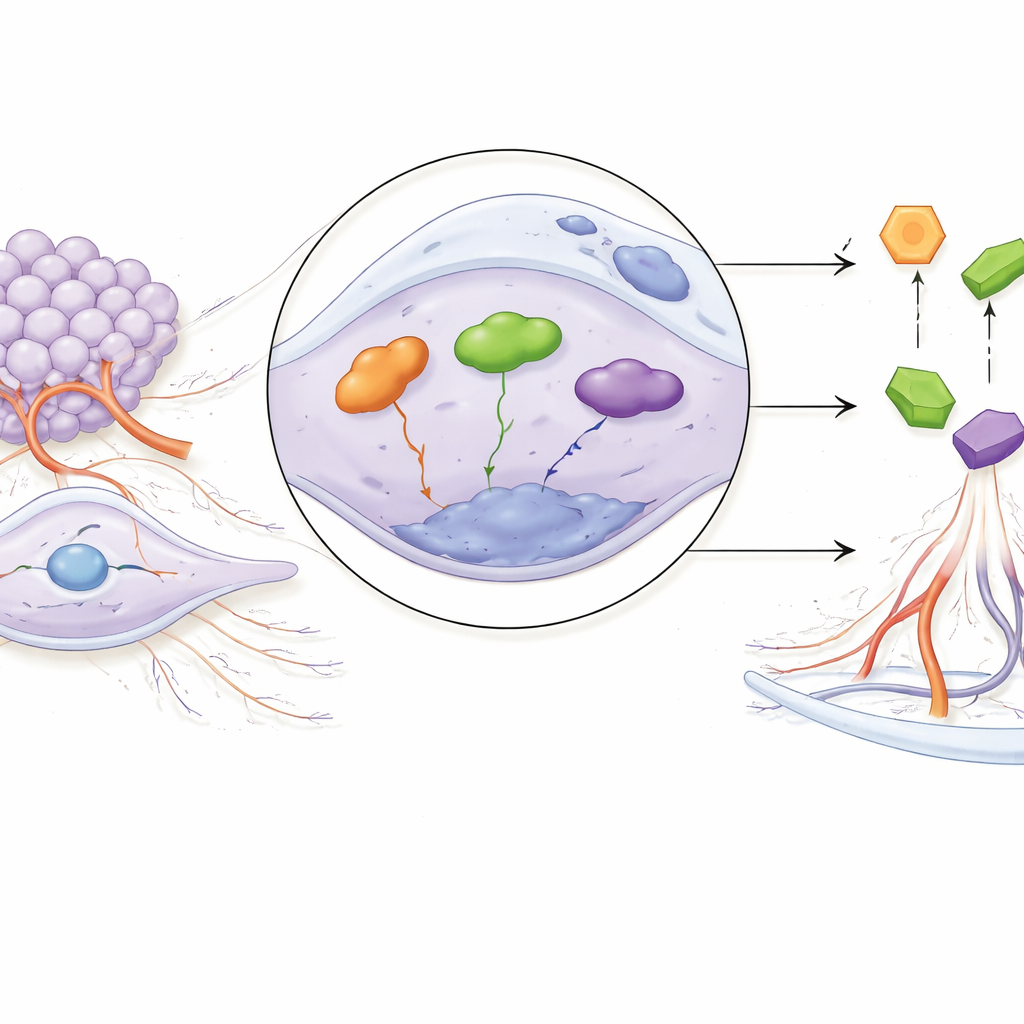
Von Netzwerken zu möglichen Wirkstoffen
Die Forschenden betteten die drei Biomarker anschließend in größere regulatorische und Wirkstoff‑Interaktionsnetzwerke ein. Sie identifizierten ein Geflecht von Transkriptionsfaktoren, microRNAs und langen nichtkodierenden RNAs, die offenbar diese Gene steuern; ein Faktor, STAT1, hob sich als zentrales Element heraus, das alle drei berührt. Mit computergestützten Methoden sagten sie außerdem mehrere bereits existierende Verbindungen voraus, die an die von HSPA8, LMNA und SERPINH1 kodierten Proteine binden könnten. Simulierte Docking‑Analysen zeigten starke Bindung zwischen HSPA8 und ADP, zwischen LMNA und dem experimentellen Krebswirkstoff Lonafarnib sowie mäßige Bindung eines dritten kleinen Moleküls an SERPINH1. Abschließend bestätigten Labortests an Patientenproben, dass die drei Gene in Chondrosarkom tatsächlich stärker exprimiert sind als in gesunden Kontrollen, was ihre Relevanz als realweltliche Marker untermauert.
Was das für Patienten bedeuten könnte
Vereinfacht gesagt legt diese Studie nahe, dass drei Moleküle — HSPA8, LMNA und SERPINH1 — als wichtige Unterstützer des Chondrosarkoms fungieren, indem sie den stützenden Zellen helfen, Stress zu überstehen, ihre Umgebung umzubauen und neue Blutgefäße zu fördern. Da sie in Tumoren von Patientinnen und Patienten konstant erhöht sind und an zentralen Überlebenswegen sitzen, könnten sie als Frühwarnsignale für Diagnosen oder als Angriffspunkte für zukünftige Medikamente dienen. Obwohl noch viel Arbeit nötig ist — insbesondere die Prüfung vorgeschlagener Wirkstoffe und die Bestätigung dieser Wege in weiteren Patientenkohorten — liefert die Untersuchung eine klarere Karte, wie sich dieser Knochentumor selbst erhält, und weist auf neue Strategien hin, sein Wachstum zu verlangsamen oder zu stoppen.
Zitation: Li, S., Zhao, J., Qin, Q. et al. Utilizing bulk and single-cell RNA sequencing to identify potential biomarkers linked to angiogenesis and integrated stress response in chondrosarcoma. Sci Rep 16, 10133 (2026). https://doi.org/10.1038/s41598-026-40800-3
Schlüsselwörter: Chondrosarkom, Angiogenese, integrierte Stressantwort, Einzelzell‑RNA‑Sequenzierung, Biomarker