Clear Sky Science · fr
Décodage quantitatif assisté par IA de la configuration moléculaire et des effets stériques pour des électrolytes de batteries au zinc haute performance
Des batteries plus intelligentes pour un avenir renouvelable
À mesure que panneaux solaires et parcs éoliens se multiplient, nous avons besoin de batteries bon marché et sûres capables de stocker de grandes quantités d’énergie pendant des heures ou des jours. Les batteries aqueuses au zinc-ion sont particulièrement attractives car le zinc est peu coûteux, abondant et fonctionne dans des électrolytes aqueux plutôt que dans des liquides organiques inflammables. Mais les batteries au zinc actuelles souffrent encore de durées de vie courtes et de surfaces métalliques instables. Cette étude montre comment l’intelligence artificielle peut trier des milliers de molécules candidates pour en trouver quelques-unes qui modifient subtilement la manière dont les ions zinc se déplacent dans le liquide, prolongeant ainsi de façon spectaculaire la durée de vie de la batterie.
Utiliser l’IA pour sonder un océan de molécules
Les auteurs partent d’un problème bien connu en chimie : il existe bien plus de molécules organiques possibles que ce qu’un laboratoire peut tester empiriquement. Pour y remédier, ils ont constitué une grande base de données de plus de 20 000 petites molécules issues d’archives chimiques publiques, puis l’ont reliée à un système d’IA basé sur des modèles de langage de grande taille. En utilisant une méthode appelée génération augmentée par récupération, l’IA a d’abord « lu » et résumé 50 articles récents sur les batteries au zinc afin d’extraire ce qui compte réellement pour les additifs d’électrolyte — par exemple la solubilité dans l’eau, la position des groupes polaires et la manière dont la molécule interagit avec les ions zinc et la surface métallique. Les chercheurs ont ensuite conçu des prompts précis pour que l’IA applique de façon cohérente ces règles dérivées de la littérature lors du criblage des molécules selon trois critères clés : structures à anneau simple ou chaînes courtes, solubilité aqueuse modérée, et types appropriés de groupes chimiques polaires.
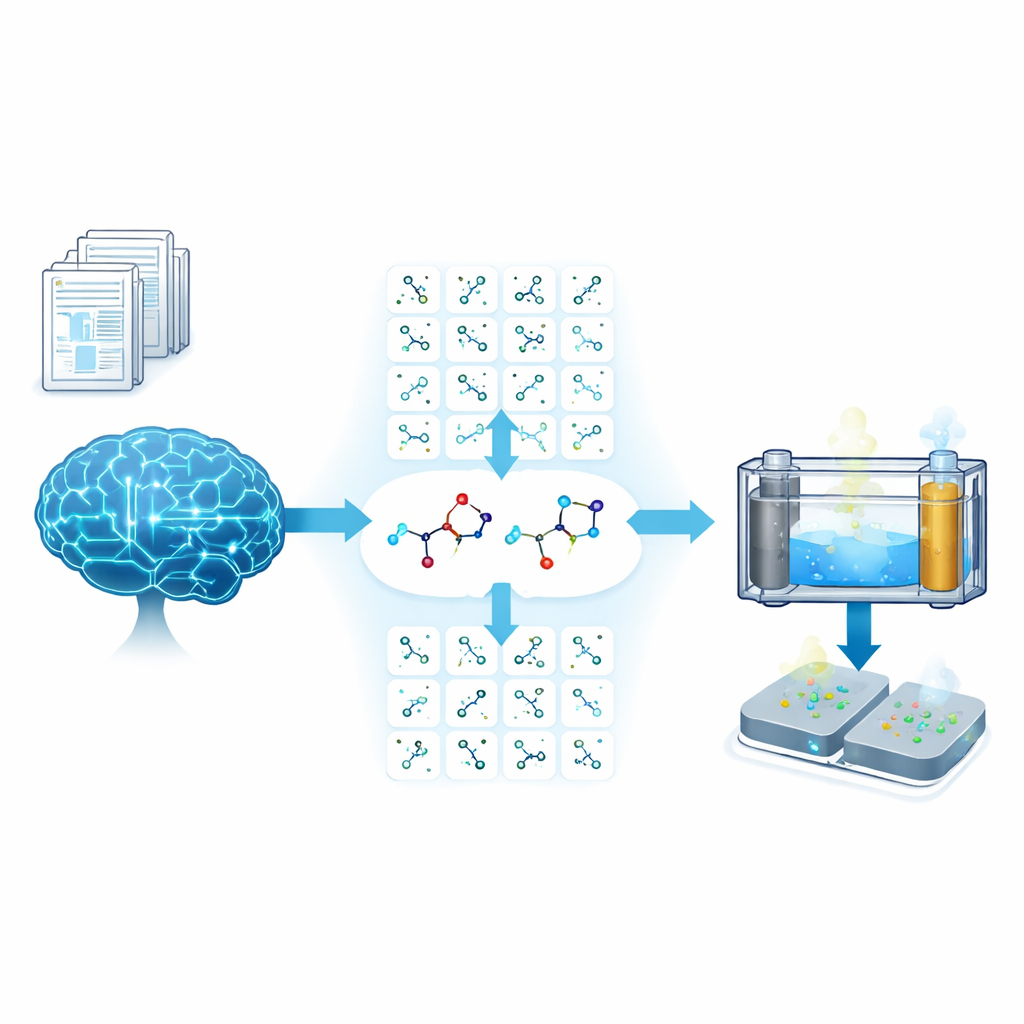
De milliers d’options à deux aides remarquables
Le criblage initial par l’IA a réduit l’immense pool moléculaire à 18 candidats prometteurs. Pour affiner cette liste, l’équipe a réalisé des calculs de mécanique quantique afin de quantifier deux propriétés de base : la force de liaison de chaque molécule à un ion zinc et sa masse moléculaire. En traçant la force de liaison en fonction du poids moléculaire, ils ont pu repérer des paires similaires sur ces aspects mais très différentes par leur forme. De cette approche sont ressorties deux molécules comme « partenaires de contraste » idéales : la 2-méthylimidazole (MI), un cycle rigide, et la 3-aminopropanol (AP), une chaîne flexible. Cet appariement a permis aux chercheurs d’explorer clairement comment la forme moléculaire et le volume occupé par une molécule — ses effets stériques — gouvernent la structure microscopique autour des ions zinc et, in fine, les performances de la batterie.
Comment la forme moléculaire dirige le mouvement des ions
À l’aide de simulations de dynamique moléculaire à grande échelle, les auteurs ont observé comment MI et AP se placent dans la première sphère de solvatation autour d’un ion zinc en solution aqueuse. L’anneau rigide de la MI forme une cage volumineuse et inflexible qui contraint les molécules d’eau environnantes dans un arrangement serré, élevant une sorte de « barrière d’entrée » pour la réorganisation du solvant et limitant la mobilité de l’ion zinc. En revanche, la chaîne flexible de l’AP change de conformation pour s’adapter à l’environnement, créant une couche plus compacte mais moins encombrée qui permet aux eaux et aux ions de se déplacer plus librement. L’AP coordonne également le zinc via plusieurs sites le long de sa chaîne, incluant des atomes d’azote et d’oxygène, ce qui lui permet de stabiliser l’ion tout en laissant de la place pour une migration rapide. Ces différences structurelles se répercutent, modifiant l’agglomération des ions zinc et sulfate, le paysage électrostatique ressenti par les ions, et la manière dont les molécules d’eau forment et cassent les liaisons hydrogène.
Reconstruire le réseau caché du liquide
L’équipe a exploré plus en profondeur le « câblage invisible » de l’électrolyte : le réseau de liaisons hydrogène entre molécules d’eau. Dans une solution de sulfate de zinc pure, les molécules d’eau sont fortement liées, ce qui favorise le saut rapide des protons via le mécanisme de Grotthuss et alimente l’évolution indésirable d’hydrogène à la surface du zinc. L’ajout de MI perturbe quelque peu ce réseau mais laisse de nombreux chemins intacts. L’AP, grâce à sa chaîne flexible et à ses multiples sites de liaison, va beaucoup plus loin : elle « vole » des liaisons hydrogène aux paires eau–eau, transforme de nombreux liens longs et faibles en liens plus forts mais plus localisés, et réduit substantiellement la réponse diélectrique globale et les fluctuations de dipôle du liquide. En conjonction avec des énergies de solvatation/dé-solvatation favorables et une forte adsorption sur la surface du zinc, cette réorganisation du réseau hydrogène calme les réactions secondaires, abaisse la barrière énergétique au mouvement des ions zinc et favorise un dépôt uniforme plutôt que la formation de dendrites en aiguilles.
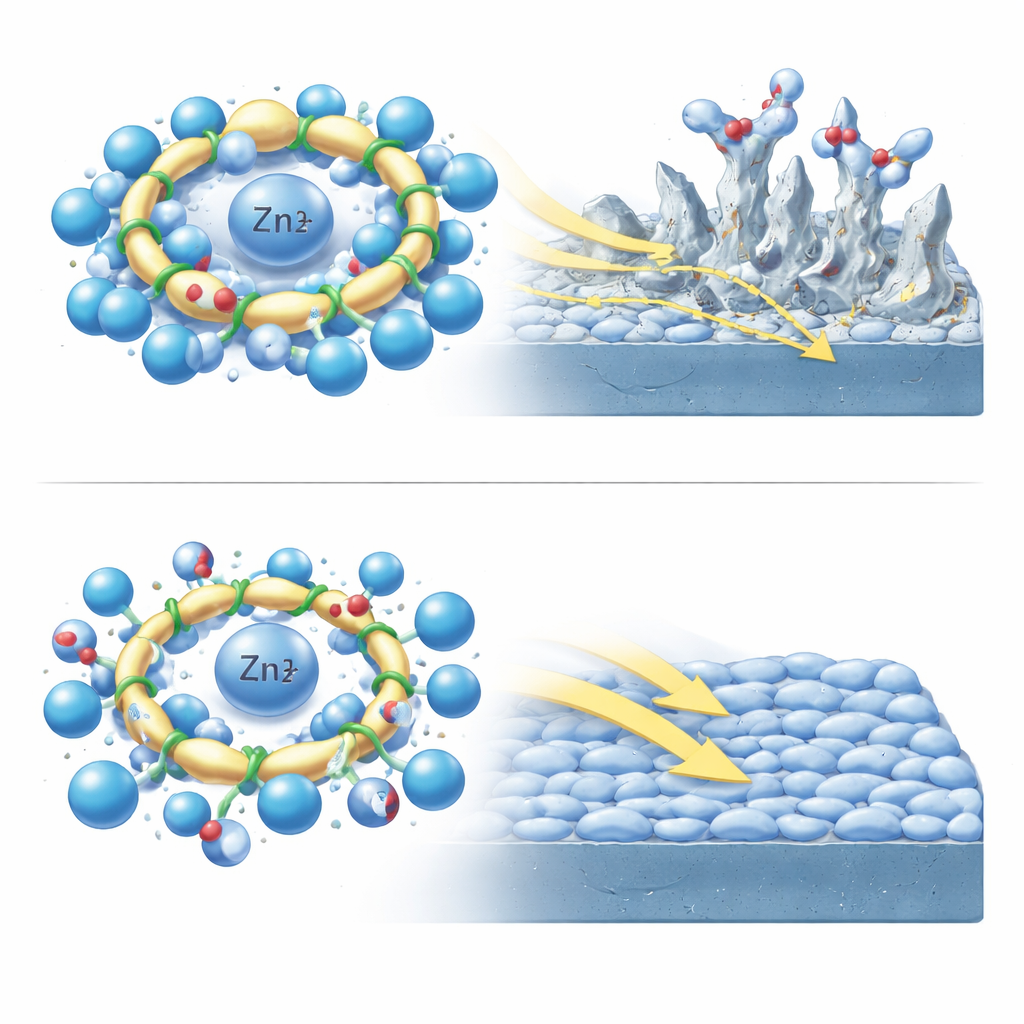
Des ajustements microscopiques à des cellules plus durables
Lorsque ces additifs ont été testés dans de véritables cellules zinc symétriques, les enseignements microscopiques se sont traduits par des gains spectaculaires. Dans une solution de sulfate de zinc seule, les cellules ont lâché après environ 130 heures de cyclage. Avec MI, la durée est passée à environ 1500 heures ; avec AP elle a atteint près de 1900 heures, tandis que les courants de corrosion ont diminué et que l’apparition de l’évolution de l’hydrogène s’est décalée vers des tensions plus négatives. La microscopie a montré que l’AP entraînait des dépôts de zinc plats et compacts au lieu de protubérances pointues. Pour le non-spécialiste, la conclusion est qu’une molécule à chaîne flexible, choisie par une recherche guidée par l’IA et validée par des simulations et des expériences détaillées, peut réarranger l’environnement liquide autour du zinc de sorte que les ions se déplacent rapidement, que les réactions secondaires ralentissent et que la batterie dure bien plus longtemps. Plus largement, l’étude illustre une feuille de route pour utiliser l’IA non seulement pour trouver des matériaux prometteurs, mais aussi pour comprendre pourquoi ils fonctionnent — offrant une voie puissante vers des solutions de stockage d’énergie meilleures et plus sûres.
Citation: Gao, Y., Sun, R., Shi, Y. et al. AI-assisted quantitative deciphering of molecular configuration and steric effects for high-performance zinc battery electrolytes. Commun Mater 7, 93 (2026). https://doi.org/10.1038/s43246-026-01100-5
Mots-clés: batteries aqueuses au zinc-ion, additifs pour électrolytes, intelligence artificielle en science des matériaux, structure de solvation, réseau de liaisons hydrogène