Clear Sky Science · es
Descifrado cuantitativo asistido por IA de la configuración molecular y los efectos estéricos para electrolitos de baterías de zinc de alto rendimiento
Baterías más inteligentes para un futuro renovable
A medida que se multiplican los paneles solares y los parques eólicos, necesitamos baterías asequibles y seguras que puedan almacenar grandes cantidades de energía durante horas o días. Las baterías acuosas de ion-zinc son especialmente atractivas porque el zinc es barato, abundante y funciona en electrolitos a base de agua en lugar de líquidos orgánicos inflamables. Pero las baterías de zinc actuales siguen sufriendo de vidas cortas y superficies metálicas inestables. Este estudio muestra cómo la inteligencia artificial puede cribar miles de moléculas candidatas para encontrar unas pocas que transforman silenciosamente la forma en que se mueven los iones de zinc en el líquido, alargando dramáticamente la vida útil de la batería.
Usar la IA para buscar en un mar de moléculas
Los autores parten de un problema familiar en química: hay muchas más moléculas orgánicas posibles de las que puede ensayar cualquier laboratorio por ensayo y error. Para afrontarlo, construyeron una gran base de datos de más de 20.000 moléculas pequeñas a partir de archivos químicos públicos y la vincularon a un sistema de IA basado en modelos de lenguaje de gran tamaño. Usando un método llamado generación aumentada por recuperación, la IA primero «leyó» y resumió 50 artículos recientes sobre baterías de zinc para extraer lo que realmente importa para los aditivos de electrolito—como cuán bien se disuelve una molécula en agua, dónde se sitúan sus grupos polares y cómo interactúa con los iones de zinc y la superficie metálica. Los investigadores luego diseñaron cuidadosamente los prompts para que la IA pudiera aplicar estas reglas derivadas de la literatura de forma consistente al cribar moléculas según tres criterios clave: estructuras sencillas en anillo o cadenas cortas, solubilidad acuosa moderada y los tipos adecuados de grupos químicos polares.
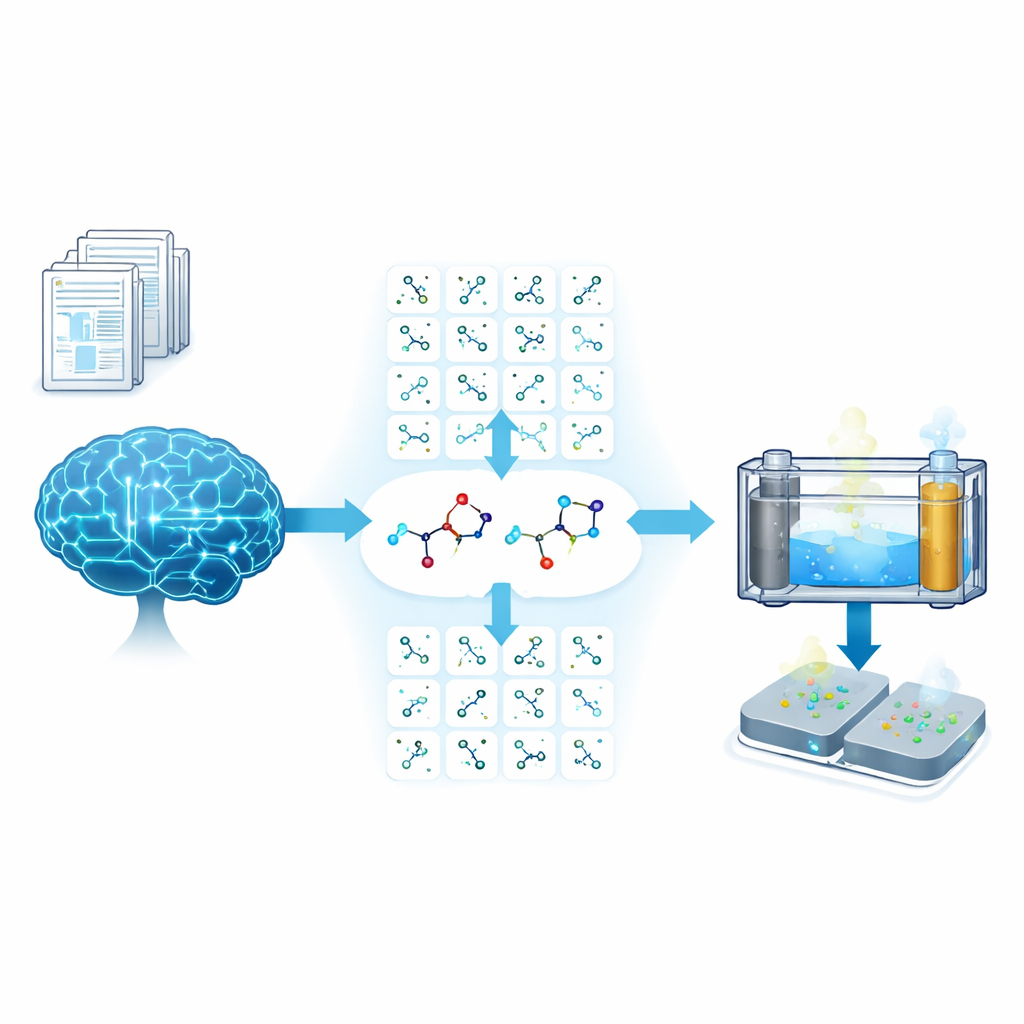
De miles de opciones a dos ayudantes destacados
El cribado inicial con IA redujo la enorme bolsa molecular a 18 candidatas prometedoras. Para afinar más la lista, el equipo realizó cálculos mecánico-cuánticos para cuantificar dos propiedades básicas: cuán fuertemente se une cada molécula a un ion de zinc y cuál es su masa molecular. Trazar la fuerza de unión frente al peso molecular les permitió identificar pares que eran similares en esos aspectos pero muy distintos en forma. De este enfoque emergieron dos moléculas como «socias de contraste» ideales: 2-metilimidazol (MI), un anillo rígido, y 3-aminopropanol (AP), una cadena flexible. Esta pareja permitió a los investigadores sondear con claridad cómo la forma molecular y el espacio que ocupa una molécula—sus llamados efectos estéricos—gobiernan la estructura microscópica alrededor de los iones de zinc y, en última instancia, el rendimiento de la batería.
Cómo la forma molecular dirige el movimiento iónico
Mediante simulaciones de dinámica molecular a gran escala, los autores observaron cómo MI y AP se sitúan en la primera capa de moléculas que rodea a un ion de zinc en agua. El anillo rígido de MI forma una jaula voluminosa e inflexible que obliga a las moléculas de agua circundantes a disponerse de forma apretada, elevando una especie de «barrera de entrada» para la reorganización del disolvente y limitando la facilidad con la que puede moverse el ion de zinc. En contraste, la cadena flexible de AP ajusta su conformación para adaptarse al entorno, construyendo una capa más compacta pero menos congestionada que permite que el agua y los iones se muevan con mayor libertad. AP también coordina con el zinc a través de múltiples sitios a lo largo de su cadena, incluyendo átomos de nitrógeno y oxígeno, lo que le permite estabilizar el ion y aún así dejar espacio para una migración rápida. Estas diferencias estructurales se propagan hacia afuera, alterando cuán estrechamente se agrupan los iones de zinc y sulfato, el paisaje electrostático que experimentan los iones y la manera en que las moléculas de agua forman y rompen enlaces de hidrógeno.
Reconstruyendo la red oculta del líquido
El equipo profundizó en el «cableado invisible» del electrolito: la red de enlaces de hidrógeno entre las moléculas de agua. En una solución simple de sulfato de zinc, las moléculas de agua están fuertemente enlazadas, lo que facilita que los protones salten rápidamente mediante el mecanismo de Grotthuss, alimentando la indeseada evolución de gas hidrógeno en la superficie de zinc. Añadir MI perturba esta red en cierta medida pero deja muchos caminos intactos. AP, con su cadena flexible y múltiples sitios de unión, hace mucho más: roba enlaces de hidrógeno a pares agua-agua, convierte muchos enlaces largos y débiles en enlaces más fuertes pero más localizados y reduce sustancialmente la respuesta dieléctrica global y las fluctuaciones de dipolo del líquido. Junto con energías de solvatación y desolvatación favorables y una fuerte adsorción en la superficie de zinc, este reordenamiento de la red de enlaces de hidrógeno calma las reacciones secundarias, reduce la barrera energética para el movimiento de iones de zinc y favorece que los iones se depositen de forma uniforme en lugar de formar dendritas tipo aguja.
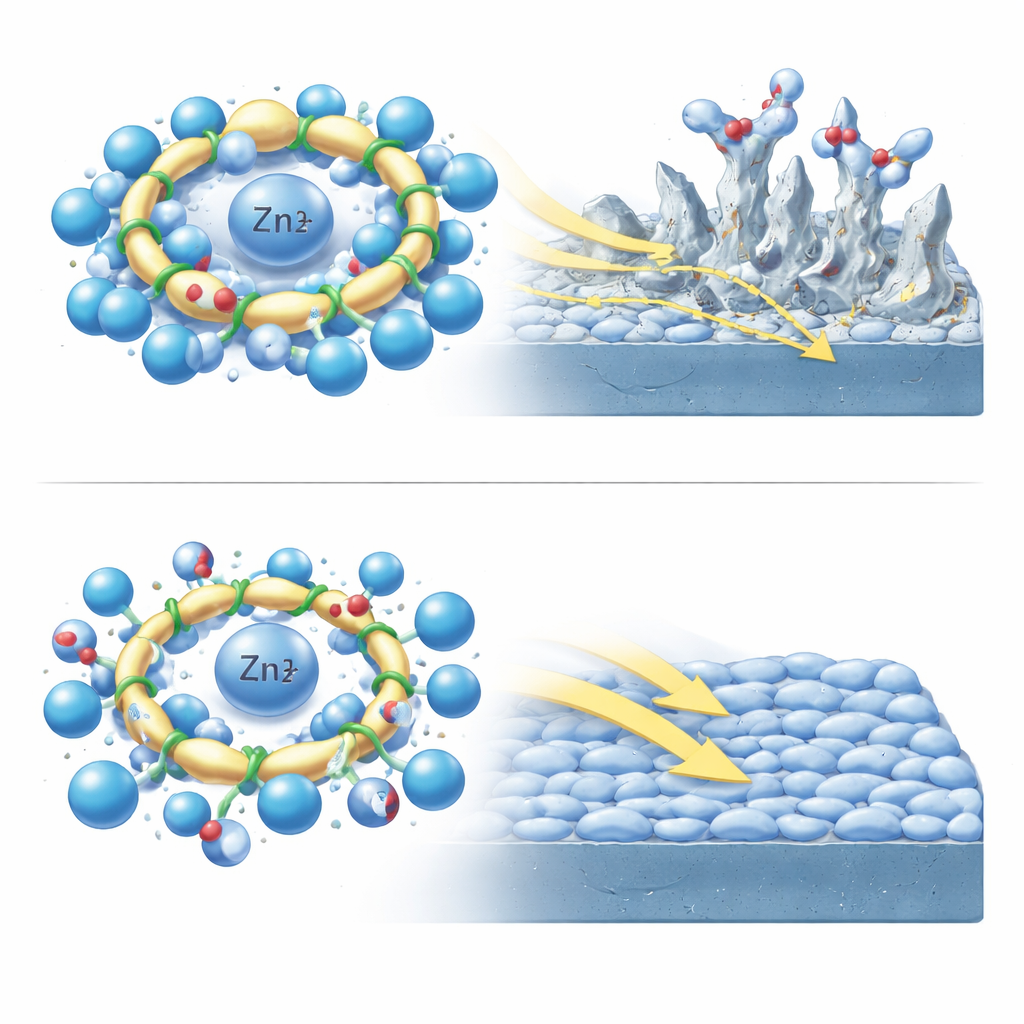
De ajustes microscópicos a celdas con mayor durabilidad
Cuando estos aditivos se probaron en celdas simétricas de zinc reales, las ideas microscópicas se tradujeron en ganancias sorprendentes. En sulfato de zinc simple, las celdas fallaban tras unas 130 horas de ciclo. Con MI, la vida se alargó hasta aproximadamente 1500 horas; con AP alcanzó unas 1900 horas, mientras que las corrientes de corrosión disminuyeron y el inicio de la evolución de hidrógeno se desplazó a voltajes más negativos. La microscopía mostró que AP condujo a depósitos de zinc planos y compactos en lugar de salientes afilados. Para un no especialista, la conclusión es que una molécula en forma de cadena flexible, elegida mediante una búsqueda guiada por IA y validada por simulaciones detalladas y experimentos, puede reorganizar el entorno líquido alrededor del zinc para que los iones se muevan rápidamente, las reacciones secundarias se ralenticen y la batería dure mucho más. En términos más amplios, el estudio muestra un plan para usar la IA no solo para buscar materiales prometedores, sino para entender por qué funcionan—ofreciendo un camino poderoso hacia tecnologías de almacenamiento de energía mejores y más seguras.
Cita: Gao, Y., Sun, R., Shi, Y. et al. AI-assisted quantitative deciphering of molecular configuration and steric effects for high-performance zinc battery electrolytes. Commun Mater 7, 93 (2026). https://doi.org/10.1038/s43246-026-01100-5
Palabras clave: baterías acuosas de ion-zinc, aditivos para electrolitos, inteligencia artificial en ciencia de materiales, estructura de solvatación, red de enlaces de hidrógeno