Clear Sky Science · fr
Cartographie à l’échelle cérébrale révèle des actions opioïdes temporelles et sexuellement dimorphes
Pourquoi c’est important pour la crise des opioïdes
Les médicaments opioïdes comme la morphine sont des analgésiques puissants, mais ils alimentent aussi une épidémie dévastatrice de dépendance. Pour mettre au point de meilleurs traitements, les scientifiques doivent savoir précisément comment ces drogues modifient l’activité à l’échelle de l’ensemble du cerveau, et comment ces effets diffèrent entre les hommes et les femmes et au fil du temps. Cette étude a utilisé des techniques d’imagerie 3D du cerveau de pointe chez la souris pour établir une carte cérébrale globale de l’impact de la morphine sur les cellules nerveuses, révélant quand, où et chez qui le médicament reconfigure le plus fortement l’activité cérébrale.
Voir tout le cerveau en une fois
Plutôt que de se concentrer sur quelques points chauds bien connus, les chercheurs ont entrepris de scanner l’ensemble du cerveau de la souris avec une résolution cellule par cellule. Après avoir injecté des souris mâles et femelles soit avec de la morphine soit avec une solution saline, ils ont prélevé les cerveaux une ou quatre heures plus tard. Les cerveaux ont été rendus optiquement transparents et marqués pour la protéine c‑Fos, qui s’allume dans les neurones récemment actifs. À l’aide de microscopes confocaux à grande vitesse, ils ont acquis d’immenses fichiers d’images 3D pour chaque cerveau entier. Un pipeline informatique personnalisé a ensuite détecté automatiquement les cellules lumineuses individuelles et aligné leurs positions sur un atlas standard du cerveau de souris, permettant à l’équipe de compter les cellules actives dans des centaines de régions nommées simultanément. 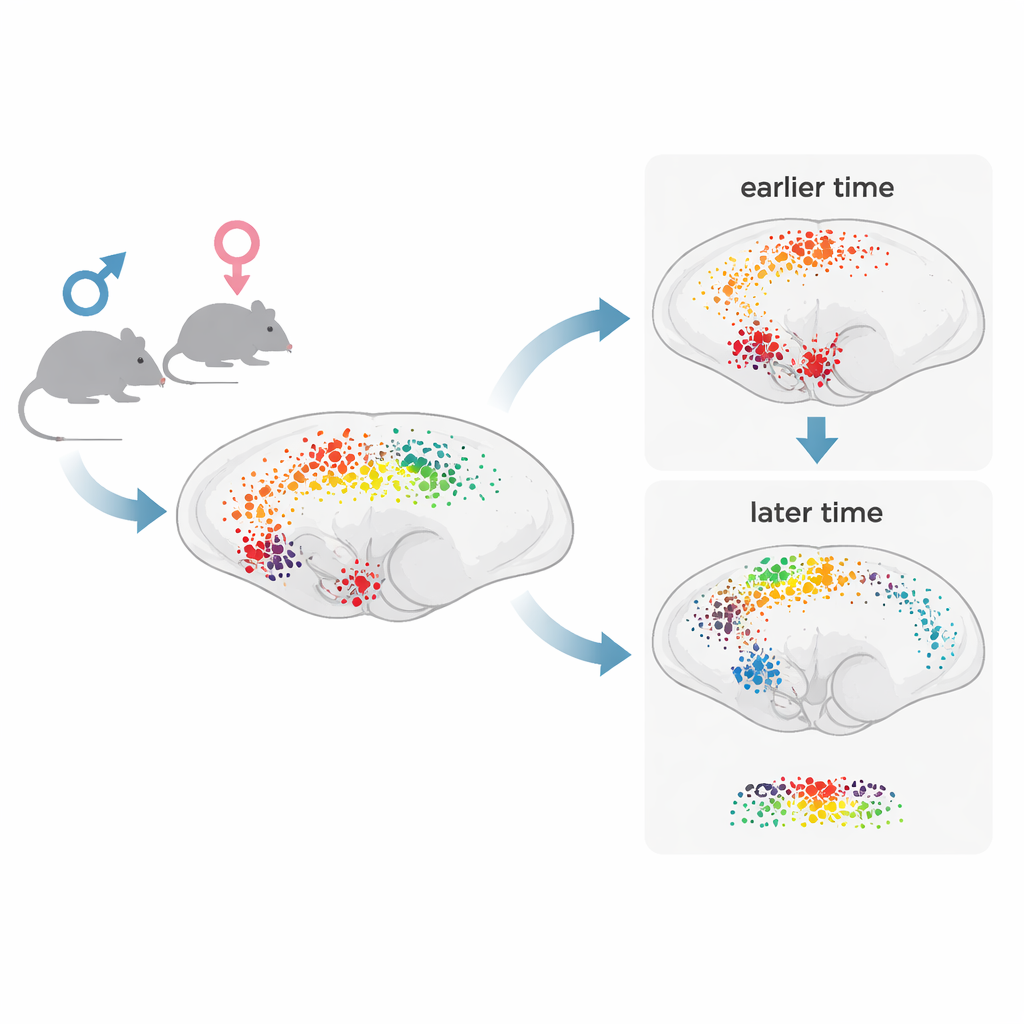
Comment les effets de la morphine se propagent dans le temps
Les cartes ont montré qu’une seule dose de morphine augmente globalement l’activité neuronale par rapport aux témoins, mais que toutes les régions ne réagissent pas de la même manière ni au même moment. Environ les deux tiers des structures cérébrales majeures présentaient plus de cellules actives après morphine, avec des réponses particulièrement fortes dans des régions profondes telles que le tronc cérébral, le pont et l’hypothalamus, ainsi qu’une activation dense dans certaines couches du cortex. À une heure, bon nombre des zones les plus réactives faisaient partie des circuits classiques de soulagement de la douleur et de la récompense, comme la substance grise périaqueducale, le noyau accumbens, l’aire tegmentale ventrale, les noyaux de relais thalamiques et des sites du tronc cérébral impliqués dans la modulation de la douleur et les fonctions corporelles. À quatre heures, moins de régions montraient de grands changements au niveau global, mais le motif d’activité avait évolué : les signaux s’étaient propagés de façon plus marquée vers des zones corticales et hippocampiques liées à l’apprentissage, la mémoire et l’adaptation à long terme. Cela soutient un modèle en « deux vagues » dans lequel une poussée précoce dans les circuits sous‑ corticaux est suivie d’une vague plus lente de plasticité corticale.
Réponses cérébrales différentes chez les mâles et les femelles
L’étude a également mis au jour des différences sexuelles marquées. En général, les mâles présentaient une activation induite par la morphine plus forte que les femelles dans de nombreuses régions clés liées à la récompense et au stress. Cela incluait le noyau accumbens, le septum latéral, le pallidum ventral, plusieurs noyaux de l’amygdale, le noyau du lit de la strie terminale et des parties de l’hippocampe et du cortex cingulaire. Chez les mâles, la morphine augmentait principalement l’activité aux deux points temporels. Chez les femelles, le tableau était plus complexe : les niveaux étaient souvent diminués à une heure puis plus élevés à quatre heures, ce qui reflète probablement des réponses au stress plus marquées liées à l’injection dans le groupe contrôle femelle et des différences dans la façon dont les récepteurs opioïdes s’apparient aux cellules cérébrales. Les données soulignent que la même dose de médicament peut mobiliser des réseaux partiellement différents dans les cerveaux mâle et femelle, en particulier dans des régions associées au craving, au sevrage, à l’humeur et au sommeil. 
Une nouvelle feuille de route pour étudier les drogues addictives
Au‑delà des centres d’addiction familiers, l’enquête à l’échelle du cerveau a révélé de nombreuses régions rarement associées aux opioïdes, comme certaines aires sensorielles et d’association corticales, des noyaux thalamiques et hypothalamiques spécifiques, des structures du tronc cérébral et même des parties du cervelet. Beaucoup de ces zones expriment des récepteurs opioïdes mais avaient été peu étudiées dans ce contexte. En combinant l’imagerie à grande échelle avec des modèles d’apprentissage automatique, les auteurs ont montré que prédire avec précision si une souris avait reçu de la morphine nécessite des informations provenant de nombreuses régions simultanément, ce qui souligne combien l’impact du médicament est réellement distribué. Pour un lecteur non spécialiste, la leçon à retenir est que la morphine ne « frappe » pas seulement un centre du plaisir : elle envoie des ondes à travers d’immenses réseaux cérébraux, le moment et le sexe façonnant les circuits les plus affectés. Cette nouvelle approche de cartographie offre un outil puissant pour cibler des régions cérébrales en vue de traitements antalgiques plus sûrs et de thérapies plus efficaces pour le trouble lié à l’usage d’opioïdes.
Citation: Vasylieva, I., Smith, R., Aravind, E. et al. Brain-wide mapping reveals temporal and sexually dimorphic opioid actions. Commun Biol 9, 466 (2026). https://doi.org/10.1038/s42003-026-09730-8
Mots-clés: dépendance aux opioïdes, cartographie cérébrale, différences entre les sexes, morphine, activité neuronale